1 . Ⅰ. 、
、 、
、 都是重要的能源物质,也是重要的化工原料。
都是重要的能源物质,也是重要的化工原料。
(1)下列事实能说明 分子呈正四面体结构的是_______(填字母)。
分子呈正四面体结构的是_______(填字母)。
(2)甲烷与下列烃的通式相同的是_______ (填字母)。_______ 。
②写出装置C中 与
与 反应生成氯仿(
反应生成氯仿( )的化学方程式
)的化学方程式_______ 。
③若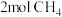 与
与 发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是
发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是_______ mol。
Ⅱ.用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(4)反应过程中的能量变化如下图所示。若生成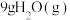 ,该反应会
,该反应会_____ (填“放出”或“吸收”)______ KJ热量。(用含有 、
、 的式子表示)
的式子表示) 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: 的浓度随时间变化曲线为
的浓度随时间变化曲线为_______ (填“a”、“b”或“c”),在M点,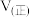
_______ 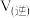 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②2min时,反应速率改变的原因可能是_______ 。
A.升高温度 B.降低温度 C.充入一定量的 D.加入催化剂
D.加入催化剂
 、
、 、
、 都是重要的能源物质,也是重要的化工原料。
都是重要的能源物质,也是重要的化工原料。(1)下列事实能说明
 分子呈正四面体结构的是_______(填字母)。
分子呈正四面体结构的是_______(填字母)。A. 分子的4个C—H共价键键长相等 分子的4个C—H共价键键长相等 | B. 分子中每个键角都是109°28′ 分子中每个键角都是109°28′ |
C.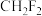 没有同分异构体 没有同分异构体 | D. 分子的沸点高于 分子的沸点高于 |
(2)甲烷与下列烃的通式相同的是
a. b.
b.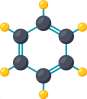 c.
c.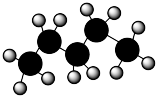 d.
d.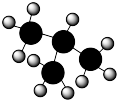
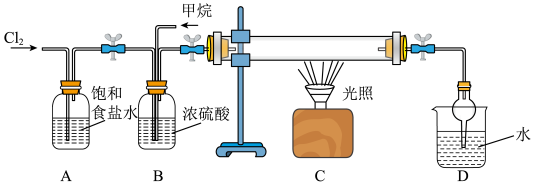
②写出装置C中
 与
与 反应生成氯仿(
反应生成氯仿( )的化学方程式
)的化学方程式③若
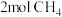 与
与 发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是
发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是Ⅱ.用
 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(4)反应过程中的能量变化如下图所示。若生成
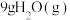 ,该反应会
,该反应会 、
、 的式子表示)
的式子表示)
 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: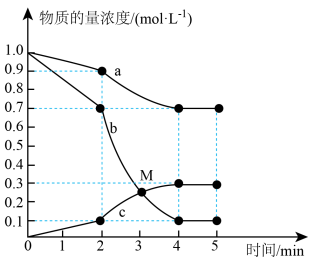
 的浓度随时间变化曲线为
的浓度随时间变化曲线为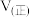
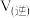 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②2min时,反应速率改变的原因可能是
A.升高温度 B.降低温度 C.充入一定量的
 D.加入催化剂
D.加入催化剂
您最近一年使用:0次
解题方法
2 . 回答下列问题
(1)对于在一个密闭容器中进行的反应 C(s)+H2O(g) = CO(g)+H2(g) ,下列条件的改变对反应速率几乎没有影响的是___________ 。
①增加C的量;②增加CO的量;③将容器的体积缩小一半; ④保持体积不变,充入 He以增大压强;⑤升高反应体系的温度; ⑥保持压强不变,充入 He 以增大体积。
(2)新型纳米材料氧缺位高铁酸盐( )能将烟气中
)能将烟气中 除去,原理如图所示。该过程中转化的
除去,原理如图所示。该过程中转化的 和消耗的
和消耗的 体积比为
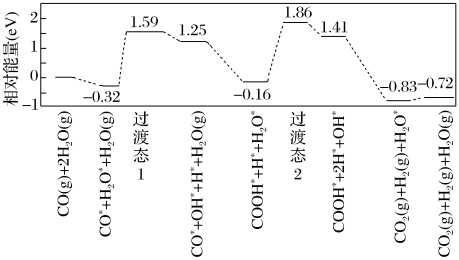
体积比为___________ 。___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=___________ eV,写出该步骤的化学方程式___________ 。
(1)对于在一个密闭容器中进行的反应 C(s)+H2O(g) = CO(g)+H2(g) ,下列条件的改变对反应速率几乎没有影响的是
①增加C的量;②增加CO的量;③将容器的体积缩小一半; ④保持体积不变,充入 He以增大压强;⑤升高反应体系的温度; ⑥保持压强不变,充入 He 以增大体积。
(2)新型纳米材料氧缺位高铁酸盐(
 )能将烟气中
)能将烟气中 除去,原理如图所示。该过程中转化的
除去,原理如图所示。该过程中转化的 和消耗的
和消耗的 体积比为
体积比为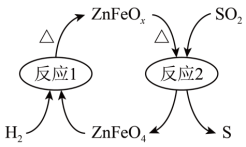
您最近一年使用:0次
解题方法
3 . 回答下列问题
(1)下列反应是氧化还原反应且是吸热反应的是___________ 。
A.稀醋酸与烧碱溶液的反应
B.灼热的炭与CO2的反应
C.铁片与稀盐酸反应
D.Ba(OH)2•8H2O与NH4Cl反应
E.干冰汽化
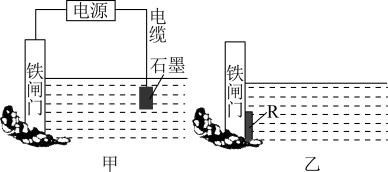
(2)实际生产生活中,钢铁等金属因电化学腐蚀损失巨大,而电化学在金属制备和加工中也发挥着重要的作用。生活中钢铁腐蚀以吸氧腐蚀为主,该腐蚀过程中正极的电极反应式为___________ 。金属的两种常见电化学防护方法如下图所示,图甲中铁闸门连接电源的___________ (填“正极”或“负极”),图乙所示金属的防护方法称为___________ 。
(1)下列反应是氧化还原反应且是吸热反应的是
A.稀醋酸与烧碱溶液的反应
B.灼热的炭与CO2的反应
C.铁片与稀盐酸反应
D.Ba(OH)2•8H2O与NH4Cl反应
E.干冰汽化
(2)实际生产生活中,钢铁等金属因电化学腐蚀损失巨大,而电化学在金属制备和加工中也发挥着重要的作用。生活中钢铁腐蚀以吸氧腐蚀为主,该腐蚀过程中正极的电极反应式为
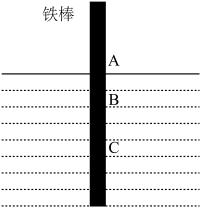
| A.铁棒AB段发生的反应为O2+2H2O+4e-=4OH- |
| B.腐蚀过程中在铁棒上会产生微电流,且方向是从BC段到AB段 |
| C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响 |
| D.产生这种现象的本质是铁棒所处的化学环境不同 |
您最近一年使用:0次
解题方法
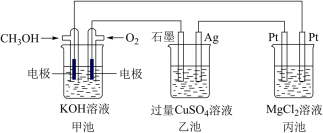
4 . 如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:___________ 。
(2)写出乙池石墨电极的名称为___________ (填“正极”“负极”或“阴极”“阳极”)。写出乙池中电解总反应的化学方程式:___________ 。
(3)甲池中消耗224 mL(标准状况下)O2,此时丙池中理论上最多产生___________ g沉淀,此时乙池中溶液的体积为400 mL,该溶液的pH=___________ 。
(4)若丙中电极不变,将其溶液换成NaOH溶液,开关闭合一段时间后,甲中溶液的pH将___________ (填“增大”“减小”或“不变”,下同),丙中溶液的pH将___________ 。
(5)某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图)。若用于制漂白液,a为电池的___________ 极,电解质溶液最好用___________ 。若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用___________ 作电极。阳极反应的电极方程式为___________ 。
(2)写出乙池石墨电极的名称为
(3)甲池中消耗224 mL(标准状况下)O2,此时丙池中理论上最多产生
(4)若丙中电极不变,将其溶液换成NaOH溶液,开关闭合一段时间后,甲中溶液的pH将
(5)某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图)。若用于制漂白液,a为电池的

您最近一年使用:0次
解题方法
5 . 化学电池的发明,是贮能和供能技术的巨大进步。
(1)如图所示装置中, 片是
片是_______ (填“正极”或“负极”),该极的电极反应式_______ 。_______ (写化学方程式)反应释放的能量直接转变为电能;能证明化学能转化为电能的实验现象是:电流表指针偏转、铜片上_______ 。
(1)如图所示装置中,
 片是
片是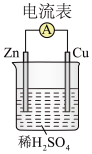
您最近一年使用:0次
名校
6 . 为了达到下表的实验目的,请选择合适的试剂及实验方法,并将其标号填入对应的空格。
A.加热升华
B.向溶液中加入足量CO2气体
C.分别加入品红溶液中,观察现象
D.分别加入紫色石蕊试剂中,观察现象
E.加入硫酸铜固体观察现象
| 序号 | 实验目的 | 试剂及方法 |
| (1) | 鉴别CO2和SO2气体 | |
| (2) | 除去食盐中混有的少量碘 | |
| (3) | 检验无水乙醇中是否含有水 | |
| (4) | 除去NaHCO3溶液中混有的Na2CO3 |
B.向溶液中加入足量CO2气体
C.分别加入品红溶液中,观察现象
D.分别加入紫色石蕊试剂中,观察现象
E.加入硫酸铜固体观察现象
您最近一年使用:0次
7 . 从A.苯、B.甲醛、C.乙酸、D.淀粉、E.氨基酸、F.碳酸钠、G.乙烯、H.甲烷8种有机物中选择合适的物质,将其标号填在横线上。
(1)最简单的芳香烃,难溶于水,易溶于有机溶剂,化学式为C6H6的是_______ 。
(2)作为细胞中碳水化合物最普遍的储藏形式,且遇碘水显蓝色的是_______ 。
(3)蛋白质水解可以得到_______ 。
(4)作为一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产:_______ 。
(5)含35%~40%的_______ 水溶液可用来浸制生物标本。
(6)食醋可作为增加食品酸味的调味剂,是因为其中含有_______ 。
(7)衡量一个国家石油工业发展水平的标志是_______ 。
(8)可燃冰的主要成分_______ 。
(1)最简单的芳香烃,难溶于水,易溶于有机溶剂,化学式为C6H6的是
(2)作为细胞中碳水化合物最普遍的储藏形式,且遇碘水显蓝色的是
(3)蛋白质水解可以得到
(4)作为一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产:
(5)含35%~40%的
(6)食醋可作为增加食品酸味的调味剂,是因为其中含有
(7)衡量一个国家石油工业发展水平的标志是
(8)可燃冰的主要成分
您最近一年使用:0次
8 . 按下列要求填空
(1)Cr原子的核外电子排布式______ 。
(2) 外围电子的轨道表示式
外围电子的轨道表示式______ 。
(3)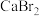 电子式
电子式______ 。 分子中所有原子均满足8电子构型,则其结构式为
分子中所有原子均满足8电子构型,则其结构式为______ 。
(4) 分子的空间结构为
分子的空间结构为______ 。
(5)如图所示为Zn的四种卤化物的熔点,据此判断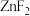 的晶体类型为
的晶体类型为______ , 微粒间的作用力为
微粒间的作用力为______ 。
(1)Cr原子的核外电子排布式
(2)
 外围电子的轨道表示式
外围电子的轨道表示式(3)
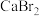 电子式
电子式 分子中所有原子均满足8电子构型,则其结构式为
分子中所有原子均满足8电子构型,则其结构式为(4)
 分子的空间结构为
分子的空间结构为(5)如图所示为Zn的四种卤化物的熔点,据此判断
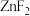 的晶体类型为
的晶体类型为 微粒间的作用力为
微粒间的作用力为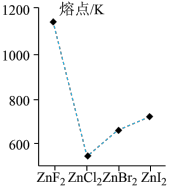
您最近一年使用:0次
名校
解题方法
9 . 茶是中国人喜爱的一种饮品,茶叶中含有铁元素,可以用以下实验操作检验茶叶中的铁元素:A.取少量茶叶;B.检验滤液中的 Fe3+;C.过滤得到滤液;D.将茶叶灼烧为茶叶灰;E.用足量稀盐酸溶解茶叶灰,并加蒸馏水稀释;请回答下列问题。
(1)上述实验操作的正确顺序是___________ (填字母)。
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、___________ 。
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式___________ 。
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式___________ 。
(1)上述实验操作的正确顺序是
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式
您最近一年使用:0次
10 . 硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)分别向Na2SiO3溶液中加入下列物质,能生成不溶于NaOH溶液的白色沉淀的是________ 。
①K ②稀盐酸 ③CaCl2溶液 ④KNO3溶液
(2)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·4H2O)等化合物。写出三硅酸镁的氧化物形式为_______________ 。
(3)为什么实验室中盛放NaOH溶液的试剂瓶不能用玻璃塞(用离子方程式表示):_________________ 。
(4)当前制备高纯硅的主要生产过程示意图如下:_________________ 。
②高纯硅的用途:_____________ 。(写出一种)
③整个制备过程必须严格控制无水无氧。H2还原SiHCl3过程中若混有O2,可能引起的后果是_______________ 。
(1)分别向Na2SiO3溶液中加入下列物质,能生成不溶于NaOH溶液的白色沉淀的是
①K ②稀盐酸 ③CaCl2溶液 ④KNO3溶液
(2)胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·4H2O)等化合物。写出三硅酸镁的氧化物形式为
(3)为什么实验室中盛放NaOH溶液的试剂瓶不能用玻璃塞(用离子方程式表示):
(4)当前制备高纯硅的主要生产过程示意图如下:

②高纯硅的用途:
③整个制备过程必须严格控制无水无氧。H2还原SiHCl3过程中若混有O2,可能引起的后果是
您最近一年使用:0次



