1 . 利用 制甲醇具有重要意义。其过程可能发生的反应如下:
制甲醇具有重要意义。其过程可能发生的反应如下:
反应1: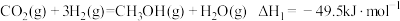
反应2:
反应3: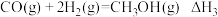
(1)
_______ 
(2)恒容条件下,下列有利于提高 平衡产率的条件是_______。
平衡产率的条件是_______。
(3)控制一定压强,通入 和
和 ,反应
,反应 后,
后, 转化率
转化率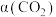 、
、 产率
产率 及
及 产率
产率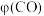 随温度变化曲线如图。
随温度变化曲线如图。
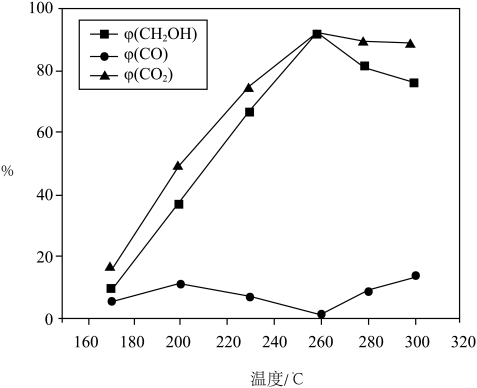
①温度升高, 先升高后降低的原因是
先升高后降低的原因是_______ 。
②260℃时,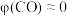 (认为此时只发生反应1),
(认为此时只发生反应1),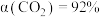 ,气体总体积为
,气体总体积为 ,则该温度下反应1的平衡常数
,则该温度下反应1的平衡常数
_______ (列出代数式即可),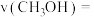
_______ (列出代数式即可)。
③280℃时, ,
, ,则反应2的平衡常数
,则反应2的平衡常数
_______ (列出代数式即可)。
(4)学界关于反应2产生的 能否发生反应3存在争议。科学家利用
能否发生反应3存在争议。科学家利用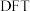 模拟
模拟 催化剂表面合成
催化剂表面合成 的两种不同路径,其决速步及活化能
的两种不同路径,其决速步及活化能 分别如下。
分别如下。
路径1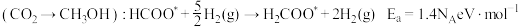
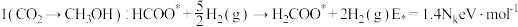 路径2
路径2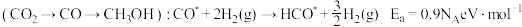
由此分析,200~260℃时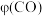 降低的原因是
降低的原因是_______ 。
 制甲醇具有重要意义。其过程可能发生的反应如下:
制甲醇具有重要意义。其过程可能发生的反应如下:反应1:
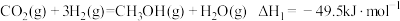
反应2:

反应3:
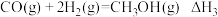
(1)


(2)恒容条件下,下列有利于提高
 平衡产率的条件是_______。
平衡产率的条件是_______。| A.使用催化剂 | B.调整 和 和 的投料比由1∶1至1∶3 的投料比由1∶1至1∶3 |
| C.增大反应物总压 | D.通入稀有气体 |
 和
和 ,反应
,反应 后,
后, 转化率
转化率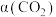 、
、 产率
产率 及
及 产率
产率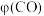 随温度变化曲线如图。
随温度变化曲线如图。
①温度升高,
 先升高后降低的原因是
先升高后降低的原因是②260℃时,
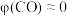 (认为此时只发生反应1),
(认为此时只发生反应1),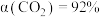 ,气体总体积为
,气体总体积为 ,则该温度下反应1的平衡常数
,则该温度下反应1的平衡常数
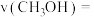
③280℃时,
 ,
, ,则反应2的平衡常数
,则反应2的平衡常数
(4)学界关于反应2产生的
 能否发生反应3存在争议。科学家利用
能否发生反应3存在争议。科学家利用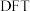 模拟
模拟 催化剂表面合成
催化剂表面合成 的两种不同路径,其决速步及活化能
的两种不同路径,其决速步及活化能 分别如下。
分别如下。路径1
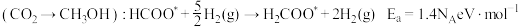
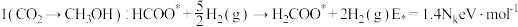 路径2
路径2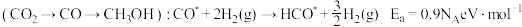
由此分析,200~260℃时
 降低的原因是
降低的原因是
您最近一年使用:0次
2 . 化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,1g甲醇 在氧气中充分燃烧生成二氧化碳和液态水释放出
在氧气中充分燃烧生成二氧化碳和液态水释放出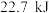 的热量,写出甲醇燃烧的热化学方程式
的热量,写出甲醇燃烧的热化学方程式_______ 。
(2)已知反应CH3-CH3(g) → CH2=CH2(g)+H2(g),有关化学键的键能如下。
试计算该反应的反应热
_______ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变
_______ 。
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+ O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
(4)根据能量变化示意图:
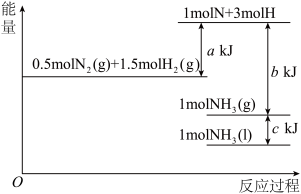
写出N2(g)+3H2(g)=2NH3(l)
_______ 
(1)实验测得,1g甲醇
 在氧气中充分燃烧生成二氧化碳和液态水释放出
在氧气中充分燃烧生成二氧化碳和液态水释放出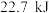 的热量,写出甲醇燃烧的热化学方程式
的热量,写出甲醇燃烧的热化学方程式(2)已知反应CH3-CH3(g) → CH2=CH2(g)+H2(g),有关化学键的键能如下。
| 化学键 | C-H |  |  | H-H | |
键能 | 414.4 | 615.3 | 347.3 | 435.3 |

(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变

①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+
 O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1(4)根据能量变化示意图:

写出N2(g)+3H2(g)=2NH3(l)


您最近一年使用:0次
3 . 有效除去大气中的 和氮氧化物,是打赢蓝天保卫战的重中之重。
和氮氧化物,是打赢蓝天保卫战的重中之重。
某温度下, 气体在一体积固定的密闭容器中发生如下反应:
气体在一体积固定的密闭容器中发生如下反应: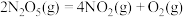 (慢反应)
(慢反应)  ,
,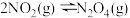 (快反应)
(快反应)  ,体系的总压强
,体系的总压强 和
和 随时间的变化如图所示:
随时间的变化如图所示:

(1)图中表示 压强变化的曲线是
压强变化的曲线是________ (填“甲”或“乙”)。
(2)已知 分解的反应速率
分解的反应速率 ,
, 时,
时,
________  ,
,
________ 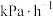 (结果保留两位小数,下同)。
(结果保留两位小数,下同)。
(3)该温度下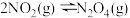 反应的平衡常数
反应的平衡常数
________  (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
 和氮氧化物,是打赢蓝天保卫战的重中之重。
和氮氧化物,是打赢蓝天保卫战的重中之重。某温度下,
 气体在一体积固定的密闭容器中发生如下反应:
气体在一体积固定的密闭容器中发生如下反应: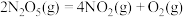 (慢反应)
(慢反应)  ,
,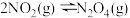 (快反应)
(快反应)  ,体系的总压强
,体系的总压强 和
和 随时间的变化如图所示:
随时间的变化如图所示:
(1)图中表示
 压强变化的曲线是
压强变化的曲线是(2)已知
 分解的反应速率
分解的反应速率 ,
, 时,
时,
 ,
,
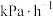 (结果保留两位小数,下同)。
(结果保留两位小数,下同)。(3)该温度下
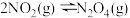 反应的平衡常数
反应的平衡常数
 (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
您最近一年使用:0次
2023-02-14更新
|
565次组卷
|
4卷引用:2020届福建高三化学总复习——-压强平衡常数辅助练习
2020届福建高三化学总复习——-压强平衡常数辅助练习专题5.3 化学计算(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专项特训3 多平衡体系的综合分析(已下线)03 常考题空3 分压平衡常数(Kp)计算 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
解题方法
4 . 为测定某 溶液的浓度,取
溶液的浓度,取 待测液,向其中加入过量
待测液,向其中加入过量 溶液。充分反应后过滤、洗涤并干燥,得到
溶液。充分反应后过滤、洗涤并干燥,得到 沉淀的质量为
沉淀的质量为 ,反应的化学方程式为
,反应的化学方程式为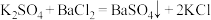 。求该溶液中
。求该溶液中 的物质的量浓度
的物质的量浓度_______ (请写出计算过程)。
 溶液的浓度,取
溶液的浓度,取 待测液,向其中加入过量
待测液,向其中加入过量 溶液。充分反应后过滤、洗涤并干燥,得到
溶液。充分反应后过滤、洗涤并干燥,得到 沉淀的质量为
沉淀的质量为 ,反应的化学方程式为
,反应的化学方程式为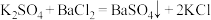 。求该溶液中
。求该溶液中 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
解题方法
5 . 填空。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式_______ 。
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=_______ kJ∙mol-1。
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
则N2(g)+O2(g)=2NO(g) ΔH=_______ kJ·mol-1。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
| 物质 | N2 | O2 | NO |
| 能量(kJ·mol-1) | 946 | 498 | 632 |
您最近一年使用:0次
6 . 现欲利用锌粒和稀盐酸制取标准状况下33.6LH2,则至少需消耗锌粒多少克_______ ?消耗稀盐酸中HCl的物质的量是多少_______ ?
您最近一年使用:0次
7 . 回答下列问题
(1)m gH2 含有n个H2分子,则阿伏加德罗常数为_______ (用含m和n表示)。
(2)在8克某物质中含有3.01×1023个分子,该物质的相对分子质量为:_______ 。
(3)若O2和O3的质量相等,则其物质的量之比_______ ,原子数之比 _______ 。
(4)标准状况下有CH43.36L,则该CH4气体的物质的量为_______ ,质量为_______ ,所含氢原子的物质的量为_______ ,所含质子的物质的量为_______ 。
(1)m gH2 含有n个H2分子,则阿伏加德罗常数为
(2)在8克某物质中含有3.01×1023个分子,该物质的相对分子质量为:
(3)若O2和O3的质量相等,则其物质的量之比
(4)标准状况下有CH43.36L,则该CH4气体的物质的量为
您最近一年使用:0次
解题方法
8 . 把11.2 L(标准状况)HCl气体溶于水,配制成250mL的溶液,求:
(1)该溶液的物质的量浓度_____
(2)将该溶液与足量的锌反应,在标准状况下,能生成多少升的H2_____ ? (反应的化学方程式为 Zn + 2HCl = ZnCl2 + H2↑)
(1)该溶液的物质的量浓度
(2)将该溶液与足量的锌反应,在标准状况下,能生成多少升的H2
您最近一年使用:0次
名校
9 . 回答下列问题:
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是______(填序号)。
,该反应一定是______(填序号)。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: 。结合素材回答问题(2)~(4):
。结合素材回答问题(2)~(4):
(2)该反应中 的摩尔质量是
的摩尔质量是______
(3)28g铁粉中含有的Fe原子数是______ 。
(4)若28g铁粉完全反应,析出Cu单质的质量为______ 。
素材II.宋代《洗冤集录》中记载有“银针探毒”,其原理是: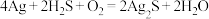 。结合素材回答问题(5)~(6):
。结合素材回答问题(5)~(6):
(5)在相同条件下体积相同的 和
和 两种气体分子数之比为
两种气体分子数之比为______ 。
(6)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的 的体积是
的体积是______ 。
素材III.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: 。结合素材回答问题(7)~(8):
。结合素材回答问题(7)~(8):
(7)该反应中,化合价升高的元素是______ (填元素符号)。
(8)该反应中,作为氧化剂的物质是______ (填化学式)。
(9)向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
该雨水中氢离子的浓度a=______ 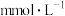 。
。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与
 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是______(填序号)。
,该反应一定是______(填序号)。| A.离子反应 | B.分解反应 | C.氧化还原反应 | D.置换反应 |
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:
 。结合素材回答问题(2)~(4):
。结合素材回答问题(2)~(4):(2)该反应中
 的摩尔质量是
的摩尔质量是(3)28g铁粉中含有的Fe原子数是
(4)若28g铁粉完全反应,析出Cu单质的质量为
素材II.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
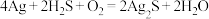 。结合素材回答问题(5)~(6):
。结合素材回答问题(5)~(6):(5)在相同条件下体积相同的
 和
和 两种气体分子数之比为
两种气体分子数之比为(6)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的
 的体积是
的体积是素材III.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
 。结合素材回答问题(7)~(8):
。结合素材回答问题(7)~(8):(7)该反应中,化合价升高的元素是
(8)该反应中,作为氧化剂的物质是
(9)向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:离子 |
|
|
|
|
|
浓度( | 0.06 | 0.08 | 0.02 | 0.04 | a |
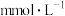 。
。
您最近一年使用:0次
2022-12-13更新
|
198次组卷
|
2卷引用:福建省厦门市第十中学2022-2023学年高一上学期期中考试化学试题
10 . 回答下列问题:
(1)0.5molSO2,含有的分子数为_______ 个,质量为_______ g,标准状况下体积为_______ L。
(2)标准状况下,14g N2所占有的体积为_______ L,所含氮原子个数为_______ 个。
(3)标准状况下,2mol NH3与_______ g CO2的体积相等。
(4)中和含0.2mol HCl的稀盐酸,需NaOH物质的量为_______ mol,如改用KOH,则所需KOH的质量为_______ g。
(5)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量为_______ 。
(6)在22.2g某二价金属的氯化物(RCl2)中含Cl- 离子0.4mol,则RCl2的摩尔质量为_______ ,R的相对原子质量为_______ 。
(1)0.5molSO2,含有的分子数为
(2)标准状况下,14g N2所占有的体积为
(3)标准状况下,2mol NH3与
(4)中和含0.2mol HCl的稀盐酸,需NaOH物质的量为
(5)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量为
(6)在22.2g某二价金属的氯化物(RCl2)中含Cl- 离子0.4mol,则RCl2的摩尔质量为
您最近一年使用:0次








