名校
1 . C、N、O、S、H、Na都是中学化学中常见的元素。按要求完成下列填空。
(1)2molC2H6O分子中含_______ mol碳原子、_______ 个氢原子。
(2)0.5NA个H2SO4分子的质量为____ ;0.1molAl2(SO4)3所含SO 的物质的量为
的物质的量为_____ 。
(3)等物质的量的NH3和N2两种气体,所含原子数之比为_______ ,等质量的NH3和N2物质的量之比为_______ 。
(4)24.8gNa2R含Na+0.8mol,则Na2R物质的量为_______ ,摩尔质量为_______ 。
(1)2molC2H6O分子中含
(2)0.5NA个H2SO4分子的质量为
 的物质的量为
的物质的量为(3)等物质的量的NH3和N2两种气体,所含原子数之比为
(4)24.8gNa2R含Na+0.8mol,则Na2R物质的量为
您最近一年使用:0次
名校
2 . 请按要求填空。
(1)标准状况下44.8L的CO2物质的量为_______ 。
(2)在14.2gNa2SO4中:含有的Na+的数目是_______ ;含有的 的质量是
的质量是_______ ;
(3)含13.8gNa+的Na3PO4溶液100mL, 的物质的量浓度为
的物质的量浓度为_______ ;
(4)已知反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,现有1.92g铜和足量稀硝酸完全反应,产生气体在标准状况下的体积是_______ 。
(1)标准状况下44.8L的CO2物质的量为
(2)在14.2gNa2SO4中:含有的Na+的数目是
 的质量是
的质量是(3)含13.8gNa+的Na3PO4溶液100mL,
 的物质的量浓度为
的物质的量浓度为(4)已知反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,现有1.92g铜和足量稀硝酸完全反应,产生气体在标准状况下的体积是
您最近一年使用:0次
3 . 已知在800 K时,反应:CO(g)+H2O(g)⇌H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%。求:
(1)800 K时该反应的平衡常数_______ ;
(2)如果将H2O的初始浓度加大为6 mol·L-1,求此时CO转化为CO2的转化率______ 。
(1)800 K时该反应的平衡常数
(2)如果将H2O的初始浓度加大为6 mol·L-1,求此时CO转化为CO2的转化率
您最近一年使用:0次
4 . 回答下列问题:
(1)_______ 克NH3分子中所含氢原子数与0.3NA个水分子中所含氢原子数相等。
(2)已知O2和CO2的混合气体,标准状况下体积为11.2L,质量为18g,则该混合气体与相同状况下的CO的密度之比为_______ 。
(3)38g某二价金属氯化物ACl2中含有0.8molCl-,则A的相对原子质量是_______ 。
(4)100mL浓度为1.2mol/L的硫酸与6.5g锌充分反应后,最多可以收集到标准状况下氢气的体积_______ L。
(5)某同学制备氢氧化铁胶体的实验过程为:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至混合液呈红褐色。请写出该过程的化学反应方程式:_______ 。
(1)
(2)已知O2和CO2的混合气体,标准状况下体积为11.2L,质量为18g,则该混合气体与相同状况下的CO的密度之比为
(3)38g某二价金属氯化物ACl2中含有0.8molCl-,则A的相对原子质量是
(4)100mL浓度为1.2mol/L的硫酸与6.5g锌充分反应后,最多可以收集到标准状况下氢气的体积
(5)某同学制备氢氧化铁胶体的实验过程为:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至混合液呈红褐色。请写出该过程的化学反应方程式:
您最近一年使用:0次
名校
5 . 回答下列问题:
(1)写出 的电离方程式
的电离方程式_________ 。
(2) 个
个 含
含_________ mol氧原子,氧原子的质量为_________ 。
(3)在同温同压条件下, 和
和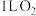 的物质的量之比为
的物质的量之比为_________ ,分子个数之比是_________ 。
(4)有 溶液,从该溶液中取出10mL,则
溶液,从该溶液中取出10mL,则
_________ ,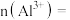
_________ 。
(5)用 氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
氧化溶质质量分数为36.5%的盐酸。反应方程式如下: ;问题:
;问题: 至少能消耗HCl的物质的量为
至少能消耗HCl的物质的量为_________ mol?被氧化的HCl为_________ mol?
(6)在无土栽培中,配制1L内含 、
、 、
、 的某营养液。若用KCl、
的某营养液。若用KCl、 、
、 配制,则需这三种固体物质的量分别为
配制,则需这三种固体物质的量分别为_________ mol、_________ mol、_________ mol。
(1)写出
 的电离方程式
的电离方程式(2)
 个
个 含
含(3)在同温同压条件下,
 和
和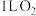 的物质的量之比为
的物质的量之比为(4)有
 溶液,从该溶液中取出10mL,则
溶液,从该溶液中取出10mL,则
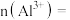
(5)用
 氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
氧化溶质质量分数为36.5%的盐酸。反应方程式如下: ;问题:
;问题: 至少能消耗HCl的物质的量为
至少能消耗HCl的物质的量为(6)在无土栽培中,配制1L内含
 、
、 、
、 的某营养液。若用KCl、
的某营养液。若用KCl、 、
、 配制,则需这三种固体物质的量分别为
配制,则需这三种固体物质的量分别为
您最近一年使用:0次
解题方法
6 . 完成下列问题
(1)3.01×1023个氯气分子的物质的量是_______ ,质量为_______ ;
(2)1.5 mol Na2SO4·10H2O中所含的Na+的物质的量是_______ ,所含的SO 的物质的量是
的物质的量是_______ ,所含H2O的数目是_______ ;
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为_______ ;
(4)0.5 mol NaOH中含有电子的物质的量是_______ ,在_______ mol Na2CO3中所含Na+数目与上述0.5 mol NaOH所含Na+数目相等。
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ ,含R的质量为1.6g的Na2R,其物质的量为_______ ;
(6)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为_______ ;
(7)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为_______ mol,CO占总质量的_______ %(结果取整数)
(1)3.01×1023个氯气分子的物质的量是
(2)1.5 mol Na2SO4·10H2O中所含的Na+的物质的量是
 的物质的量是
的物质的量是(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(4)0.5 mol NaOH中含有电子的物质的量是
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为
(6)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(7)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为
您最近一年使用:0次
7 . t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g),△H=-196.6kJ/mol。 2min时反应达到化学平衡,此时测得反应物O2还乘余0.8mol。求:
2SO3(g),△H=-196.6kJ/mol。 2min时反应达到化学平衡,此时测得反应物O2还乘余0.8mol。求:
(1)从反应开始到达化学平衡,生成SO3的平均反应速率_________ 。
(2)t℃时该反应的化学平衡常数_________ 。
(3)平衡时SO2转化率_________ 。
 2SO3(g),△H=-196.6kJ/mol。 2min时反应达到化学平衡,此时测得反应物O2还乘余0.8mol。求:
2SO3(g),△H=-196.6kJ/mol。 2min时反应达到化学平衡,此时测得反应物O2还乘余0.8mol。求:(1)从反应开始到达化学平衡,生成SO3的平均反应速率
(2)t℃时该反应的化学平衡常数
(3)平衡时SO2转化率
您最近一年使用:0次
名校
8 . 根据物质的量等相关物理量回答下列问题:
(1)_______ mol 所含氢原子数与
所含氢原子数与 所含氢原子数相等。
所含氢原子数相等。
(2)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为_______ 。
(3)20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为_______ 。
(4)NO和 可以发生反应
可以发生反应 ,若反应生成
,若反应生成 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为_______ mol。若有a molNO与b mol 充分反应,则反应后氮原子与氧原子的个数比为
充分反应,则反应后氮原子与氧原子的个数比为_______ (用含a、b的代数式表示)。
(5)36gCO与 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与 的混合气体的总物质的量为
的混合气体的总物质的量为_______ mol,其中的CO在标准状况下的体积为_______ L。
(1)
 所含氢原子数与
所含氢原子数与 所含氢原子数相等。
所含氢原子数相等。(2)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为(3)20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为
(4)NO和
 可以发生反应
可以发生反应 ,若反应生成
,若反应生成 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为 充分反应,则反应后氮原子与氧原子的个数比为
充分反应,则反应后氮原子与氧原子的个数比为(5)36gCO与
 的混合气体与足量
的混合气体与足量 充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与
充分反应后,将所得气体通入过量的澄清石灰水中,生成白色沉淀的质量为100g,则36gCO与 的混合气体的总物质的量为
的混合气体的总物质的量为
您最近一年使用:0次
名校
9 . 根据所学知识,回答下列问题:
(1)含0.1NA个 的
的 中有
中有______ 个电子。
(2)氢原子物质的量相等的 和
和 的物质的量之比为
的物质的量之比为______ 。
(3)将8.0g 溶于水配成500mL溶液,则所得溶液的物质的量浓度为
溶于水配成500mL溶液,则所得溶液的物质的量浓度为______ 。
(4)现有16.0g CO和 的混合气体,在标准状况下其体积为8.96L。请回答下列问题:
的混合气体,在标准状况下其体积为8.96L。请回答下列问题:
①混合气体中碳原子的个数为______ (用NA表示阿伏加德罗常数的值)。
②将混合气体依次通过如图所示装置,最后收集在气球中(体积在标准状况下测定)。
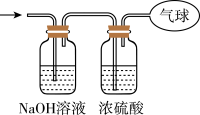
A.气球中收集到的气体的摩尔质量为______ 。
B.气球的体积为______ 。
(1)含0.1NA个
 的
的 中有
中有(2)氢原子物质的量相等的
 和
和 的物质的量之比为
的物质的量之比为(3)将8.0g
 溶于水配成500mL溶液,则所得溶液的物质的量浓度为
溶于水配成500mL溶液,则所得溶液的物质的量浓度为(4)现有16.0g CO和
 的混合气体,在标准状况下其体积为8.96L。请回答下列问题:
的混合气体,在标准状况下其体积为8.96L。请回答下列问题:①混合气体中碳原子的个数为
②将混合气体依次通过如图所示装置,最后收集在气球中(体积在标准状况下测定)。

A.气球中收集到的气体的摩尔质量为
B.气球的体积为
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题(用NA表示阿伏加德罗常数的值)
(1)9.03 1023个CO2在标准状况下的体积为
1023个CO2在标准状况下的体积为_______ ,质量是_______ 。
(2)3.4gNH3与标准状况下的_______ L的H2S含有相同数目的氢原子。
(3)在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示。

该混合液中CaCl2的物质的量为_______ ;
(4)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。回答问题:
①该混合气体的平均摩尔质量为_______ 。
②混合气体中碳原子的个数为_______ 。
(1)9.03
 1023个CO2在标准状况下的体积为
1023个CO2在标准状况下的体积为(2)3.4gNH3与标准状况下的
(3)在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示。

该混合液中CaCl2的物质的量为
(4)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。回答问题:
①该混合气体的平均摩尔质量为
②混合气体中碳原子的个数为
您最近一年使用:0次



