甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:
①

②

③

(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
由此计算
_______  ;已知
;已知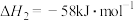 ,则
,则
_______  。
。
(2)已知在常温常压下:
①
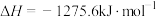
②
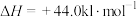
写出表示甲醇燃烧热的热化学方程式_______ 。
(3)已知常温时红磷比白磷稳定,已知:
① (白磷,s)
(白磷,s)

②4P(红磷,s)

比较反应中 的大小:
的大小:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)人体内葡萄糖的消耗可用下列热化学方程式表示:
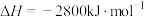 ;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为_______ 。
 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:①


②


③


(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
E/ | 436 | 343 | 1076 | 465 | 413 |

 ;已知
;已知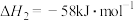 ,则
,则
 。
。(2)已知在常温常压下:
①

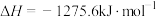
②

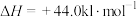
写出表示甲醇燃烧热的热化学方程式
(3)已知常温时红磷比白磷稳定,已知:
①
 (白磷,s)
(白磷,s)

②4P(红磷,s)


比较反应中
 的大小:
的大小:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)人体内葡萄糖的消耗可用下列热化学方程式表示:

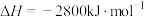 ;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
更新时间:2022-10-30 17:28:04
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的热化学方程式:
(1)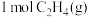 与适量
与适量 反应,生成
反应,生成 和
和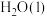 ,放出
,放出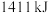 的热。
的热。___________ 。
(2)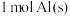 与适量
与适量 发生反应,生成
发生反应,生成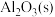 ,放出
,放出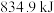 的热。
的热。___________ 。
(1)
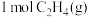 与适量
与适量 反应,生成
反应,生成 和
和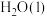 ,放出
,放出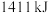 的热。
的热。(2)
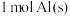 与适量
与适量 发生反应,生成
发生反应,生成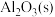 ,放出
,放出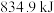 的热。
的热。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)已知甲烷和汽油(可用 C8H18表示)的燃烧的热化学方程式:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ/mol;
C8H18(l)+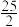 O2(g)═8CO2(g)+9H2O(l)△H=﹣5472kJ/mol;
O2(g)═8CO2(g)+9H2O(l)△H=﹣5472kJ/mol;
则等质量的甲烷和汽油燃烧,产生的热量比较多的是___________ (填“甲烷”或“汽油”)
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成 SiO2和液态 H2O。已知室温下 2gSiH4自燃放出热量 89.2kJ.SiH4自燃的热化学方程式为____________________ .
(3)1molH2(g)和1mol Cl2(g)在一定条件下反应生成2 mol HCl(g),放出184.5kJ的热量,已知断裂1molH2(g)中的H-H和1mol Cl2(g)中的Cl-Cl分别需要吸收436.4kJ和242.7kJ的能量,则1mol HCl分子中的化学键形成时释放_________ kJ的能量。
(1)已知甲烷和汽油(可用 C8H18表示)的燃烧的热化学方程式:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ/mol;
C8H18(l)+
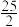 O2(g)═8CO2(g)+9H2O(l)△H=﹣5472kJ/mol;
O2(g)═8CO2(g)+9H2O(l)△H=﹣5472kJ/mol;则等质量的甲烷和汽油燃烧,产生的热量比较多的是
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成 SiO2和液态 H2O。已知室温下 2gSiH4自燃放出热量 89.2kJ.SiH4自燃的热化学方程式为
(3)1molH2(g)和1mol Cl2(g)在一定条件下反应生成2 mol HCl(g),放出184.5kJ的热量,已知断裂1molH2(g)中的H-H和1mol Cl2(g)中的Cl-Cl分别需要吸收436.4kJ和242.7kJ的能量,则1mol HCl分子中的化学键形成时释放
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某实验小组在T1温度下,向容积为1L的恒容密闭容器中,同时通入0.1mol CO(g)和0.1mol H2O(g),发生反应:CO(g)+H2O(g) CO2(g)+H2(g)△H=a kJ·mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
CO2(g)+H2(g)△H=a kJ·mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。

(1)0~10min内,CO的平均反应速率为_____________
(2)T1温度下,该反应的平衡常数K为_______________ (用分数表示)。
(3)已知:I.H2的燃烧热 △H=-285.8 kJ·mol-1;
II.CO的燃烧热 △H=-283 kJ·mol-1;
III.H2O(g) H2O(l) △H=-44 kJ·mol-1。则a=
H2O(l) △H=-44 kJ·mol-1。则a=______________
(4)T1温度下,某时刻另一实验小组测得反应容器中有关数据为c(CO)=0.6 mol·L-1、c(H2O)=1.6 mol·L-1、c(H2)=0.4 mol·L-1、c(CO2)=0.4 mol·L-1,则该反应在下一时刻将_______ (填“向正反应方向进行”“向逆反应方向进行”或“达到平衡”),判断依据是___________________ 。
 CO2(g)+H2(g)△H=a kJ·mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
CO2(g)+H2(g)△H=a kJ·mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
(1)0~10min内,CO的平均反应速率为
(2)T1温度下,该反应的平衡常数K为
(3)已知:I.H2的燃烧热 △H=-285.8 kJ·mol-1;
II.CO的燃烧热 △H=-283 kJ·mol-1;
III.H2O(g)
 H2O(l) △H=-44 kJ·mol-1。则a=
H2O(l) △H=-44 kJ·mol-1。则a=(4)T1温度下,某时刻另一实验小组测得反应容器中有关数据为c(CO)=0.6 mol·L-1、c(H2O)=1.6 mol·L-1、c(H2)=0.4 mol·L-1、c(CO2)=0.4 mol·L-1,则该反应在下一时刻将
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)已知H2(g)+Br2(1)=2HBr(g) △H=-72kJ/mol,蒸发1mol Br2(1)需要吸收的能量为30kJ,其它相关数据如下表:
①Br2(1)=Br2(g) △H1,则△H1=_______ ;
②写出H2(g)与Br2(g)反应生成HBr(g)的热化学方程式:_______
③试计算a=_______ 。
(2)磷在氧气中燃烧,可能生成两种固态氧化物。3.1g的单质磷(P)在一定量氧气中燃烧生成P2O3、P2O5各0.025mol,反应物完全耗尽,并放出X kJ热量。
①已知1mol磷完全燃烧生成稳定氧化物放出的热量为Y kJ,则1molP与O2反应生成固态P2O3的反应热△H=_______ 。
②写出1mol P与O2反应生成固态P2O3的热化学方程式:_______
H2(g) | Br2(g) | HBr(g) | |
键能/kJ·mol-1 | 436 | a | 369 |
①Br2(1)=Br2(g) △H1,则△H1=
②写出H2(g)与Br2(g)反应生成HBr(g)的热化学方程式:
③试计算a=
(2)磷在氧气中燃烧,可能生成两种固态氧化物。3.1g的单质磷(P)在一定量氧气中燃烧生成P2O3、P2O5各0.025mol,反应物完全耗尽,并放出X kJ热量。
①已知1mol磷完全燃烧生成稳定氧化物放出的热量为Y kJ,则1molP与O2反应生成固态P2O3的反应热△H=
②写出1mol P与O2反应生成固态P2O3的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】依据事实,写出下列反应的热化学方程式。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为_____________________________ 。
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为____________________________ 。
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为___________________ 。相同状况下,能量较低的是_____________ 。
(4)③C(s)+ O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____ 。写出CO燃烧的热化学方程式__________ 。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为
(4)③C(s)+
 O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:
①C(s,石墨)+O2(g) =CO2(g) ΔH1=-393.5 kJ•mol−1;
②2H2(g)+O2(g) =2H2O(l) ΔH2=-571.6 kJ•mol−1;
③2C2H2(g)+5O2(g) =4CO2(g)+2H2O(l) ΔH3=-2599 kJ•mol−1。
298K时反应2C(s,石墨)+H2(g)=C2H2(g)的焓变:ΔH=___ 。
(2)已知:
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1=-2983.2kJ•mol−1;
②P(红磷,s)+ O2(g)=
O2(g)=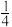 P4O10(s) ΔH2 =-738.5kJ•mol−1;
P4O10(s) ΔH2 =-738.5kJ•mol−1;
白磷的稳定性比红磷___ (填“高”或“低”)。
(3)下列热化学方程式书写正确的是(ΔH的绝对值均正确)___ 。
A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1367.0kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3kJ·mol-1(中和热)
C.S(s)+O2(g)=SO2(g) ΔH=-296.8kJ·mol-1 (燃烧热)
D.2NO2=O2+2NO ΔH=+116.2kJ·mol-1(反应热)
已知:
①C(s,石墨)+O2(g) =CO2(g) ΔH1=-393.5 kJ•mol−1;
②2H2(g)+O2(g) =2H2O(l) ΔH2=-571.6 kJ•mol−1;
③2C2H2(g)+5O2(g) =4CO2(g)+2H2O(l) ΔH3=-2599 kJ•mol−1。
298K时反应2C(s,石墨)+H2(g)=C2H2(g)的焓变:ΔH=
(2)已知:
①P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1=-2983.2kJ•mol−1;
②P(红磷,s)+
 O2(g)=
O2(g)=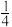 P4O10(s) ΔH2 =-738.5kJ•mol−1;
P4O10(s) ΔH2 =-738.5kJ•mol−1;白磷的稳定性比红磷
(3)下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1367.0kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3kJ·mol-1(中和热)
C.S(s)+O2(g)=SO2(g) ΔH=-296.8kJ·mol-1 (燃烧热)
D.2NO2=O2+2NO ΔH=+116.2kJ·mol-1(反应热)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜)=S(s,斜方) ΔH= -0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是____ [填“S(单斜)”或“S(斜方)”]。
(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH= -183 kJ·mol-1,则HCl(g)= H2(g)+
H2(g)+ Cl2(g) ΔH=
Cl2(g) ΔH=______ ,若破坏1 molH-H键需消耗的能量436kJ,破坏1 molH-Cl键需消耗的能量431kJ,则破坏1 molCl-Cl键需消耗的能量是_________ 。
(3)标准状况下,6.72 L C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2燃烧热的热化学方程式:____ 。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变为______ 。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成1 mol N2理论上放出的热量为____ 。

(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH= -183 kJ·mol-1,则HCl(g)=
 H2(g)+
H2(g)+ Cl2(g) ΔH=
Cl2(g) ΔH=(3)标准状况下,6.72 L C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成1 mol N2理论上放出的热量为

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算。
已知:P4(固体.白磷)+5O2(气体)= P4O10(固体) △H=-2983.2kJ·mol-1①
P(固体.红磷)+5/4 O2(气体)=1/4 P4O10(固体) △H=-738.5kJ·mol-1②
由热化学方程式来看,更稳定的磷的同素异形体是_______ 。试写出白磷转化为红磷的热化学方程式________________________ 。
已知:P4(固体.白磷)+5O2(气体)= P4O10(固体) △H=-2983.2kJ·mol-1①
P(固体.红磷)+5/4 O2(气体)=1/4 P4O10(固体) △H=-738.5kJ·mol-1②
由热化学方程式来看,更稳定的磷的同素异形体是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜) S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是______ (填“S(单斜)”或“S(斜方)”)。
(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为____ kJ·mol-1。
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:____________________________ 。
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为____ kJ·mol-1 (用含a,b,c的式子表示)。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为__________ 。

 S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
| 化学键 | H—H | H—Cl |
| 键能 | 436 | 431 |
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)已知H2(g)+Br2(1)=2HBr(g) △H=-72kJ/mol,蒸发1mol Br2(1)需要吸收的能量为30kJ,其它相关数据如下表:
①Br2(1)=Br2(g) △H1,则△H1=_______ ;
②写出H2(g)与Br2(g)反应生成HBr(g)的热化学方程式:_______
③试计算a=_______ 。
(2)磷在氧气中燃烧,可能生成两种固态氧化物。3.1g的单质磷(P)在一定量氧气中燃烧生成P2O3、P2O5各0.025mol,反应物完全耗尽,并放出X kJ热量。
①已知1mol磷完全燃烧生成稳定氧化物放出的热量为Y kJ,则1molP与O2反应生成固态P2O3的反应热△H=_______ 。
②写出1mol P与O2反应生成固态P2O3的热化学方程式:_______
H2(g) | Br2(g) | HBr(g) | |
键能/kJ·mol-1 | 436 | a | 369 |
①Br2(1)=Br2(g) △H1,则△H1=
②写出H2(g)与Br2(g)反应生成HBr(g)的热化学方程式:
③试计算a=
(2)磷在氧气中燃烧,可能生成两种固态氧化物。3.1g的单质磷(P)在一定量氧气中燃烧生成P2O3、P2O5各0.025mol,反应物完全耗尽,并放出X kJ热量。
①已知1mol磷完全燃烧生成稳定氧化物放出的热量为Y kJ,则1molP与O2反应生成固态P2O3的反应热△H=
②写出1mol P与O2反应生成固态P2O3的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式: ___________ 。
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2+3H2 2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:
2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:__________ 。
(3)以CO作还原剂与磷石膏反应,不同反应温度下可得到不同的产物。向盛有CaSO4的真空恒容密闭容器中充入CO,且c初始(CO)=1×10-4mol·L-1,反应体系起始总压强为0.1a MPa, 1150℃下,反应:CaSO4(s) + CO(g) CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=
CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=________ MPa(用含a的代数式表示;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;忽略副反应)。
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应N2+3H2
 2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:
2NH3 △H=a kJ·mol-1。试根据表中所列键能数据计算a 的数值:(3)以CO作还原剂与磷石膏反应,不同反应温度下可得到不同的产物。向盛有CaSO4的真空恒容密闭容器中充入CO,且c初始(CO)=1×10-4mol·L-1,反应体系起始总压强为0.1a MPa, 1150℃下,反应:CaSO4(s) + CO(g)
 CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=
CaO(s) + CO2(g) + SO2(g)达到平衡时, CO的转化率为80%,该反应的压强平衡常数Kp=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】由化学能产生热能是目前人类使用能源的主要途径。回答下列问题:
(1)如图表示反应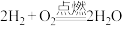 的能量变化。
的能量变化。

已知断开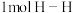 键、
键、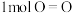 键和
键和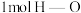 键分别需要消耗
键分别需要消耗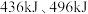 和
和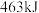 的能量。则反应过程(Ⅱ)中生成
的能量。则反应过程(Ⅱ)中生成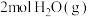 时放出能量
时放出能量______ kJ能量。
(2)已知某温度下 的溶解热为
的溶解热为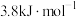 (吸热)
(吸热)

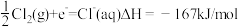
写出该温度下钠在氯气中燃烧的热化学方程式___________ 。
(3) 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为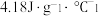 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。)请计算:
,忽略溶液体积、质量变化和金属吸收的热量。)请计算:
①该反应放出的热量
____ J。
②反应 的
的
_____  。
。
(1)如图表示反应
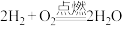 的能量变化。
的能量变化。
已知断开
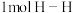 键、
键、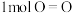 键和
键和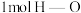 键分别需要消耗
键分别需要消耗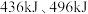 和
和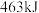 的能量。则反应过程(Ⅱ)中生成
的能量。则反应过程(Ⅱ)中生成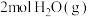 时放出能量
时放出能量(2)已知某温度下
 的溶解热为
的溶解热为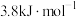 (吸热)
(吸热)
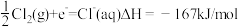
写出该温度下钠在氯气中燃烧的热化学方程式
(3)
 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。(已知:反应前后,溶液的比热容均近似为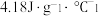 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。)请计算:
,忽略溶液体积、质量变化和金属吸收的热量。)请计算:①该反应放出的热量

②反应
 的
的
 。
。
您最近一年使用:0次



