依据事实,写出下列反应的热化学方程式。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为_____________________________ 。
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为____________________________ 。
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为___________________ 。相同状况下,能量较低的是_____________ 。
(4)③C(s)+ O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____ 。写出CO燃烧的热化学方程式__________ 。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为
(4)③C(s)+
 O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
更新时间:2018-09-26 22:09:54
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___ 。
(2)25℃、101kPa若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量___ 。
(3)25℃、101kPa已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___ 。
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算△H1=___ kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=___ kJ·mol-1。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)25℃、101kPa若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量
(3)25℃、101kPa已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C O O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
③H2(g)+ O2(g)=H2O(l) △H3=-285.8kJ/mol
O2(g)=H2O(l) △H3=-285.8kJ/mol
(1)试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=_____
(2)CH3COOH(l)的燃烧热是________
(3)在③式中,当有71.45kJ的热量放出时需要燃烧标准状况下的H2______ 升。
Ⅱ.已知下列两个热化学方程式:
2H2(g)+O2(g)=2H2O(1) △H=-570.kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是_______ 。
(2)已知:H2O(1)=H2O(g) △H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式______ 。
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
③H2(g)+
 O2(g)=H2O(l) △H3=-285.8kJ/mol
O2(g)=H2O(l) △H3=-285.8kJ/mol(1)试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
(2)CH3COOH(l)的燃烧热是
(3)在③式中,当有71.45kJ的热量放出时需要燃烧标准状况下的H2
Ⅱ.已知下列两个热化学方程式:
2H2(g)+O2(g)=2H2O(1) △H=-570.kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是
(2)已知:H2O(1)=H2O(g) △H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜) S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是______ (填“S(单斜)”或“S(斜方)”)。
(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为____ kJ·mol-1。
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:____________________________ 。
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为____ kJ·mol-1 (用含a,b,c的式子表示)。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为__________ 。

 S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
| 化学键 | H—H | H—Cl |
| 键能 | 436 | 431 |
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
③H2(g)+ O2(g)=H2O(l) △H3=-285.8kJ/mol
O2(g)=H2O(l) △H3=-285.8kJ/mol
(1)试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=_____
(2)CH3COOH(l)的燃烧热是________
(3)在③式中,当有71.45kJ的热量放出时需要燃烧标准状况下的H2______ 升。
Ⅱ.已知下列两个热化学方程式:
2H2(g)+O2(g)=2H2O(1) △H=-570.kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是_______ 。
(2)已知:H2O(1)=H2O(g) △H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式______ 。
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
③H2(g)+
 O2(g)=H2O(l) △H3=-285.8kJ/mol
O2(g)=H2O(l) △H3=-285.8kJ/mol(1)试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
(2)CH3COOH(l)的燃烧热是
(3)在③式中,当有71.45kJ的热量放出时需要燃烧标准状况下的H2
Ⅱ.已知下列两个热化学方程式:
2H2(g)+O2(g)=2H2O(1) △H=-570.kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则混合气体中H2和C3H8的体积比是
(2)已知:H2O(1)=H2O(g) △H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷(P4)和P4O6的分子结构如图所示,

已知:
则反应P4(g)+3O2(g)= P4O6(g)的△H=_________ 。
(2)已知①2C(s)+O2(g)=2CO(g) △H= -221.0 kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H= -483.6 kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+ H2(g)的△H=_______ 。

已知:
| 化学键 | P—P | P—O | O=O |
| 键能(kJ·mol1) | 198 | 360 | 498 |
则反应P4(g)+3O2(g)= P4O6(g)的△H=
(2)已知①2C(s)+O2(g)=2CO(g) △H= -221.0 kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H= -483.6 kJ/mol
则制备水煤气的反应C(s)+H2O(g)=CO(g)+ H2(g)的△H=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】还原法处理氮的氧化物是环境科学研究的热点课题。氢气还原法:H2还原NO发生的反应为:2NO(g)+2H2(g)  N2(g)+2H2O(g)。已知几种化学键的键能数据如下:
N2(g)+2H2O(g)。已知几种化学键的键能数据如下:
2NO(g)+2H2(g) N2(g)+2H2O(g) ΔH=
N2(g)+2H2O(g) ΔH=_______ kJ·mol-1。
 N2(g)+2H2O(g)。已知几种化学键的键能数据如下:
N2(g)+2H2O(g)。已知几种化学键的键能数据如下:化学键 | H—H | NO中的共价键 | N≡N | H—O |
键能(kJ·mol-1) | 436 | 630 | 946 | 463 |
2NO(g)+2H2(g)
 N2(g)+2H2O(g) ΔH=
N2(g)+2H2O(g) ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】研究化学反应中的能量变化具有重要的意义。回答下列问题:
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
①由上述热化学方程式可知甲醇的燃烧热△H=____________ 。
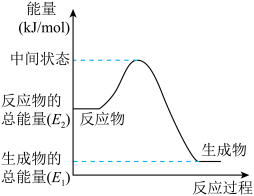
②上述第二个反应的能量变化如图所示,则△H2=___________ k/mol。(用E1、E2的相关式子表示)。.
(2)已知反应N2(g)+3H2(g) 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=________ 。
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是__________ (填化学式)。
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:_____________ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol①由上述热化学方程式可知甲醇的燃烧热△H=
②上述第二个反应的能量变化如图所示,则△H2=

(2)已知反应N2(g)+3H2(g)
 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列热化学方程式:
(1)汽车尾气中的主要污染物是NO和CO,已知:
I 2CO(g)+O2(g) = 2CO2(g) ΔH 1= -566.0kJ•mol-1
II 2NO(g) = N2(g)+O2(g) ΔH 2= -180.8kJ•mol-1;
则将汽车尾气处理成无毒无害产物的热化学方程式为___________ 。
(2)最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知298K时断裂1molN≡N键吸收942 kJ热量,生成1molN-N放出167 kJ热量。根据以上信息和数据,则由气态N2生成1 mol气态N4的的热化学方程式为___________ 。

(1)汽车尾气中的主要污染物是NO和CO,已知:
I 2CO(g)+O2(g) = 2CO2(g) ΔH 1= -566.0kJ•mol-1
II 2NO(g) = N2(g)+O2(g) ΔH 2= -180.8kJ•mol-1;
则将汽车尾气处理成无毒无害产物的热化学方程式为
(2)最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知298K时断裂1molN≡N键吸收942 kJ热量,生成1molN-N放出167 kJ热量。根据以上信息和数据,则由气态N2生成1 mol气态N4的的热化学方程式为

您最近一年使用:0次



