同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算。
已知:P4(固体.白磷)+5O2(气体)= P4O10(固体) △H=-2983.2kJ·mol-1①
P(固体.红磷)+5/4 O2(气体)=1/4 P4O10(固体) △H=-738.5kJ·mol-1②
由热化学方程式来看,更稳定的磷的同素异形体是_______ 。试写出白磷转化为红磷的热化学方程式________________________ 。
已知:P4(固体.白磷)+5O2(气体)= P4O10(固体) △H=-2983.2kJ·mol-1①
P(固体.红磷)+5/4 O2(气体)=1/4 P4O10(固体) △H=-738.5kJ·mol-1②
由热化学方程式来看,更稳定的磷的同素异形体是
11-12高二上·福建福州·阶段练习 查看更多[1]
(已下线)2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷
更新时间:2011-10-27 16:25:21
|
相似题推荐
【推荐1】回答下列问题:
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g)=CO2(g) ΔH1 B(s)+O2(g)=CO2(g) ΔH2
若ΔH1 >ΔH2 ,则两种同素异形体中较稳定的是(填“A”或“B”)_____
(2)根据以下三个热化学方程式:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol;2H2S(g)+O2(g)=2S(s)+2H2O(l) ΔH=-Q2 kJ/mol;2H2S(g)+O2(g)=2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。判断Q1、Q2、Q3三者关系为________________
(3)工业上用H2和Cl2反应制HCl,各键能数据为:H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是___________________________________
(4)已知充分燃烧 乙炔
乙炔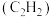 气体生成液态水和1mol二氧化碳气体时,放出热量
气体生成液态水和1mol二氧化碳气体时,放出热量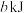 ,则下列关于乙炔气体燃烧热的热化学方程式
,则下列关于乙炔气体燃烧热的热化学方程式___________________________________
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g)=CO2(g) ΔH1 B(s)+O2(g)=CO2(g) ΔH2
若ΔH1 >ΔH2 ,则两种同素异形体中较稳定的是(填“A”或“B”)
(2)根据以下三个热化学方程式:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol;2H2S(g)+O2(g)=2S(s)+2H2O(l) ΔH=-Q2 kJ/mol;2H2S(g)+O2(g)=2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。判断Q1、Q2、Q3三者关系为
(3)工业上用H2和Cl2反应制HCl,各键能数据为:H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是
(4)已知充分燃烧
 乙炔
乙炔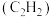 气体生成液态水和1mol二氧化碳气体时,放出热量
气体生成液态水和1mol二氧化碳气体时,放出热量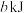 ,则下列关于乙炔气体燃烧热的热化学方程式
,则下列关于乙炔气体燃烧热的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应过程中释放或吸收的热量在生活、生产、科技及科学研究中具有广泛应用。
(1)“神舟”系列火箭用偏二甲肼( )作燃料,
)作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。
反应1: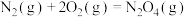

反应2: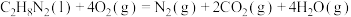
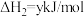
写出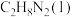 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:__________________ 。
(2)已知,在25℃和101KPa下,部分化学键的键能数据如表所示。
①25℃和101KPa下,工业合成氨的反应中每生成1 mol  就会放出46 kJ热量,在该条件下,向某容器中加入2 mol
就会放出46 kJ热量,在该条件下,向某容器中加入2 mol  、6 mol
、6 mol  及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是________________ ,表中的a=______ 。
②科学家发现了一种新的气态分子 (图),在25℃和101 KPa下,
(图),在25℃和101 KPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为______________________ ,由此可知 与
与 中更稳定的是
中更稳定的是______ (填化学式)。

③已知:
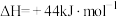 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为_________________________ 。
(1)“神舟”系列火箭用偏二甲肼(
 )作燃料,
)作燃料, 作氧化剂,反应后产物无污染。
作氧化剂,反应后产物无污染。反应1:
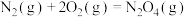

反应2:
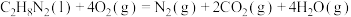
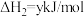
写出
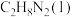 和
和 反应生成
反应生成 、
、 、
、 的热化学方程式:
的热化学方程式:(2)已知,在25℃和101KPa下,部分化学键的键能数据如表所示。
| 化学键 | H-H | H-N |  | O=O | C-H | C=O | H-O | N-N |
键能( ) ) | 436 | 391 | a | 498 | 414 | 803 | 462 | 193 |
 就会放出46 kJ热量,在该条件下,向某容器中加入2 mol
就会放出46 kJ热量,在该条件下,向某容器中加入2 mol  、6 mol
、6 mol  及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是
及合适的催化剂,充分反应后测得其放出的热量小于92 kJ,原因可能是②科学家发现了一种新的气态分子
 (图),在25℃和101 KPa下,
(图),在25℃和101 KPa下, 转化为
转化为 的热化学方程式为
的热化学方程式为 与
与 中更稳定的是
中更稳定的是
③已知:

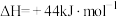 。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
。甲烷是一种常用燃料,则表示甲烷的燃烧热的热化学方程式为
您最近一年使用:0次
【推荐3】甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:
①

②

③

(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
由此计算
_______  ;已知
;已知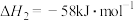 ,则
,则
_______  。
。
(2)已知在常温常压下:
①
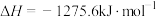
②
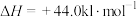
写出表示甲醇燃烧热的热化学方程式_______ 。
(3)已知常温时红磷比白磷稳定,已知:
① (白磷,s)
(白磷,s)

②4P(红磷,s)

比较反应中 的大小:
的大小:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)人体内葡萄糖的消耗可用下列热化学方程式表示:
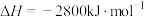 ;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为_______ 。
 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:①


②


③


(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
E/ | 436 | 343 | 1076 | 465 | 413 |

 ;已知
;已知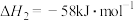 ,则
,则
 。
。(2)已知在常温常压下:
①

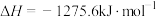
②

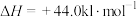
写出表示甲醇燃烧热的热化学方程式
(3)已知常温时红磷比白磷稳定,已知:
①
 (白磷,s)
(白磷,s)

②4P(红磷,s)


比较反应中
 的大小:
的大小:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)人体内葡萄糖的消耗可用下列热化学方程式表示:

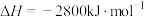 ;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】甲醛是一种重要的化工产品,可利用甲醇脱氢制备,反应式如下:
CH3OH(g)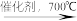 CH2O(g)+ H2(g)
CH2O(g)+ H2(g) 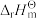 = 84.2 kJ ·mol-1 (1)
= 84.2 kJ ·mol-1 (1)
向体系中通入空气,通过以下反应提供反应(1)所需热量:
H2(g)+ O2(g)
O2(g) H2O(g)
H2O(g) 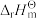 =- 241.8 2 kJ ·mol-1 (2)
=- 241.8 2 kJ ·mol-1 (2)
要使反应温度维持在700°C,计算进料中甲醇与空气的摩尔数之比。已知空气中氧气的体积分数为0.20。___________
CH3OH(g)
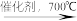 CH2O(g)+ H2(g)
CH2O(g)+ H2(g) 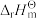 = 84.2 kJ ·mol-1 (1)
= 84.2 kJ ·mol-1 (1)向体系中通入空气,通过以下反应提供反应(1)所需热量:
H2(g)+
 O2(g)
O2(g) H2O(g)
H2O(g) 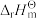 =- 241.8 2 kJ ·mol-1 (2)
=- 241.8 2 kJ ·mol-1 (2)要使反应温度维持在700°C,计算进料中甲醇与空气的摩尔数之比。已知空气中氧气的体积分数为0.20。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题
(1)已知:C(石墨,s)+O2(g)=CO2(g) △H1=-akJ•mol-1
H2(g)+ O2(g)=H2O(l) △H2=-bkJ•mol-1
O2(g)=H2O(l) △H2=-bkJ•mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H3=-ckJ•mol-1
计算C(石墨,s)与H2(g)反应生成1molCH4(g)的△H为_____ kJ•mol-1(用含a、b、c的式子表示)。
(2)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2molN2理论上放出的热量为_____ 。
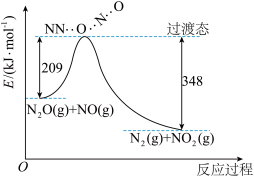
(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g) △H>0。在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
COS(g)+H2O(g) △H>0。在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
①H2S的平衡转化率α=_____ %,反应平衡常数K=______ 。
②在650K重复实验,此时反应的平衡常数K=0.25,经过8min时,测得水蒸气的物质的量为0.04mol,该反应是否达到平衡______ (填“是”或“否”),此时v(正)______ v(逆)(填“>”、“<”或“=”)。
(1)已知:C(石墨,s)+O2(g)=CO2(g) △H1=-akJ•mol-1
H2(g)+
 O2(g)=H2O(l) △H2=-bkJ•mol-1
O2(g)=H2O(l) △H2=-bkJ•mol-1CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H3=-ckJ•mol-1
计算C(石墨,s)与H2(g)反应生成1molCH4(g)的△H为
(2)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2molN2理论上放出的热量为

(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)
 COS(g)+H2O(g) △H>0。在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
COS(g)+H2O(g) △H>0。在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。①H2S的平衡转化率α=
②在650K重复实验,此时反应的平衡常数K=0.25,经过8min时,测得水蒸气的物质的量为0.04mol,该反应是否达到平衡
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】工业上常利用合理的催化剂,将含碳氧化物转化为重要的化工原料一甲醇,由CO、CO2和H2合成甲醇发生的主要反应如下:
I.CO(g)+2H2(g)⇌CH3OH(g) ΔH1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-58kJ/mol
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=41kJ/mol
回答下列问题:
已知反应I中相关的化学键键能数据如下表:
则x=_______ 。
I.CO(g)+2H2(g)⇌CH3OH(g) ΔH1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-58kJ/mol
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=41kJ/mol
回答下列问题:
已知反应I中相关的化学键键能数据如下表:
| 化学键 | H—H | C—O | C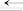 O O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | x |
则x=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。

(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示请写出该反应的热化学方程式____ 。
(2)实验测得,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧的热化学方程式:_______ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为_________ 。
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+ O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1

(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示请写出该反应的热化学方程式
(2)实验测得,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧的热化学方程式:
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+
 O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)S8分子可形成单斜硫和斜方硫,转化过程如下:S(s,单斜) S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是______ (填“S(单斜)”或“S(斜方)”)。
(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为____ kJ·mol-1。
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:____________________________ 。
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为____ kJ·mol-1 (用含a,b,c的式子表示)。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为__________ 。

 S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是
S(s,斜方) ΔH=-0.398 kJ·mol-1,则S(单斜)、S(斜方)相比,较稳定的是(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
| 化学键 | H—H | H—Cl |
| 键能 | 436 | 431 |
热化学方程式:H2(g) + Cl2(g) = 2HCl(g) ΔH=-183 kJ·mol-1,则Cl2的键能为
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(4)已知:C(石墨,s)+ O2(g) = CO2(g) ΔH1=-a kJ·mol-1
H2(g) + 1/2O2(g) = H2O(l) ΔH2=-b kJ·mol-1
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH3=-c kJ·mol-1
计算C(石墨,s)与H2(g)反应生成1 mol CH4(g)的ΔH为
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。则反应过程中,每生成2 mol N2理论上放出的热量为

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:_______ ;
(2)若已知下列数据:
试根据表中及图中数据计算N-H的键能_______ kJ• mol-1
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1_______ , 
_______ (填“增大”、“减小、” “不变”)。
(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如
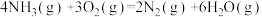



若1mol NH3还原NO至N2,则该反应过程中的反应热
_______ kJ/mol (用含a、b的式子表示)
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ • mol-1 | 435 | 943 |
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1

(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如
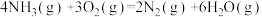



若1mol NH3还原NO至N2,则该反应过程中的反应热

您最近一年使用:0次
【推荐3】(1)已知单质硫16 g燃烧放热为149 kJ,写出硫燃烧热的热化学方程式:_________________
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:_____________ 。
(3)已知:N2、O2分子中化学键的键能分别是946 kJ/mol、497 kJ/mol。 N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol,NO分子中化学键的键能为_____ kJ/mol。
(4)S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)=SO2(g) ΔH1=-297.16 kJ/mol;
②S(正交,s)+O2(g)=SO2(g) ΔH2=-296.83 kJ/mol;
③S(单斜,s)=S(正交,s) ΔH3=_____ 。
S(单斜,s)比S(正交,s)更_________ (填“稳定”或“不稳定”)
(5)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1 、ΔH2,则ΔH1___________ ΔH2。(用“>”、“<”或“=”填空)
(6)相同条件下,2 mol氢原子所具有的能量________ 1 mol 氢分子所具有的能量。(用“>”、“<”或“=”填空)
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:
(3)已知:N2、O2分子中化学键的键能分别是946 kJ/mol、497 kJ/mol。 N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol,NO分子中化学键的键能为
(4)S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)=SO2(g) ΔH1=-297.16 kJ/mol;
②S(正交,s)+O2(g)=SO2(g) ΔH2=-296.83 kJ/mol;
③S(单斜,s)=S(正交,s) ΔH3=
S(单斜,s)比S(正交,s)更
(5)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1 、ΔH2,则ΔH1
(6)相同条件下,2 mol氢原子所具有的能量
您最近一年使用:0次



