(1)已知单质硫16 g燃烧放热为149 kJ,写出硫燃烧热的热化学方程式:_________________
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:_____________ 。
(3)已知:N2、O2分子中化学键的键能分别是946 kJ/mol、497 kJ/mol。 N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol,NO分子中化学键的键能为_____ kJ/mol。
(4)S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)=SO2(g) ΔH1=-297.16 kJ/mol;
②S(正交,s)+O2(g)=SO2(g) ΔH2=-296.83 kJ/mol;
③S(单斜,s)=S(正交,s) ΔH3=_____ 。
S(单斜,s)比S(正交,s)更_________ (填“稳定”或“不稳定”)
(5)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1 、ΔH2,则ΔH1___________ ΔH2。(用“>”、“<”或“=”填空)
(6)相同条件下,2 mol氢原子所具有的能量________ 1 mol 氢分子所具有的能量。(用“>”、“<”或“=”填空)
(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:
(3)已知:N2、O2分子中化学键的键能分别是946 kJ/mol、497 kJ/mol。 N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol,NO分子中化学键的键能为
(4)S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)=SO2(g) ΔH1=-297.16 kJ/mol;
②S(正交,s)+O2(g)=SO2(g) ΔH2=-296.83 kJ/mol;
③S(单斜,s)=S(正交,s) ΔH3=
S(单斜,s)比S(正交,s)更
(5)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1 、ΔH2,则ΔH1
(6)相同条件下,2 mol氢原子所具有的能量
更新时间:2020-04-13 22:16:17
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】人类过多地使用化石燃料,造成了二氧化碳的大量排放,致使地球气温上升。二氧化碳是温室气体,也是一种重要的资源,如以CO2为基本原料可合成甲醇,已知下列热化学方程式:
①2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ∆H1=−122.6kJ·mol−1
②CH3OCH3(g)+H2O(g)=2CH3OH(g) ∆H2=+23.4kJ·mol−1
则用CO2(g)与H2(g)反应合成CH3OH(g)的热化学方程式③_______
①2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ∆H1=−122.6kJ·mol−1
②CH3OCH3(g)+H2O(g)=2CH3OH(g) ∆H2=+23.4kJ·mol−1
则用CO2(g)与H2(g)反应合成CH3OH(g)的热化学方程式③
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。

(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示请写出该反应的热化学方程式____ 。
(2)实验测得,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧的热化学方程式:_______ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为_________ 。
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+ O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1

(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示请写出该反应的热化学方程式
(2)实验测得,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧的热化学方程式:
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。试依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g)===CH3COOH(l)的焓变为
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+
 O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.8 kJ·mol-1
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH1=-112.3 kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) ΔH2=-234 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=179.5 kJ·mol-1
请写出CO和NO2生成N2、CO2的热化学方程式_________________________ 。
(2)亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g) 2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):
2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):
则2NO(g)+C12(g) 2C1NO(g)反应的ΔH和a的关系为ΔH=
2C1NO(g)反应的ΔH和a的关系为ΔH=________ kJ·mol-1。
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH1=-112.3 kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) ΔH2=-234 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=179.5 kJ·mol-1
请写出CO和NO2生成N2、CO2的热化学方程式
(2)亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g)
 2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):
2C1NO(g),已知几种化学键的键能数据如下表(NO的结构为N≡O,亚硝酸氯的结构为Cl-N=O):| 化学键 | N≡O | Cl- Cl | Cl-N | N=O |
| 键能/kJ·mol-1 | 630 | 243 | a | 607 |
则2NO(g)+C12(g)
 2C1NO(g)反应的ΔH和a的关系为ΔH=
2C1NO(g)反应的ΔH和a的关系为ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】CH4—CO2催化重整反应为CH4(g)+CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol-1
C(s)+ O2(g)=CO(g) ΔH=-111 kJ·mol-1
O2(g)=CO(g) ΔH=-111 kJ·mol-1
该催化重整反应的ΔH=____ kJ·mol-1。
已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol-1
C(s)+
 O2(g)=CO(g) ΔH=-111 kJ·mol-1
O2(g)=CO(g) ΔH=-111 kJ·mol-1该催化重整反应的ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)工业上利用天然气(主要成分为 )与
)与 进行高温重整制备CO的化学方程式为
进行高温重整制备CO的化学方程式为 ,已知
,已知 、
、 和CO的燃烧热分别为
和CO的燃烧热分别为 、
、 和
和 ,则生成
,则生成 (标准状况)CO所需的热量为
(标准状况)CO所需的热量为__________ 。
(2)已知将 氧化为
氧化为 的
的 ,单质硫的燃烧热为
,单质硫的燃烧热为 ,计算由
,计算由 生成
生成 的
的
_________ (需写出计算过程)。
 )与
)与 进行高温重整制备CO的化学方程式为
进行高温重整制备CO的化学方程式为 ,已知
,已知 、
、 和CO的燃烧热分别为
和CO的燃烧热分别为 、
、 和
和 ,则生成
,则生成 (标准状况)CO所需的热量为
(标准状况)CO所需的热量为(2)已知将
 氧化为
氧化为 的
的 ,单质硫的燃烧热为
,单质硫的燃烧热为 ,计算由
,计算由 生成
生成 的
的
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得:5g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5 kJ的热量。试写出甲醇燃烧的热化学方程式:________________________________________________________ 。
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,破坏旧化学键需要吸收能量,形成新化学键又会释放能量。
已知反应N2+3H2===2NH3 ΔH=a kJ·mol-1。试根据表中数据计算a的数值为________ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式:
____________________________________________________________________________ 。
(1)实验测得:5g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出113.5 kJ的热量。试写出甲醇燃烧的热化学方程式:
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,破坏旧化学键需要吸收能量,形成新化学键又会释放能量。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应N2+3H2===2NH3 ΔH=a kJ·mol-1。试根据表中数据计算a的数值为
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。下表列出了一些化学键的键能E:
请回答下列问题:
(1)反应 H2(g) + O2(g)= H2O(g) △H=-242kJ∙mol-1,x=
O2(g)= H2O(g) △H=-242kJ∙mol-1,x=_______ 。
(2)历史上曾用“地康法”制Cl2,这一方法是用CuCl2做催化剂,在450°条件下,用空气中的氧气跟氯化氢反应制氯气,若反应生成液态水,请写出该反应的热化学方程式为_______ 。
(3)若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1mol电子转移时,反应的能量变化为_______ 。
(4)关于2SO2(g)+O2(g) 2SO3(g),已知1mol SO2 (g)被氧化为1mol SO3(g)的△H=-akJ∙mol-1(a>0)。回答下列问题:
2SO3(g),已知1mol SO2 (g)被氧化为1mol SO3(g)的△H=-akJ∙mol-1(a>0)。回答下列问题:
在一定温度下,将2mol SO2和1mol O2放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量_______ (填“等于”、“大于”或“小于”)2akJ。
(5)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:①_______ ;②2V2O4+O2=2V2O5
| 化学键 | H-H | Cl-Cl | O=O | C-Cl | C-H | O-H | H-Cl |
| E/( kJ∙mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)反应 H2(g) +
 O2(g)= H2O(g) △H=-242kJ∙mol-1,x=
O2(g)= H2O(g) △H=-242kJ∙mol-1,x=(2)历史上曾用“地康法”制Cl2,这一方法是用CuCl2做催化剂,在450°条件下,用空气中的氧气跟氯化氢反应制氯气,若反应生成液态水,请写出该反应的热化学方程式为
(3)若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1mol电子转移时,反应的能量变化为
(4)关于2SO2(g)+O2(g)
 2SO3(g),已知1mol SO2 (g)被氧化为1mol SO3(g)的△H=-akJ∙mol-1(a>0)。回答下列问题:
2SO3(g),已知1mol SO2 (g)被氧化为1mol SO3(g)的△H=-akJ∙mol-1(a>0)。回答下列问题:在一定温度下,将2mol SO2和1mol O2放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量
(5)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:①
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)5.7g汽油(主要成分为C8H18,相对分子质量为114)完全燃烧生成液态水和CO2,放出275.9kJ的热量,则汽油的燃烧热为___________ ;
(2)已知:2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
H2O(l)= H2O(g) △H=+44kJ/mol
①写出H2与O2反应生成液态水时的热化学方程式____________ ;
②在通常情况下,若要得到857.4kJ的热量,需H2的质量为________ ,这些H2在标况下的体积为______ 。
(2)已知:2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
H2O(l)= H2O(g) △H=+44kJ/mol
①写出H2与O2反应生成液态水时的热化学方程式
②在通常情况下,若要得到857.4kJ的热量,需H2的质量为
您最近一年使用:0次
【推荐3】(1)0.5 mol气态高能燃料乙硼烷 在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为
在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为_________ 。已知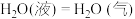
 ,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量
,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量____________
(2)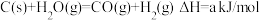 ,
,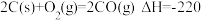
 ,又已知
,又已知 、
、 和
和 键的键能分别为
键的键能分别为 、
、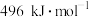 和
和 ,则a为
,则a为__________ 。
(3)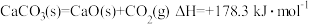 ,
, ,该反应能够自发进行,则温度所满足的条件是
,该反应能够自发进行,则温度所满足的条件是______________ 。
(4)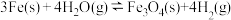 平衡常数的表达式为
平衡常数的表达式为____________ 。反应 的平衡常数为49,则该温度下反应
的平衡常数为49,则该温度下反应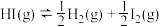 的平衡常数为
的平衡常数为____________ 。
 在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为
在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为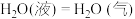
 ,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量
,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量(2)
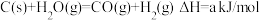 ,
,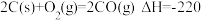
 ,又已知
,又已知 、
、 和
和 键的键能分别为
键的键能分别为 、
、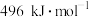 和
和 ,则a为
,则a为(3)
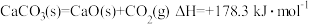 ,
, ,该反应能够自发进行,则温度所满足的条件是
,该反应能够自发进行,则温度所满足的条件是(4)
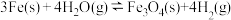 平衡常数的表达式为
平衡常数的表达式为 的平衡常数为49,则该温度下反应
的平衡常数为49,则该温度下反应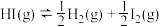 的平衡常数为
的平衡常数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】依据事实,写出下列反应的热化学方程式。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为_____________________________ 。
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为____________________________ 。
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为___________________ 。相同状况下,能量较低的是_____________ 。
(4)③C(s)+ O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____ 。写出CO燃烧的热化学方程式__________ 。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为
(4)③C(s)+
 O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)已知H-H键键能(断裂时吸收或生成时释放的能量)为436 kJ·mol-1,H-N键键能为391 kJ·mol-1,根据热化学方程式:N2(g) +3H2(g) =2NH3(g) ΔH=-92.4 kJ·mol-1。则N≡N键的键能是_________ 。
(2)已知下列热化学方程式:
①Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H=﹣25 kJ·mol-1
②3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) △H=﹣47 kJ·mol-1
③Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) △H=﹢19 kJ·mol-1
写出FeO(s)被CO还原成Fe和CO2的热化学方程式______________ 。
(3)氯化铁水解的离子方程式为__________ ,配制氯化铁溶液时滴加少量盐酸的作用是_____ 。
(2)已知下列热化学方程式:
①Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H=﹣25 kJ·mol-1
②3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) △H=﹣47 kJ·mol-1
③Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) △H=﹢19 kJ·mol-1
写出FeO(s)被CO还原成Fe和CO2的热化学方程式
(3)氯化铁水解的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水放出133.5 kJ热量。写出该反应的热化学方程式______
(2)已知H—H的键能为436kJ·mol–1 ,Cl—Cl的键能为243kJ·mol–1,H—Cl的键能为431kJ·mol–1,写出氢气在氯气中燃烧生成1 mol氯化氢的热化学方程式_________
(3)神舟系列载人飞船的火箭推进剂中盛有液态肼(N2H4)和强氧化剂NO2,这两者混合反应生成大量的N2和水蒸气,并放出大量的热。又知:
① N2(g) + O2(g) = 2NO(g) ΔH= +180 kJ·mol-1
②2NO(g) + O2(g) = 2NO2(g) ΔH= –112.3 kJ·mol-1
③N2H4(l) + O2(g) = N2(g) + 2H2O(g) △H = –534 kJ·mol-1
试写出液态肼与NO2反应的热化学方程式 :_________ 。
(2)已知H—H的键能为436kJ·mol–1 ,Cl—Cl的键能为243kJ·mol–1,H—Cl的键能为431kJ·mol–1,写出氢气在氯气中燃烧生成1 mol氯化氢的热化学方程式
(3)神舟系列载人飞船的火箭推进剂中盛有液态肼(N2H4)和强氧化剂NO2,这两者混合反应生成大量的N2和水蒸气,并放出大量的热。又知:
① N2(g) + O2(g) = 2NO(g) ΔH= +180 kJ·mol-1
②2NO(g) + O2(g) = 2NO2(g) ΔH= –112.3 kJ·mol-1
③N2H4(l) + O2(g) = N2(g) + 2H2O(g) △H = –534 kJ·mol-1
试写出液态肼与NO2反应的热化学方程式 :
您最近一年使用:0次



