将10.6gNa2CO3粉末投入500mL一定浓度的硫酸溶液中,恰好完全反应。求:
(1)标准状况下收集到CO2气体体积为___________ 。
(2)硫酸溶液的物质的量浓度为___________ 。
(1)标准状况下收集到CO2气体体积为
(2)硫酸溶液的物质的量浓度为
更新时间:2024-03-15 16:39:01
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】根据所学知识填写下列空白。
(1)在标准状况下,67.2 L CO2是_______ mol,质量为_______ g,含有_______ 个CO2分子,其中含有_______ mol氧原子。
(2)在标准状况下,1.7 g氨气所占的体积约为_______ L,它与同条件下_______ mol H2S含有相同的氢原子数。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(4)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1.则c(Na+)为_______ 。
(1)在标准状况下,67.2 L CO2是
(2)在标准状况下,1.7 g氨气所占的体积约为
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为
(4)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1.则c(Na+)为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】标准状况下,33.6LNO和NO2混合气体质量为53g,求混合气体中NO和NO2的体积比和质量比_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】8.7g二氧化锰粉末与足量浓盐酸共热,可以生成标况下的氯气的体积为__ L,参与反应的盐酸中被氧化的物质的量为___ mol。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室中所用少量氯气是用MnO2和浓盐酸制取的,用浓盐酸200ml,其密度为1.19g·cm-3,HCl的质量分数为36.5%,跟MnO2恰好完全反应,产生了11.2L(标况)的氯气。试计算:
①浓盐酸的物质的量浓度?___
②求参加反应的HCl的物质的量?___
③被氧化的HCl的质量?___
①浓盐酸的物质的量浓度?
②求参加反应的HCl的物质的量?
③被氧化的HCl的质量?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】按要求完成。
(1)19.6克硫酸是___________ molH2SO4,含有___________ 个原子,1.7克NH3在同温同压下与___________ 克H2S气体含有的氢原子数相同。
(2)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数___________ ,混合气体的平均摩尔质量为___________ 该气体对氢气的相对密度为___________ 。
(3)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是___________ (其中阿伏加德罗常数用NA表示)。
(4)将MgCl2·xH2O的晶体4.06g溶于水配成100mL溶液,取出50mL溶液正好与0.02moL的AgNO3溶液完全作用,4.06g的MgCl2·xH2O物质的量为___________ 式中x的数值___________ 。
(5)配制100mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为___________ mL。
(6)现要配制1mol·L-1Na2CO3溶液250mL
①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)___________ g;
②在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有___________
A.固体Na2CO3·10H2O放在右盘(1g以下用游码);
B.容量瓶用碳酸钠溶液先润洗;
C.转移溶液时未洗涤烧杯
D.定容时溶液未冷却;
E.定容时视线仰视;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G.容量瓶未干燥。
(1)19.6克硫酸是
(2)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数
(3)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是
(4)将MgCl2·xH2O的晶体4.06g溶于水配成100mL溶液,取出50mL溶液正好与0.02moL的AgNO3溶液完全作用,4.06g的MgCl2·xH2O物质的量为
(5)配制100mL1mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为
(6)现要配制1mol·L-1Na2CO3溶液250mL
①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)
②在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有
A.固体Na2CO3·10H2O放在右盘(1g以下用游码);
B.容量瓶用碳酸钠溶液先润洗;
C.转移溶液时未洗涤烧杯
D.定容时溶液未冷却;
E.定容时视线仰视;
F.摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G.容量瓶未干燥。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)相同质量的氢气、甲烷(CH4)、水,其中含分子数最多的是________ ;等物质的量的三种物质含氢原子最多的是________ 。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92 g该氧化物的体积为448 mL,则该氧化物的物质的量为______ ,该氧化物的摩尔质量为______ 。
(3)某化学兴趣小组对某品牌矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,Mg2+的物质的量浓度为______ 。
(4)现有0.1 mol·L-1 Na2SO4和0.3 mol·L-1 H2SO4的混合溶液100 mL,向其中逐滴加入0.2 mol·L-1的Ba(OH)2溶液,并不断搅拌,使反应充分进行。(忽略混合过程中的体积变化)
①当加入50 mL Ba(OH)2溶液时,所得溶液中SO42-离子的物质的量浓度为________ mol·L-1。
②当溶液中沉淀量达到最大时,所加Ba(OH)2溶液的体积为________ mL。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92 g该氧化物的体积为448 mL,则该氧化物的物质的量为
(3)某化学兴趣小组对某品牌矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,Mg2+的物质的量浓度为
(4)现有0.1 mol·L-1 Na2SO4和0.3 mol·L-1 H2SO4的混合溶液100 mL,向其中逐滴加入0.2 mol·L-1的Ba(OH)2溶液,并不断搅拌,使反应充分进行。(忽略混合过程中的体积变化)
①当加入50 mL Ba(OH)2溶液时,所得溶液中SO42-离子的物质的量浓度为
②当溶液中沉淀量达到最大时,所加Ba(OH)2溶液的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)相同质量的CO和CO2,它们所含的原子数之比为___________ ,标准状况下,含有相同氧原子数的CO和CO2的体积之比为_____________ 。
(2)若a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是___________ (设NA为阿伏加 德罗常数的值)。
(3)标准状况下有①0.112 L水 ②0.5NA个HCl分子 ③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol Ne 所含原子个数从大到小的顺序为___________ 。
(4)V mL Fe2(SO4)3溶液中,含有Fe 3+ m g,取出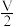 mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为
mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为___________________ 。(用含有m、V的式子表示)
(1)相同质量的CO和CO2,它们所含的原子数之比为
(2)若a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是
(3)标准状况下有①0.112 L水 ②0.5NA个HCl分子 ③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol Ne 所含原子个数从大到小的顺序为
(4)V mL Fe2(SO4)3溶液中,含有Fe 3+ m g,取出
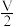 mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为
mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为
您最近一年使用:0次



