解题方法
1 . 将某质量的镁铝合金溶解在500 mL盐酸中,向反应后的溶液中逐滴加入2 mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示。请填写下列空白:
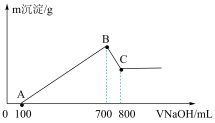
(1)写出BC段发生反应的化学方程式:_______ 。
(2)合金中铝的质量为_______ 。
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是_______ 。

(1)写出BC段发生反应的化学方程式:
(2)合金中铝的质量为
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是
您最近一年使用:0次
2 . 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
您最近一年使用:0次
3 . 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。
(1)为研究A的组成与结构,进行如下实验:
(2)综上所述,A的结构简式为___________ 。
(3)两分子A可反应生成一个六元环状化合物,写出该反应的化学方程式___________ 。
(1)为研究A的组成与结构,进行如下实验:
| 实验步骤: | 实验结论 |
| ①称取9.0 g A,升温使其汽化,测其密度是相同条件下H2的45倍 | A的相对分子质量为 |
| ②将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | A的分子式为 |
| ③另取9.0 g A,与足量的NaHCO3粉末反应,生成2.24 LCO2(标准状况);若与足量金属钠反应则生成2.24 LH2 (标准状况) | 用结构简式表示A中含有的官能团 |
④A的核磁共振氢谱如图: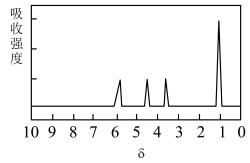 | A中含有 |
(3)两分子A可反应生成一个六元环状化合物,写出该反应的化学方程式
您最近一年使用:0次
2023-07-31更新
|
129次组卷
|
2卷引用:陕西省延安市宜川中学2020-2021学年高二上学期期末考试化学试题
解题方法
4 . 在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
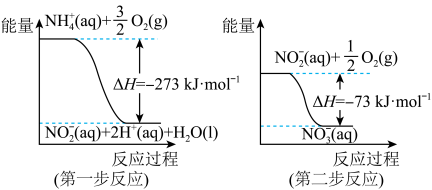
(1)第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
(2)1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为___________ 。
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=___________ (用ΔH1、ΔH3、ΔH4表示) 。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
(1)第一步反应是
(2)1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3)在0℃、101kPa时,44.8LH2在足量O2中完全燃烧生成H2O(l)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g) +H2(g)ΔH2
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3
2H2(g)+O2(g)=2H2O(g)ΔH4
则ΔH2=
您最近一年使用:0次
解题方法
5 . 回答下列问题
(1)常温下,0.05mol/L硫酸溶液中,
___________ mol/L,pH值为___________ ,水电离的
___________ mol/L;25℃ 的盐酸中,由水电离产生的
的盐酸中,由水电离产生的 的物质的量浓度为
的物质的量浓度为___________ 。
(2)氨水和稀盐酸反应后的溶液呈中性,所得溶液中的离子浓度大小关系是___________ 。
(3)某温度(t℃)时,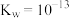 ,则该温度(填大于、等于或小于)
,则该温度(填大于、等于或小于)___________ 25℃,理由是___________ 。将此温度下pH=11的NaOH溶液a L与pH=l的 溶液b L混合,若所得混合溶液为中性,则a:b=
溶液b L混合,若所得混合溶液为中性,则a:b=___________ ;
(4)已知 的
的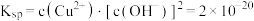 。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某
。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某 溶液里
溶液里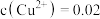 mol/L,如要生成
mol/L,如要生成 沉淀,应调整溶液的pH大于
沉淀,应调整溶液的pH大于___________ 。
②要使0.2
 溶液中
溶液中 沉淀较为完全(使
沉淀较为完全(使 浓度降至原来的千分之一),则应向溶液里加入
浓度降至原来的千分之一),则应向溶液里加入 溶液,使溶液的pH为
溶液,使溶液的pH为___________ 。
(1)常温下,0.05mol/L硫酸溶液中,


 的盐酸中,由水电离产生的
的盐酸中,由水电离产生的 的物质的量浓度为
的物质的量浓度为(2)氨水和稀盐酸反应后的溶液呈中性,所得溶液中的离子浓度大小关系是
(3)某温度(t℃)时,
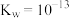 ,则该温度(填大于、等于或小于)
,则该温度(填大于、等于或小于) 溶液b L混合,若所得混合溶液为中性,则a:b=
溶液b L混合,若所得混合溶液为中性,则a:b=(4)已知
 的
的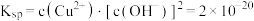 。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某
。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某 溶液里
溶液里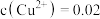 mol/L,如要生成
mol/L,如要生成 沉淀,应调整溶液的pH大于
沉淀,应调整溶液的pH大于②要使0.2

 溶液中
溶液中 沉淀较为完全(使
沉淀较为完全(使 浓度降至原来的千分之一),则应向溶液里加入
浓度降至原来的千分之一),则应向溶液里加入 溶液,使溶液的pH为
溶液,使溶液的pH为
您最近一年使用:0次
名校
解题方法
6 . 完成下列问题
(1)在 25℃、101 kPa 下,已知 SiH4气体在氧气中完全燃烧后恢复至原状态,平均每转移1 mol 电子放出热量 a kJ,该反应的热化学方程式为___________ 。
(2)燃料的热值是指单位质量某种燃料完全燃烧放出的热量,已知25℃、101kPa下C8H18(辛烷)的热值为b kJ/g,表示辛烷燃烧热的热化学方程式为___________ 。
(3)已知:H2O(l)= H2O(g) ΔH= +44.0kJ·mol-1,甲烷完全燃烧与不完全燃烧的热效应如下图所示。

①写出表示甲烷燃烧热的热化学方程式:___________ 。
②CO的燃烧热ΔH=___________ kJ·mol-1
③已知氢气的燃烧热为-286kJ·mol-1,氧气中O=O键的键能为496kJ·mol-1,水蒸气中H-O键的键能为463kJ·mol-1,则氢气中H-H键的键能为___________ kJ·mol-1。
(1)在 25℃、101 kPa 下,已知 SiH4气体在氧气中完全燃烧后恢复至原状态,平均每转移1 mol 电子放出热量 a kJ,该反应的热化学方程式为
(2)燃料的热值是指单位质量某种燃料完全燃烧放出的热量,已知25℃、101kPa下C8H18(辛烷)的热值为b kJ/g,表示辛烷燃烧热的热化学方程式为
(3)已知:H2O(l)= H2O(g) ΔH= +44.0kJ·mol-1,甲烷完全燃烧与不完全燃烧的热效应如下图所示。

①写出表示甲烷燃烧热的热化学方程式:
②CO的燃烧热ΔH=
③已知氢气的燃烧热为-286kJ·mol-1,氧气中O=O键的键能为496kJ·mol-1,水蒸气中H-O键的键能为463kJ·mol-1,则氢气中H-H键的键能为
您最近一年使用:0次
名校
解题方法
7 . 6.5g锌投入足量的稀硫酸溶液,充分反应,测得溶液体积为200mL。计算:
(1)标准状况下生成H2的体积___________ 。
(2)所得ZnSO4溶液溶质物质的量浓度___________ 。
(1)标准状况下生成H2的体积
(2)所得ZnSO4溶液溶质物质的量浓度
您最近一年使用:0次
2023-05-04更新
|
169次组卷
|
2卷引用:陕西省西安市长安区第一中学2022-2023学年高二上学期期末考试化学试题(文科)
名校
8 . Ⅰ.按要求填空:
(1)_______  中含有的氧原子数与
中含有的氧原子数与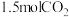 中含有的氧原子数相等。
中含有的氧原子数相等。
(2)将等物质的量的 和
和 混合,混合气体中
混合,混合气体中 与
与 的质量比为
的质量比为_______ ;要使 与
与 含相同数目的H原子,则
含相同数目的H原子,则 和
和 的物质的量之比为
的物质的量之比为_______ 。
(3)瓦斯中甲烷与氧气的质量比为1∶4时极易发生爆炸,此时甲烷与氧气的体积比为_________ 。
Ⅱ.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6LH2(标准状况)。试计算(写过程):
(4)该合金中铝的质量分数_________ ;
(5)该合金中镁铝的物质的量之比________ 。
(1)
 中含有的氧原子数与
中含有的氧原子数与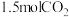 中含有的氧原子数相等。
中含有的氧原子数相等。(2)将等物质的量的
 和
和 混合,混合气体中
混合,混合气体中 与
与 的质量比为
的质量比为 与
与 含相同数目的H原子,则
含相同数目的H原子,则 和
和 的物质的量之比为
的物质的量之比为(3)瓦斯中甲烷与氧气的质量比为1∶4时极易发生爆炸,此时甲烷与氧气的体积比为
Ⅱ.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6LH2(标准状况)。试计算(写过程):
(4)该合金中铝的质量分数
(5)该合金中镁铝的物质的量之比
您最近一年使用:0次
名校
解题方法
9 . 某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90,取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。
(1)试求该有机物的分子式_____ 。
(2)若该有机物呈现酸性,且该有机物的核磁共振氢谱图中出现4个吸收峰,面积比为3:1:1:1,写出其结构简式_____ 。
(1)试求该有机物的分子式
(2)若该有机物呈现酸性,且该有机物的核磁共振氢谱图中出现4个吸收峰,面积比为3:1:1:1,写出其结构简式
您最近一年使用:0次
名校
解题方法
10 . 在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片上只发生电化学腐蚀,当在铜片上共放出3.36 L(标准状况)的气体时,H2SO4恰好用完,求:
(1)参加反应锌片的质量___________ ?
(2)原H2SO4溶液的浓度___________ ?
(3)整个过程中外电路通过的电子的物质的量___________ ?
(1)参加反应锌片的质量
(2)原H2SO4溶液的浓度
(3)整个过程中外电路通过的电子的物质的量
您最近一年使用:0次



