6.5g锌投入足量的稀硫酸溶液,充分反应,测得溶液体积为200mL。计算:
(1)标准状况下生成H2的体积___________ 。
(2)所得ZnSO4溶液溶质物质的量浓度___________ 。
(1)标准状况下生成H2的体积
(2)所得ZnSO4溶液溶质物质的量浓度
更新时间:2023-05-04 21:58:55
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室用17.4g的MnO2与100mL足量的浓盐酸制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)求生成氯气的体积(标准状况)______ 。
(2)求参加反应的HCl的物质的量_____ 。
(3)假设反应后溶液的体积不变(仍为100mL),求生成的MnCl2的物质的量浓度_____ 。
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)求生成氯气的体积(标准状况)
(2)求参加反应的HCl的物质的量
(3)假设反应后溶液的体积不变(仍为100mL),求生成的MnCl2的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】实验室需要制备22.4L(标准状况)H2,现用质量分数为90.0%的锌粒与足量的稀盐酸反应(假设杂质不与稀盐酸反应),问:(要求写出计算过程)
(1)至少需要质量分数为90.0%的锌粒多少克?____
(2)生成的氯化锌的物质的量是多少?______
(1)至少需要质量分数为90.0%的锌粒多少克?
(2)生成的氯化锌的物质的量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】把铝、铁混合物1.1 g溶于200 mL 5mol/L盐酸中,反应后盐酸的浓度变为4.6mol/L(溶液体积变化忽略不计).求
(1)反应中消耗HCl的物质的量:__________ mol,混合物中铝的质量是:________ g,现有某工业反应混合液,其可能含有的组分为乙醚(C2H5OC2H5)、乙醇(C2H5OH)和水。经分析知,液体中各元素的原子个数之比为C∶H∶O=16∶42∶5。
(2)若该混合液中只含两种组分,则所有可能的组合是___ 。
(3)若该混合液中含有三种组分,且知在628g该混合液中含有1molH2O,则此时乙醇和乙醚的物质的量各是多少?_______ (写出解题过程)
(4)将含氧气和甲烷的混合气体充入放有23.4 g 的密闭容器里,用电火花间断地点燃,反应结束后,容器内于150℃时压强为0 Pa,将残留物溶于水无气体生成.求甲烷和氧气在标况下体积各为多少
的密闭容器里,用电火花间断地点燃,反应结束后,容器内于150℃时压强为0 Pa,将残留物溶于水无气体生成.求甲烷和氧气在标况下体积各为多少_______ ?(写出解题过程)
(1)反应中消耗HCl的物质的量:
(2)若该混合液中只含两种组分,则所有可能的组合是
(3)若该混合液中含有三种组分,且知在628g该混合液中含有1molH2O,则此时乙醇和乙醚的物质的量各是多少?
(4)将含氧气和甲烷的混合气体充入放有23.4 g
 的密闭容器里,用电火花间断地点燃,反应结束后,容器内于150℃时压强为0 Pa,将残留物溶于水无气体生成.求甲烷和氧气在标况下体积各为多少
的密闭容器里,用电火花间断地点燃,反应结束后,容器内于150℃时压强为0 Pa,将残留物溶于水无气体生成.求甲烷和氧气在标况下体积各为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】向500mLNaOH溶液中投入10.8g的铝,二者恰好完全反应,试计算:
(1)求铝的物质的量___ ;
(2)参加反应的氢氧化钠的物质的量___ 和物质的量浓度___ 。
(1)求铝的物质的量
(2)参加反应的氢氧化钠的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在 300 mL 2 mol/L H2SO4溶液中,SO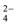 的物质的量浓度是
的物质的量浓度是_____ ?其中含有_____ 个 SO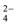 ?溶质的质量是
?溶质的质量是__________ ?
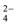 的物质的量浓度是
的物质的量浓度是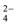 ?溶质的质量是
?溶质的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________ 。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________ 。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________ 。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________ 。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___ w4;若ρ1<ρ2,w3______ w4(填“>”“<”或“=”)。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度
(2)该溶液的质量分数
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
| 溶质的质量分数 | 溶液的密度(g·cm-3) | |
| 第一份溶液 | w1 | ρ1 |
| 第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3
您最近一年使用:0次



