解题方法
1 . 铝是中学化学学习阶段的唯一一种既能与酸(非氧化性酸)反应又能与强碱溶液反应放出 的金属,就铝的这一特殊性质,回答下列问题:
的金属,就铝的这一特殊性质,回答下列问题:
(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 的体积之比是
的体积之比是___________ 。
(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸和氢氧化钠溶液中,产生 的体积之比是
的体积之比是___________ 。
(3)足量的两份铝分别投入到等体积、一定物质的量浓度的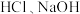 溶液中,二者产生的
溶液中,二者产生的 相等,则
相等,则 和
和 的物质的量浓度之比是
的物质的量浓度之比是___________ 。
(4)甲、乙两烧杯中各盛有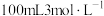 的盐酸和
的盐酸和 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为
溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为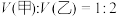 ,则加入铝粉的质量为___________(填字母)。
,则加入铝粉的质量为___________(填字母)。
 的金属,就铝的这一特殊性质,回答下列问题:
的金属,就铝的这一特殊性质,回答下列问题:(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 的体积之比是
的体积之比是(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸和氢氧化钠溶液中,产生
 的体积之比是
的体积之比是(3)足量的两份铝分别投入到等体积、一定物质的量浓度的
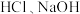 溶液中,二者产生的
溶液中,二者产生的 相等,则
相等,则 和
和 的物质的量浓度之比是
的物质的量浓度之比是(4)甲、乙两烧杯中各盛有
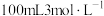 的盐酸和
的盐酸和 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为
溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为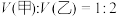 ,则加入铝粉的质量为___________(填字母)。
,则加入铝粉的质量为___________(填字母)。A.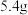 | B.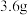 | C.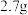 | D.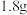 |
您最近一年使用:0次
2023-02-09更新
|
238次组卷
|
10卷引用:2016-2017学年吉林长春外国语学校高一上期末理化学卷
2016-2017学年吉林长春外国语学校高一上期末理化学卷(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】(已下线)专题3.2 铝及其重要化合物(讲)——2020年高考化学一轮复习讲练测(已下线)3.2.2 物质的量在化学方程式计算中的应用(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)(已下线)考点15 铝及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第08讲 金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省虎林市高级中学2022-2023学年高三上学期第一次月考化学试题黑龙江省齐齐哈尔市三立高级中学2022-2023学年高三上学期期中考试化学试题第三章 金属及其化合物 第15讲 金属材料 金属冶炼(已下线)考点15 铝及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
解题方法
2 . 把10.2g镁铝合金的粉末放入过量的盐酸中,得到11.2LH2(标准状况下)。试计算:
(1)该合金中镁的质量分数为_______ 。
(2)该合金中镁与铝的物质的量之比为_______ 。
(3)该合金溶于足量的烧碱溶液中,产生H2的体积(标准状况下)用是_______ ;
(1)该合金中镁的质量分数为
(2)该合金中镁与铝的物质的量之比为
(3)该合金溶于足量的烧碱溶液中,产生H2的体积(标准状况下)用是
您最近一年使用:0次
3 . (1)有相同物质的量的H2O和H2SO4,其质量之比为___________ 。
(2)由CO2与CO组成的混和气体对H2的相对密度为20,则混和气体中CO2的体积分数为___________ ;CO的质量分数为___________ 。
(3)同温同压下,12C18O和14N2两种气体的密度之比为___________ 。
(4)将乙烯、CO、N2三种气体分别盛放在三个相同的容器中,若三个容器的温度和质量相等,则三个容器的气体压强之比为___________ 。
(2)由CO2与CO组成的混和气体对H2的相对密度为20,则混和气体中CO2的体积分数为
(3)同温同压下,12C18O和14N2两种气体的密度之比为
(4)将乙烯、CO、N2三种气体分别盛放在三个相同的容器中,若三个容器的温度和质量相等,则三个容器的气体压强之比为
您最近一年使用:0次
名校
解题方法
4 . (1)反应3A(g)+B(g)=2C(g)在三种不同的条件下进行反应,一段时间后,测得的反应速率用不同的物质表示为:①vA=1mol/(L·min);②vC=0.5mol/(L·min);③vB=0.5mol/(L·min),则在三种不同条件下该反应速率由大到小的关系是___ (请用序号表示)。
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
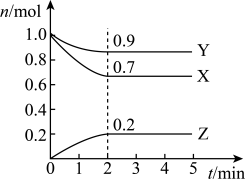
①该反应的化学方程式为___ 。
②反应开始至2min,以气体Z表示的平均反应速率为___ 。
③若2min后反应达平衡,与初始时刻相比,此时容器内混合气体的平均相对分子质量___ (填“增大”、“减小”或“不变”,下同),混合气体密度比起始时___ 。
④上述反应,在第2min时,X的转化率为___ 。
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
②反应开始至2min,以气体Z表示的平均反应速率为
③若2min后反应达平衡,与初始时刻相比,此时容器内混合气体的平均相对分子质量
④上述反应,在第2min时,X的转化率为
您最近一年使用:0次
2021-06-02更新
|
384次组卷
|
6卷引用:吉林省长春市农安县2019-2020学年高一下学期期末考试化学试题
5 . 过氧化钙晶体(CaO2·8H2O)可用于改善地表水质、处理含重金属粒子废水、应急供氧等。
(1)已知:I2+2 =2I-+
=2I-+ ,测定制备的过氧化钙晶体中CaO2的含量的实验步骤如下:
,测定制备的过氧化钙晶体中CaO2的含量的实验步骤如下:
第一步:准确称取a g产品放入锥形瓶中,再加入过量的b g KI晶体,加入适量蒸馏水溶解,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。第二步:向上述锥形瓶中加入几滴淀粉溶液。第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液发生反应,滴定达到终点时出现的现象是___________ 。若滴定消耗Na2S2O3溶液V mL,则样品中CaO2的质量分数为___________ (用字母表示)。
(2)已知过氧化钙加热至350 ℃左右开始分解放出氧气。将过氧化钙晶体(CaO2·8H2O)在坩埚中加热逐渐升高温度,测得样品质量随温度的变化如图所示,则350 ℃左右所得固体物质的化学式为___________ 。

(1)已知:I2+2
 =2I-+
=2I-+ ,测定制备的过氧化钙晶体中CaO2的含量的实验步骤如下:
,测定制备的过氧化钙晶体中CaO2的含量的实验步骤如下:第一步:准确称取a g产品放入锥形瓶中,再加入过量的b g KI晶体,加入适量蒸馏水溶解,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。第二步:向上述锥形瓶中加入几滴淀粉溶液。第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液发生反应,滴定达到终点时出现的现象是
(2)已知过氧化钙加热至350 ℃左右开始分解放出氧气。将过氧化钙晶体(CaO2·8H2O)在坩埚中加热逐渐升高温度,测得样品质量随温度的变化如图所示,则350 ℃左右所得固体物质的化学式为

您最近一年使用:0次
6 . 一定温度下,在10 L密闭容器中加入5 mol SO2和3 mol O2,发生反应:2SO2(g)+O2(g)⇌2SO3(g),10 min时,反应达到平衡状态,此时容器中还含有3 mol SO2。
(1)反应起始时, SO2的浓度为___ ,O2的浓度为___ ,反应生成了___ mol SO3,v(SO2)=___ 。
(2)平衡时SO3的浓度是__ ,SO2的转化率是___ 。
(3)平衡时容器内气体的总物质的量为__ mol。
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是______ (填序号)。
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3)∶n(O2)∶n(SO2)=2∶1∶2
(1)反应起始时, SO2的浓度为
(2)平衡时SO3的浓度是
(3)平衡时容器内气体的总物质的量为
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3)∶n(O2)∶n(SO2)=2∶1∶2
您最近一年使用:0次
解题方法
7 . 计算题
将足量铁粉投入到盛有1L 2 mol·L-1稀盐酸的烧杯中发生反应,计算在标准状况下生成氢气的体积是多少升?___________
将足量铁粉投入到盛有1L 2 mol·L-1稀盐酸的烧杯中发生反应,计算在标准状况下生成氢气的体积是多少升?
您最近一年使用:0次
解题方法
8 . 下列溶液,c(H+)由小到大的排列顺序是___ ;pH由小到大的排列顺序是___ 。
①0.1mol/LHCl溶液;②0.1mol/LH2SO4溶液;③0.1mol/LNaOH溶液;④0.1mol/LCH3COOH溶液
①0.1mol/LHCl溶液;②0.1mol/LH2SO4溶液;③0.1mol/LNaOH溶液;④0.1mol/LCH3COOH溶液
您最近一年使用:0次
2021-03-03更新
|
654次组卷
|
3卷引用:吉林长春市榆树高级中学2019-2020学年高二下学期期末考试化学试题
吉林长春市榆树高级中学2019-2020学年高二下学期期末考试化学试题人教2019版选择性必修一第三章 第二节 水的电离和溶液酸碱性 课后习题(已下线)3.1.2 pH的计算与测量-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
名校
解题方法
9 . 常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因:___________ (用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)___________ (填”>”、” <”或”=”)0.1mol/L NaOH溶液中由水电离出的c(H+)。
(3)求出混合液中下列算式的精确计算结果(填具体数字):
___________ mol/L。
(4)已知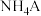 溶液为中性,又知HA溶液加到
溶液为中性,又知HA溶液加到 溶液中有气体放出,试推断
溶液中有气体放出,试推断 溶液的pH
溶液的pH___________ (填“大于”、“小于”或“等于”)7。
(5)工业上以软锰矿(主要成分为 )和黄铁矿(主要成分为
)和黄铁矿(主要成分为 )为主要原料制备碳酸锰的工艺流程中,加入NaF的目的是除去溶液中的
)为主要原料制备碳酸锰的工艺流程中,加入NaF的目的是除去溶液中的 ,若溶液中
,若溶液中 浓度为0.001
浓度为0.001 ,取等体积的该溶液与NaF溶液混合,要使反应发生,则NaF溶液的浓度至少为
,取等体积的该溶液与NaF溶液混合,要使反应发生,则NaF溶液的浓度至少为___________  [已知:
[已知: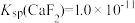 ]。
]。
(1)混合溶液的pH=8的原因:
(2)混合溶液中由水电离出的c(H+)
(3)求出混合液中下列算式的精确计算结果(填具体数字):

(4)已知
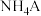 溶液为中性,又知HA溶液加到
溶液为中性,又知HA溶液加到 溶液中有气体放出,试推断
溶液中有气体放出,试推断 溶液的pH
溶液的pH(5)工业上以软锰矿(主要成分为
 )和黄铁矿(主要成分为
)和黄铁矿(主要成分为 )为主要原料制备碳酸锰的工艺流程中,加入NaF的目的是除去溶液中的
)为主要原料制备碳酸锰的工艺流程中,加入NaF的目的是除去溶液中的 ,若溶液中
,若溶液中 浓度为0.001
浓度为0.001 ,取等体积的该溶液与NaF溶液混合,要使反应发生,则NaF溶液的浓度至少为
,取等体积的该溶液与NaF溶液混合,要使反应发生,则NaF溶液的浓度至少为 [已知:
[已知: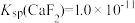 ]。
]。
您最近一年使用:0次
10 . (1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为_______ ;同质量的氨气和硫化氢气体体积比为_______ ,若二者氢原子数相等,则它们的体积比为_______ 。
(2)一氧化碳和二氧化碳的混合气体18 g,完全燃烧后测得二氧化碳的体积为11.2 L(标准状况)。试回答:
①混合气体中一氧化碳的质量是_______ 。
②混合气体中二氧化碳在标准状况下的体积是_______ 。
(3)实验室用密度为1.25 g·mL-1,质量分数为36.5%的浓盐酸配制240 mL 0.1 mol·L-1的盐酸,请回答下列问题:
①浓盐酸的物质的量浓度为_______ 。
②配制240 mL 0.1 mol·L-1的盐酸,应量取浓盐酸体积_______ mL。
(2)一氧化碳和二氧化碳的混合气体18 g,完全燃烧后测得二氧化碳的体积为11.2 L(标准状况)。试回答:
①混合气体中一氧化碳的质量是
②混合气体中二氧化碳在标准状况下的体积是
(3)实验室用密度为1.25 g·mL-1,质量分数为36.5%的浓盐酸配制240 mL 0.1 mol·L-1的盐酸,请回答下列问题:
①浓盐酸的物质的量浓度为
②配制240 mL 0.1 mol·L-1的盐酸,应量取浓盐酸体积
您最近一年使用:0次



