1 . 用18mol·L-1浓硫酸配制100mL3.0mol·L-1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④转移、洗涤⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是___________ ,量取浓硫酸所用的量筒的规格是___________ (从下列中选用)。
A.10mL B.25mL C.50mL D.100mL
(2)第③步实验的操作是___________ 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中___________ ;
B.容量瓶用蒸馏洗涤后残留有少量的水___________ ;
C.所用过的烧杯、玻璃棒未洗涤___________ ;
D.定容时俯视刻度线___________ 。
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④转移、洗涤⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是
A.10mL B.25mL C.50mL D.100mL
(2)第③步实验的操作是
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
您最近一年使用:0次
解题方法
2 . (I).请按要求写出下列反应的离子方程式。
(1)铝和烧碱溶液反应___________ 。
(2)向 溶液中滴加过量浓氨水
溶液中滴加过量浓氨水___________ 。
(II).氧气是支持生命活动的一种重要物质,回答下列问题:
(3)氧气的摩尔质量为___________ 。
(4)现有0.5molO2,含氧原子物质的量为___________ ,含氧分子数为___________ 个,其体积(标准状况)为___________ ,其质量为___________ 。
(5)氧气与炭在一定条件下发生反应可以生成 CO和CO2.在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的物质的量之比是___________ 。
(1)铝和烧碱溶液反应
(2)向
 溶液中滴加过量浓氨水
溶液中滴加过量浓氨水(II).氧气是支持生命活动的一种重要物质,回答下列问题:
(3)氧气的摩尔质量为
(4)现有0.5molO2,含氧原子物质的量为
(5)氧气与炭在一定条件下发生反应可以生成 CO和CO2.在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的物质的量之比是
您最近一年使用:0次
3 . 按要求填空:

(1)有机物的名称为_______ ,与足量H2反应后所得生成物名称为_______ 。
(2)分子式为C4H8的有机物中,属于烯烃的物质有_______ 种,其中存在顺反异构现象的物质的结构简式为______ 。
(3) 转化为
转化为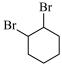 的化学方程式为:
的化学方程式为:______ 。
(4)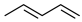 中共面的原子最多有
中共面的原子最多有______ 个,与溴发生加成反应的产物最多有______ 种。

(1)有机物的名称为
(2)分子式为C4H8的有机物中,属于烯烃的物质有
(3)
 转化为
转化为 的化学方程式为:
的化学方程式为:(4)
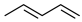 中共面的原子最多有
中共面的原子最多有
您最近一年使用:0次
4 . 按要求填空:
(1)将80克NaOH溶解于水中,配成5L溶液,则NaOH的物质的量浓度是
(2)在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为
(3)某些化学反应可以表示为A+B→C+D+H2O,若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(4)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(5)某+3价阳离子(M3+)含有24个电子,它的质量数为56,该离子核内中子数为
您最近一年使用:0次
解题方法
5 . 选择相应的试剂或操作方法除去下列各物质的杂质(括号内为杂质),并按要求写出化学或离子方程式。
(1)Fe(Al):试剂___________ ,化学方程式为___________ 。
(2)FeCl3(FeCl2):试剂___________ ,离子方程式为___________ 。
(3)Na2CO3固体(NaHCO3固体):方法___________ ,化学方程式为___________ 。
(1)Fe(Al):试剂
(2)FeCl3(FeCl2):试剂
(3)Na2CO3固体(NaHCO3固体):方法
您最近一年使用:0次
解题方法
6 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:

(1)写出工业上由食盐制备
 的离子方程式:
的离子方程式:(2)步骤Ⅰ中已获得
 ,步骤Ⅱ中又将
,步骤Ⅱ中又将 转化为
转化为 和
和 ,其目的是
,其目的是(3)步骤Ⅱ中通入热空气吹出
 ,利用了
,利用了 的___________(填标号)。
的___________(填标号)。| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(4)步骤Ⅱ中用纯碱溶液吸收
 ,该反应的化学方程式为
,该反应的化学方程式为(5)从理论上考虑,下列物质也能吸收
 的是___________(填标号)。
的是___________(填标号)。A. | B.NaCl溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(6)查阅资料知,
 的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
您最近一年使用:0次
7 . 按要求填空:现有7种物质:①Na、②FeCl3溶液、③稀盐酸、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl晶体。
(1)属于非电解质的是___________ ;上述状态下的物质能导电的电解质有 ___________ (填序号)。
(2)制备⑥的方法是:在小烧杯中加入40mL蒸馏水,加热至沸腾后,向烧杯中加入5至6滴FeCl3饱和溶液,继续煮沸至液体呈___________ 色,即可制得Fe(OH)3胶体。区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是 ___________ 。
(3)FeCl3在水溶液中的电离方程式是___________ 。
(1)属于非电解质的是
(2)制备⑥的方法是:在小烧杯中加入40mL蒸馏水,加热至沸腾后,向烧杯中加入5至6滴FeCl3饱和溶液,继续煮沸至液体呈
(3)FeCl3在水溶液中的电离方程式是
您最近一年使用:0次
8 . 现有下列10种物质:①铝,②纯碱,③CO2,④稀H2SO4,⑤Ba(OH)2固体,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙固体,⑩乙醇。
(1)上述物质中属于电解质的有___________ ,属于混合物的有___________ (填序号),属于盐的有___________ 。(填序号)
(2)写出⑧在水中的电离方程式为___________ 。
(3)少量③通入⑤的溶液中发生反应的离子反应方程式为___________ 。
(4)⑦和⑨混合反应的离子反应方程式为___________ 。
(5)④和⑤的稀溶液混合至中性时的离子方程式___________ 。
(1)上述物质中属于电解质的有
(2)写出⑧在水中的电离方程式为
(3)少量③通入⑤的溶液中发生反应的离子反应方程式为
(4)⑦和⑨混合反应的离子反应方程式为
(5)④和⑤的稀溶液混合至中性时的离子方程式
您最近一年使用:0次
9 . 回答下列问题:
(1)已知H2A在水中发生电离:H2A=H++HA-,HA-⇌H++A2-。
①向H2A稀溶液中加入少量NaHA固体,溶液的pH_______ (填“增大”“减小”或“不变”)。
②常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)⇌Ca2+(aq)+A2-(aq)。加入少量Na2A固体,c(Ca2+)_______ (填“增大”“减小”或“不变”),原因是_______ 。
(2)含有Cr2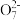 的废水毒性较大。经化学分析,某工厂废水中Cr2
的废水毒性较大。经化学分析,某工厂废水中Cr2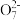 的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2
的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2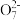
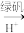 Cr3+、Fe3+
Cr3+、Fe3+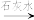 Cr(OH)3、Fe(OH)3。
Cr(OH)3、Fe(OH)3。
①在废水中加入FeSO4·7H2O和稀硫酸,发生反应的离子方程式为_______ 。
②已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Cr(OH)3]=7.0×10-31。若处理后的废水中残留的c(Fe3+)=2.0×10-14mol·L-1,则残留的Cr3+的浓度为_______ 。
(1)已知H2A在水中发生电离:H2A=H++HA-,HA-⇌H++A2-。
①向H2A稀溶液中加入少量NaHA固体,溶液的pH
②常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)⇌Ca2+(aq)+A2-(aq)。加入少量Na2A固体,c(Ca2+)
(2)含有Cr2
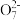 的废水毒性较大。经化学分析,某工厂废水中Cr2
的废水毒性较大。经化学分析,某工厂废水中Cr2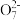 的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2
的浓度为4.00×10-3mol·L-1。为使废水能达标排放,作如下处理:Cr2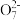
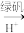 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3。
Cr(OH)3、Fe(OH)3。①在废水中加入FeSO4·7H2O和稀硫酸,发生反应的离子方程式为
②已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Cr(OH)3]=7.0×10-31。若处理后的废水中残留的c(Fe3+)=2.0×10-14mol·L-1,则残留的Cr3+的浓度为
您最近一年使用:0次
10 . 碳酸钠是一种重要的化工原料,在生产、生活和实验研究中均有广泛应用。下面是与碳酸钠溶液相关问题的探讨,请按要求回答问题。
(1)实验室需配制240mL0.2mol/LNa2CO3溶液,请回答下列问题:
①实验中除了用到托盘天平、药匙、量筒、烧杯、玻璃棒、胶体滴管外,还需用到的玻璃仪器有______ 。
②通过计算可知,该实验需要用托盘天平称量______ gNa2CO3·10H2O。
③经测定实际配得溶液的浓度为0.19mol/L,原因不可能______ (填序号)。
a.转移溶液前容量瓶内有少量蒸馏水
b.定容摇匀后,发现液面下降,继续加水至刻度线
c.转移溶液后未洗涤烧杯
d.定容时俯视刻度线
(2)联合制碱法改进国外的纯碱生产工艺,使原料氯化钠的利用率从70%提高到90%以上,该生产方法在制得纯碱的同时,还可得到一种副产品。生产流程可简要表示如图:
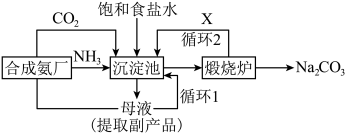
①煅烧炉中发生的化学方程式为______ 。
②产品碳酸钠中可能含有氯化钠,验证方法为______ 。
(1)实验室需配制240mL0.2mol/LNa2CO3溶液,请回答下列问题:
①实验中除了用到托盘天平、药匙、量筒、烧杯、玻璃棒、胶体滴管外,还需用到的玻璃仪器有
②通过计算可知,该实验需要用托盘天平称量
③经测定实际配得溶液的浓度为0.19mol/L,原因不可能
a.转移溶液前容量瓶内有少量蒸馏水
b.定容摇匀后,发现液面下降,继续加水至刻度线
c.转移溶液后未洗涤烧杯
d.定容时俯视刻度线
(2)联合制碱法改进国外的纯碱生产工艺,使原料氯化钠的利用率从70%提高到90%以上,该生产方法在制得纯碱的同时,还可得到一种副产品。生产流程可简要表示如图:

①煅烧炉中发生的化学方程式为
②产品碳酸钠中可能含有氯化钠,验证方法为
您最近一年使用:0次



