1 . 把少量锌粒加入足量稀硫酸中,锌粒完全溶解,生成2.24L氢气(标准状况下)。化学方程式为: ,请计算:
,请计算:
(1)生成氢气的物质的量________ 。
(2)参加反应的锌的质量________ 。
 ,请计算:
,请计算:(1)生成氢气的物质的量
(2)参加反应的锌的质量
您最近一年使用:0次
解题方法
2 . 2.7g纯净的铝片与足量稀硫酸完全反应,化学方程式为: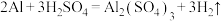 。请计算:
。请计算:
(1)参加反应的铝片的物质的量_______ 。
(2)标准状况下,生成氢气的体积_______ 。
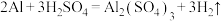 。请计算:
。请计算:(1)参加反应的铝片的物质的量
(2)标准状况下,生成氢气的体积
您最近一年使用:0次
解题方法
3 . 元素在周期表中的位置反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题:
(1)元素①位于元素周期表的第_______ 周期第_______ 族,它是形成化合物种类最多的元素。
(2)写出②的元素符号_______ 。
(3)画出元素④的原子结构示意图_______ 。
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是_______ (填化学式)。
(5)比较⑦和⑧的简单离子半径大小_______ >_______ (填离子符号)。
(6)写出元素⑧的单质与水反应的化学方程式:_______ 。
族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)写出②的元素符号
(3)画出元素④的原子结构示意图
(4)元素③和⑤的最高价氧化物对应的水化物中碱性较强的是
(5)比较⑦和⑧的简单离子半径大小
(6)写出元素⑧的单质与水反应的化学方程式:
您最近一年使用:0次
2023-03-15更新
|
489次组卷
|
3卷引用:云南省2022-2023学年高二下学期普通高中学业水平考试化学试题
4 . 元素在周期表中的位置,反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题。
(1)元素⑤位于周期表中的第___________ 周期第___________ 族。
(2)④⑥两种元素形成的化合物可用作防腐剂,常用于腌制食物,该化合物的电子式为______ ,高温灼烧该化合物时,火焰呈________ 色。
(3)①②③三种元素中,原子半径最小的是___________ (填元素符号)。
(4)④⑦两种元素最高价氧化物对应的水化物碱性较强的是___________ (填化学式)。
(5)①⑥两种元素的简单氢化物相遇会迅速反应,产生大量白烟,请写出该反应的化学方程式_____ 。
| He | |||||||||||||||||
| ① | ② | ③ | Ne | ||||||||||||||
| ④ | ⑤ | ⑥ | Ar | ||||||||||||||
| ⑦ | Kr |
(2)④⑥两种元素形成的化合物可用作防腐剂,常用于腌制食物,该化合物的电子式为
(3)①②③三种元素中,原子半径最小的是
(4)④⑦两种元素最高价氧化物对应的水化物碱性较强的是
(5)①⑥两种元素的简单氢化物相遇会迅速反应,产生大量白烟,请写出该反应的化学方程式
您最近一年使用:0次
2022-01-11更新
|
651次组卷
|
3卷引用:云南省2021年高二上学期期末普通高中学业水平考试化学(新教材)试题
5 . I.如图为维生素C的结构简式,回答下列问题:
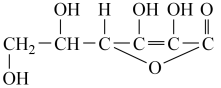
(1)维生素C由_______ 种元素组成。
(2)维生素C属于_______ (填“脂溶性”或“水溶性”)维生素。
(3)维生素C属于_______ (填“小分子”或“高分子”)有机化合物。
II.化学与人类生活密切相关。回答下列问题:
(4)下列药物既有解热镇痛作用,又有防止心脏病发作,减缓老年人视力衰退和提高免疫功能的是_______ (填序号)
A.阿司匹林B.青霉素C.小苏打抗酸药片
(5)硬铝合金中含Cu4%、Mg0.5%、Mn0.5%、Si0.7%,是制作飞机和宇宙飞船的理想材料。硬铝合金具有较多优点,写出其中一点_______ 。
(6)铁合金在食盐水中发生电化学腐蚀(吸氧腐蚀)的正极反应为O2+2H2O+4e-=4OH-,其负极反应式为_______ 。
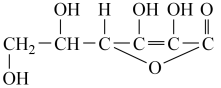
(1)维生素C由
(2)维生素C属于
(3)维生素C属于
II.化学与人类生活密切相关。回答下列问题:
(4)下列药物既有解热镇痛作用,又有防止心脏病发作,减缓老年人视力衰退和提高免疫功能的是
A.阿司匹林B.青霉素C.小苏打抗酸药片
(5)硬铝合金中含Cu4%、Mg0.5%、Mn0.5%、Si0.7%,是制作飞机和宇宙飞船的理想材料。硬铝合金具有较多优点,写出其中一点
(6)铁合金在食盐水中发生电化学腐蚀(吸氧腐蚀)的正极反应为O2+2H2O+4e-=4OH-,其负极反应式为
您最近一年使用:0次
解题方法
6 . 下表是元素周期表的一部分,按要求完成各小题。
(1)元素①的原子结构示意图为_______ ,元素④的原子的电子式为_______ 。
(2)元素②的最简单氢化物的化学式为_______ , 该物质与O2完全燃烧时的化学反应方程式为_______ 。
(3)上述6种元素对应的化合物中,最高价氧化物对应水化物碱性最强的是_______ (填化学式),最高价氧化物对应水化物具有两性的是_______ (填化学式),两者发生反应的离子方程式为_______ 。
| ① | He | ||||||
| ② | ③ | Ne | |||||
| ④ | ⑤ | ⑥ | Ar |
(2)元素②的最简单氢化物的化学式为
(3)上述6种元素对应的化合物中,最高价氧化物对应水化物碱性最强的是
您最近一年使用:0次
7 . 联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性,图中表示了元素周期表中属期的一部分,①~⑦代表10种短周期元素。
(1)七种元素中化学性质最不活泼的是_______ (填元素符号),形成化合物数目最多的元素是_______ (填元素符号)
(2)元素②的最低价阴离子的离子结构示意图是_______ 。
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是_______ (填化学式)。
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是_______ (填化学式)。
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为:_______ 。
| ① | ② | ||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
(2)元素②的最低价阴离子的离子结构示意图是
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为:
您最近一年使用:0次
2021-07-11更新
|
473次组卷
|
4卷引用:云南省2020-2021学年高一下学期普通高中学业水平考试化学试题
解题方法
8 . I.图为某品牌鲜花饼标签的一部分,其配料表中

(1)富含淀粉的是_______ 。
(2)属于防腐剂的是_______ 。
(3)富含蛋白质的是_______ 。
II.材料是人类社会生活的物质基础,材料创新则是科技进步的集中体现。
(4)聚对苯二甲酰对苯二胺纤维俗称“凯夫拉”,具有密度低、强度高、韧性好、耐高温、
易于加工和成型等特点,是防弹衣的优质选材,它属于_______ (填选项)。
A.金属材料 B.无机非金属材料 C.有机高分子材料
(5)航时中供水管道多采用PE(聚乙烯)材料,聚乙烯的结构简式为_______ 。
(6)新型战斗机常用纳米SiC粉体作为吸波材料。高温分解Si(CH3)2Cl2可制得SiC,同时还生成CH4和一种常见酸性气体,写出该反应的化学方程式:_______ 。

(1)富含淀粉的是
(2)属于防腐剂的是
(3)富含蛋白质的是
II.材料是人类社会生活的物质基础,材料创新则是科技进步的集中体现。
(4)聚对苯二甲酰对苯二胺纤维俗称“凯夫拉”,具有密度低、强度高、韧性好、耐高温、
易于加工和成型等特点,是防弹衣的优质选材,它属于
A.金属材料 B.无机非金属材料 C.有机高分子材料
(5)航时中供水管道多采用PE(聚乙烯)材料,聚乙烯的结构简式为
(6)新型战斗机常用纳米SiC粉体作为吸波材料。高温分解Si(CH3)2Cl2可制得SiC,同时还生成CH4和一种常见酸性气体,写出该反应的化学方程式:
您最近一年使用:0次
9 . 根据表格中关于四种元素的相关信息,按要求回答下列问题:
(1)完成表中空白:①_______ ②_______ ③_______ ④_______
(2)丁元素的最高价氧化物对应水化物的化学式为_______ ,其与丙元素的最高价氧化物对应水化物反应的离子方程式为_______ 。
(3)乙与丁两元素形成化合物的电子式为_______ 。
(4)甲元素的氢化物中最简单的是_______ (填化学式),该氢化物光照时可与氯气发生取代反应生成一氯代物,其化学方程式为_______ 。
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子序数 | 11 | ③ | ||
| 元素符号 | ① | Cl | ||
| 原子结构示意图 | ② | |||
| 位置 | 第二周期第ⅣA族 | 第三周期第ⅢA族 | ④ |
(1)完成表中空白:①
(2)丁元素的最高价氧化物对应水化物的化学式为
(3)乙与丁两元素形成化合物的电子式为
(4)甲元素的氢化物中最简单的是
您最近一年使用:0次
解题方法
10 . 重金属离子会污染水体。某化学兴趣小组设计如图流程除去工业废水(含有K+、Fe3+、Ag+ )中的重金属离子:

回答下列问题:
(1)操作①是_______ 。
(2)滤渣2的化学式为_______ 。
(3)检验工业废水是否含有K+的方法是_______ 。

回答下列问题:
(1)操作①是
(2)滤渣2的化学式为
(3)检验工业废水是否含有K+的方法是
您最近一年使用:0次



