1 . 某温度时,在2L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
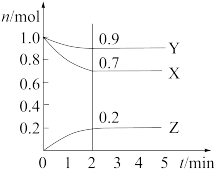
(1)该反应的化学方程式为___________ 。反应进行到2min时,正反应速率和逆反应速率___________ (填“相等”或“不相等”)
(2)反应开始至2min,用Y表示的平均反应速率为___________ ,X的转化率为___________ 。混合气中Y的体积分数为___________ 。
(3)在密闭容器里,通入amolA(g)和bmolB(g),发生反应A(g)+B(g)=2C(g),当改变下列条件时,会加快反应速率的是___________ (填序号)。
①降低温度②保持容器的体积不变,充入氦气
③加入催化剂④保持容器的体积不变,增加A(g)的物质的量

(1)该反应的化学方程式为
(2)反应开始至2min,用Y表示的平均反应速率为
(3)在密闭容器里,通入amolA(g)和bmolB(g),发生反应A(g)+B(g)=2C(g),当改变下列条件时,会加快反应速率的是
①降低温度②保持容器的体积不变,充入氦气
③加入催化剂④保持容器的体积不变,增加A(g)的物质的量
您最近一年使用:0次
解题方法
2 . 下图中的实线表示元素周期表的边界。①~⑦分别表示元素周期表中对应位置的元素。

(1)⑤在周期表中的位置是第三周期第___________ 族;⑦的原子结构示意图为___________ 。
(2)上述元素所能形成的简单离子中半径最小的是___________ (填离子符号),⑥⑦两元素非金属性较强的是(写元素符号)___________ 。
(3)元素①的简单氢化物电子式为___________ 。
(4)⑦的氢化物的还原性比元素⑥的氢化物的还原性___________ (填“强”或“弱”)。

(1)⑤在周期表中的位置是第三周期第
(2)上述元素所能形成的简单离子中半径最小的是
(3)元素①的简单氢化物电子式为
(4)⑦的氢化物的还原性比元素⑥的氢化物的还原性
您最近一年使用:0次
3 . A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
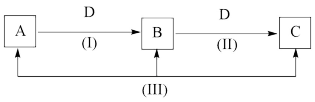
(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为___________ ;D中化学键的类型为___________ (填“离子键”或“共价键”)
②反应Ⅲ的离子方程式是___________ 。
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:___________ 、___________ 。
(3)写出Al(OH)3受热分解的化学方程式:___________ 。

(1)若A、B、C的焰色反应均为黄色,A的水溶液能使酚酞溶液呈红色,C为发酵粉的主要成分之一,D的过度排放会造成温室效应。
①B的化学式为
②反应Ⅲ的离子方程式是
(2)写出Na2O2做防毒面具时涉及到的化学反应的化学方程式:
(3)写出Al(OH)3受热分解的化学方程式:
您最近一年使用:0次
4 . 材料是人类赖以生存和发展的重要物质基础。
(1)合成橡胶、合成纤维和___________ 被称为三大合成材料。
(2)制造普通玻璃的三种原料的化学式为___________ 、CaCO3和SiO2.硅酸三钙是水泥的主要成分之一,3CaO•SiO2中Ca、Si、O三种元素的原子个数比为___________ ,水泥属于___________ (填字母)。
a、金属材料b、无机非金属材料c、有机高分子材料
(3)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式___________ 。
(1)合成橡胶、合成纤维和
(2)制造普通玻璃的三种原料的化学式为
a、金属材料b、无机非金属材料c、有机高分子材料
(3)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式
您最近一年使用:0次
5 . 水溶液中的离子平衡是以化学平衡理论为基础的进一步探究。
(1)常温下,等体积的0.10mol/L氨水与0.10mol/L烧碱溶液相比,c(OH-)的大小关系为前者_____ 后者(填“大于”“等于”或“小于”,下同);常温下,pH均为5的氯化铵溶液与盐酸相比,溶液中水的电离程度前者_____ 后者,两者均稀释10倍,pH的大小关系为前者_____ 后者。
(2)醋酸钠溶液呈碱性,其原因是_____ (用离子方程式表示)。
(3)常温下,Ksp(FeS)=6.3×10-18、Ksp(CuS)=1.3×10-36,则FeS的溶解度_____ CuS的溶解度(填“大于”“等于”或“小于”);在处理含有Cu2+的污水时,可向其中加入FeS固体作为沉淀剂,FeS逐渐溶解,Cu2+转化为CuS沉淀,用沉淀溶解平衡原理解释其原因为_____ 。
(1)常温下,等体积的0.10mol/L氨水与0.10mol/L烧碱溶液相比,c(OH-)的大小关系为前者
(2)醋酸钠溶液呈碱性,其原因是
(3)常温下,Ksp(FeS)=6.3×10-18、Ksp(CuS)=1.3×10-36,则FeS的溶解度
您最近一年使用:0次
2023-01-07更新
|
125次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
解题方法
6 . 化学反应过程中,不仅有物质的变化,同时还伴有能量的变化。
(1)如图所示的原电池装置中,银电极作_____ (填“正”或“负”)极,负极的电极反应式为_____ 。

(2)在镀件上镀铜时,铜电极作_____ (填“阳”或“阴”)极;工业上通过电解熔融NaCl制取金属钠,其电解总反应方程式为_____ 。
(3)实验在25℃、101kPa时,lmolCH4完全燃烧生成二氧化碳和液态水,放出的热量为890.31kJ/mol,则32gCH4在此状态下完全燃烧放出的热量为_____ kJ,该反应的热化学方程式为_____ 。
(1)如图所示的原电池装置中,银电极作

(2)在镀件上镀铜时,铜电极作
(3)实验在25℃、101kPa时,lmolCH4完全燃烧生成二氧化碳和液态水,放出的热量为890.31kJ/mol,则32gCH4在此状态下完全燃烧放出的热量为
您最近一年使用:0次
2023-01-07更新
|
136次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
7 . 材料是人类赖以生存和发展的重要物质基础。
(1)下列材料中属于合金的是_____ (填字母代号,下同):属下复合材料的是_____ ;属于纤维的是_____ 。
a.腈纶 b.玻璃钢 c.青铜 d.塑料
(2)生产普通玻璃的主要原料是石灰石、石英砂和_____ 。
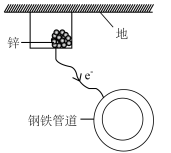
(3)用牺牲金属锌的方法来防止地下钢铁管道的腐蚀(如图所示),则钢铁管道作_____ 极,负极的电极反应电极方程为_____ 。
(1)下列材料中属于合金的是
a.腈纶 b.玻璃钢 c.青铜 d.塑料
(2)生产普通玻璃的主要原料是石灰石、石英砂和
(3)用牺牲金属锌的方法来防止地下钢铁管道的腐蚀(如图所示),则钢铁管道作

您最近一年使用:0次
2023-01-07更新
|
193次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
8 . 合理选择饮食和药物是保证身体健康的重要方面。
(1)正常情况下,人体血液的pH在7.35~7.45之间,呈弱_____ (填“酸性”或“碱性”,下同);食物的酸碱性是按食物在体内代谢最终产物的性质来分类的,按照这分类方式,鸡肉属于_____ 食物,水果中的柠檬属于_____ 食物。
(2)现有下列物质——青霉素、维生素C、阿司匹林、碳酸氢钠,其中具有解热镇痛作用的是_____ ;可做抗生素的是_____ ;可用于治疗胃酸过多的是_____ ,治疗时发生反应的离子方程式为_____ 。
(3)食用加入适量碘酸钾(KIO3)的食盐可以预防甲状腺肿大。现有一包加碘食盐,含碘0.0127g,则其中含KIO3的质量为_____ g。
(1)正常情况下,人体血液的pH在7.35~7.45之间,呈弱
(2)现有下列物质——青霉素、维生素C、阿司匹林、碳酸氢钠,其中具有解热镇痛作用的是
(3)食用加入适量碘酸钾(KIO3)的食盐可以预防甲状腺肿大。现有一包加碘食盐,含碘0.0127g,则其中含KIO3的质量为
您最近一年使用:0次
2023-01-07更新
|
98次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
解题方法
9 . 改善大气质量、进行污水处理和将垃圾资源化等要靠化学等科学的发展。
(1)为了保护环境,防治酸雨的方法是减少_____ 的排放(填“氟氯代烷”“SO2”或“N2”,下同);减缓臭氧层受损的方法是减少使用_____ 。
(2)垃圾是放错地方的资源。下列垃圾处理方式正确的是______ (填字母代号)。
a.回收利用易拉罐 b.焚烧废旧报纸 c.随意丢弃废旧电池
(3)可用过滤的方法对污水进行初步处理,过滤属于_____ (填“物理”或“化学”)方法:工业上可用中和法处理废水,现用Ca(OH)2处理含HCl的废水,反应的化学方程式为_____ 。
(4)ClO2可用于饮用水消毒。将Cl2通入NaClO2溶液中即可制得ClO2,反应的化学方程式为Cl2+2NaClO2=2X+2ClO2,则X的化学式为_____ 。
(1)为了保护环境,防治酸雨的方法是减少
(2)垃圾是放错地方的资源。下列垃圾处理方式正确的是
a.回收利用易拉罐 b.焚烧废旧报纸 c.随意丢弃废旧电池
(3)可用过滤的方法对污水进行初步处理,过滤属于
(4)ClO2可用于饮用水消毒。将Cl2通入NaClO2溶液中即可制得ClO2,反应的化学方程式为Cl2+2NaClO2=2X+2ClO2,则X的化学式为
您最近一年使用:0次
2023-01-07更新
|
218次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
名校
10 . 化学是一门以实验为基础的自然科学。掌握实验方法以及完成化学实验所必需的技能是学好化学的关键。请填写下列空白:
(1)把一小块绿豆大小的金属钠放入水中,可观察到的实验现象为______ (填字母代号:a,钠沉到水底b,钠熔成小球并快速移动),发生反应的化学方程式为______ ;实验室要把钠保存在______ 中。
(2)如图是探究氯气性质的实验装置图(夹持仪器略去)。
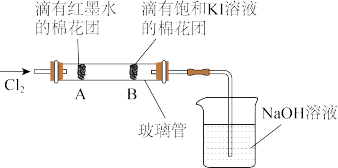
通入Cl2后,A处观察到的现象是______ ;B处有紫黑色的I2生成,反应的离子方程式为______ ,烧杯中NaOH溶液的作用是______ 。
(1)把一小块绿豆大小的金属钠放入水中,可观察到的实验现象为
(2)如图是探究氯气性质的实验装置图(夹持仪器略去)。

通入Cl2后,A处观察到的现象是
您最近一年使用:0次
2023-01-07更新
|
228次组卷
|
4卷引用:2021年河南省普通高中学生学业水平考试化学试题



