1 . 科学家开发了“氧化裂解技术”,将废弃物中的聚苯乙烯(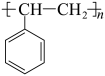 )转变为有用的苯甲酸(
)转变为有用的苯甲酸(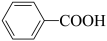 ),变废为宝。转变反应如下:
),变废为宝。转变反应如下: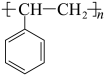
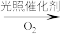
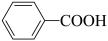 。结合上述材料,回答下列问题:
。结合上述材料,回答下列问题:
| A.属于氧化反应 | B.属于加聚反应 |
| C.发生了碳碳键的断裂 | D.反应物和产物都含有苯分子 |
(2)关于聚苯乙烯的说法正确的是___________。
| A.其单体是乙烯 | B.难溶于水 |
| C.可以制成泡沫包装材料 | D.难以自然降解,应回收处理 |
(3)苯乙烯的一些性质类似于乙烯。苯乙烯___________。
| A.属于烷烃 | B.属于不饱和烃 |
C.不能使溴的 溶液褪色 溶液褪色 | D.能使酸性 溶液褪色 溶液褪色 |
(4)苯甲酸的一些性质类似于乙酸。苯甲酸___________。
| A.可与Na反应 | B.可与NaOH反应 |
| C.一定条件下可与乙醇反应 | D.是一种常见的食品防腐剂 |
(5)一些苯环上有取代基的聚苯乙烯类高分子,也能利用上述的“氧化裂解技术”发生类似的反应。已知一种高分子R的结构如图。下列有关R的说法正确的是___________。
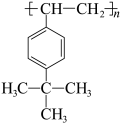
| A.能发生取代反应 | B.能在空气中燃烧 |
C.分子式为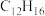 | D.能氧化裂解生成含羧基的物质 |
您最近一年使用:0次
2 . “民以食为天”,对元素周期表中有关元素的认识可使我们更好地了解食品的营养和安全。
结合上述材料,回答下列问题:
(1)仅含a、b、d三种元素的营养物质有___________。
(2)成熟水果会释放出由a和b按原子数目比 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。
(3)某些元素的单质或化合物常用于食品加工和保存。下列说法正确的是___________。
(4)土豆中富含淀粉。淀粉___________。
(5)由a、b、d和e四种元素形成的物质可用作糕点膨松剂。下列说法正确的是___________。
| 周期 | ⅠA | 0 | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h |
(1)仅含a、b、d三种元素的营养物质有___________。
| A.脂肪 | B.葡萄糖 | C.蛋白质 | D.氨基酸 |
 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。A.分子式为 | B.呈四面体结构 |
| C.呈三角锥形结构 | D.所有原子共平面 |
| A.a的单质可与植物油发生加成反应 | B.c的单质充入食品包装袋中可防腐 |
| C.f的单质制作的容器可用于贮存酸菜 | D.e和h形成的化合物可用于腌制食品 |
| A.遇碘溶液变色 | B.可水解得到乙醇 |
| C.由a、b、g三种元素组成 | D.水解的最终产物能发生银镜反应 |
| A.非金属性:b>a>d | B.原子半径:e>b>d |
| C.e的最高价氧化物的水化物是强碱 | D.b、d、e原子具有相同的电子层数 |
您最近一年使用:0次
3 . 下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。Na、Mg两种元素中,原子半径较大的是___________ 。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
(5)由碳与氢元素形成的最简单有机物的化学式为___________ ,该物质中碳元素与氢元素的质量比为___________ ,其分子立体构型为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
(5)由碳与氢元素形成的最简单有机物的化学式为
您最近一年使用:0次
解题方法
4 . 在1~18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
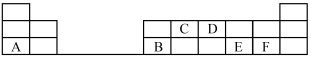
(1)写出D单质的电子式:___________ 。
(2)写出C的最高价氧化物的结构式:___________ 。
(3)E和F分别形成的气态氢化物中较稳定的是___________ (填氢化物的化学式)。
(4)A最高价氧化物的水化物所含化学键为___________ ,其水溶液与F单质反应的离子方程式为___________ 。

(1)写出D单质的电子式:
(2)写出C的最高价氧化物的结构式:
(3)E和F分别形成的气态氢化物中较稳定的是
(4)A最高价氧化物的水化物所含化学键为
您最近一年使用:0次
5 . 现以A为主要原料合成乙酸乙酯,其合成路线如图所示:
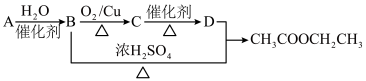
回答下列问题:
(1)写出C的结构简式:
(2)B、D分子中的官能团名称分别是
(3)写出A→B的反应类型:
(4)1 mol A与氯气发生完全加成反应,所得产物与氯气在光照的条件下发生完全取代反应,则两个过程中消耗的氯气的总的物质的量是
您最近一年使用:0次
解题方法
6 . 2021年10月20日,央视新闻报道:
a.2022年冬奥会火种抵达北京,火炬传递方案确定;
b.我国自主研制的世界最大推力整体式固体火箭发动机试车成功;
c.我国将加快推进汽车动力电池回收利用立法。
(1)关于奥运火炬燃料、固体火箭发动机燃料和汽车动力电池,下列说法正确的是___________ (填字母)。
A.作为奥运火炬燃料的主要成分,丙烷和丁烷互为同系物
B.固体火箭发动机燃料燃烧时,发生剧烈氧化还原反应
C.汽车动力电池只能将化学能转化为电能
(2)结合上述新闻报道,从多个角度谈谈你的认识___________ 。
a.2022年冬奥会火种抵达北京,火炬传递方案确定;
b.我国自主研制的世界最大推力整体式固体火箭发动机试车成功;
c.我国将加快推进汽车动力电池回收利用立法。
(1)关于奥运火炬燃料、固体火箭发动机燃料和汽车动力电池,下列说法正确的是
A.作为奥运火炬燃料的主要成分,丙烷和丁烷互为同系物
B.固体火箭发动机燃料燃烧时,发生剧烈氧化还原反应
C.汽车动力电池只能将化学能转化为电能
(2)结合上述新闻报道,从多个角度谈谈你的认识
您最近一年使用:0次
7 . 基于自然界可再生资源获得石油化工产品,是绿色化学的研究热点。一定条件下,以纤维素和淀粉为原料,制备对二甲苯 (PX) 的合成路线如下:
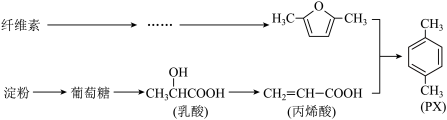
(1)下列关于纤维素、淀粉和葡萄糖的说法,正确的是
(2)乳酸的某些性质类似于乙醇和乙酸。下列关于乳酸的说法,正确的是
(3)化合物 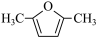 的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物
的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物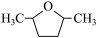 ,该反应类型为
,该反应类型为
(4)丙烯酸能通过原子利用率 100% 的加聚反应生成高分子化合物。下列化合物中,也能发生原子利用率100%的加聚反应的是
(5)化合物PX属于

(1)下列关于纤维素、淀粉和葡萄糖的说法,正确的是
| A.葡萄糖属于二糖 |
| B.葡萄糖可发生银镜反应 |
| C.稀酸催化下,纤维素和淀粉都能发生水解反应 |
| D.人体不能吸收纤维素,因此不宜食用含纤维素的食物 |
| A.分子式为C3H6O3 |
| B.能与NaOH反应 |
| C.能与CH3CH2OH发生酯化反应 |
| D.能与CH3COOH发生酯化反应 |
 的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物
的某些性质类似于乙烯,在一定条件下与H2反应,生成化合物 ,该反应类型为
,该反应类型为| A.取代反应 | B.加成反应 | C.氧化反应 | D.水解反应 |
| A.乙烷 | B.乙烯 | C.乙醇 | D.氯乙烯 |
| A.烷烃 | B.芳香烃 | C.链状烃 | D.不饱和烃 |
您最近一年使用:0次
8 . 分子筛是一类具有规整孔道结构的多孔材料,能够选择性吸附空间结构各异和不同尺寸的分子,在化学工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
(1)近期我国科学家制备了一种无缺陷的分子筛膜,可高效分离CH4与CO2两种气体。下列有关分子空间结构的描述正确的是_______
(2)传统的分子筛主要含有O、Na、Al和Si元素,通过调控这 4种元素的比例,可获得不同性能的分子筛产品。这4种元素描述中正确的是_______ 。
(3)通过将分子筛中的元素Na替换为K或Ca,可改变分子筛的孔径大小。这3种元素中说法正确的是_______
(4)N2常用于分子筛的孔结构测试,H、O和N元素可形成多种物质。下列说法正确的是_______
(5)某些分子筛可以选择性吸附Ar。Ar位于元素周期表的_______
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.CH4是平面结构 | B.CO2是V形结构 |
| C.CH4是正四面体结构 | D.CO2是直线形结构 |
| A.非金属性最强的是O |
| B.核外电子数最少的是 Na |
| C.金属性最强的是Al |
| D.原子半径最大的是Si |
| A.仅Na可与Cl2反应 |
| B.K的单质与水的反应最剧烈 |
| C.Na的氧化物与水的反应均为化合反应 |
| D.Ca的最高价氧化物的水化物碱性最强 |
| A.N2中含有共价三键 |
| B.NO可由NH3催化氧化得到 |
| C.NH3的水溶液呈碱性 |
| D.稀HNO3与Cu反应产生H2 |
| A.第二周期 | B.Ⅷ族 | C.第三周期 | D.0族 |
您最近一年使用:0次
9 . 填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:_______ 。
(2)原子符号为 X的元素属于第
X的元素属于第_______ 周期_______ 族。
(3)周期表中位于第8纵列的铁元素属于第_______ 族。
(4)周期表中第三周期最活泼的金属元素是_______ 。
(5)已知某微粒的结构示意图为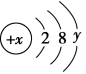 ,试回答下列问题:
,试回答下列问题:
①当x-y=10时,该微粒为_______ (填“原子”“阳离子”或“阴离子”)。
②当y=6时,元素最高价氧化物对应水化物的化学式为_______ 。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)原子符号为
 X的元素属于第
X的元素属于第(3)周期表中位于第8纵列的铁元素属于第
(4)周期表中第三周期最活泼的金属元素是
(5)已知某微粒的结构示意图为
 ,试回答下列问题:
,试回答下列问题:①当x-y=10时,该微粒为
②当y=6时,元素最高价氧化物对应水化物的化学式为
您最近一年使用:0次
2023-02-02更新
|
440次组卷
|
3卷引用:2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(一)
解题方法
10 . 亚硝酸是一种弱酸,Ka(HNO2)=5.6×10-4,NaNO2可用于滴定分析。
(1)常温下,0.1 mol/L的NaNO2溶液呈__________ (填“酸性”、“中性”或“碱性”);原因是__________ (用离子方程式表示)。
(2)0.1 mol/LNaNO2溶液中部分微粒组分及浓度如图所示,X表示的是_______ (填写微粒化学式)。c(NO2-)+c(HNO2)=__________ mol/L。

(3)NaNO2用于测药物中对氨基苯磺酸(Ar-NH2)的含量。测定原理为:酸性环境中,NaNO2先转化为HNO2:HX + NaNO2 = HNO2 + NaX,HNO2再与Ar-NH2以物质的量比1:1发生反应。
①下列酸中,能作为HX来使用的是_______ 。
A.醋酸(Ka=1.8×10-5) B.盐酸 C.次氯酸(Ka=4.0×10-8)
②反应体系中,Ar-NH2和少量KI共存时,HNO2会先与Ar-NH2完全反应后,再氧化KI。滴定时用KI-淀粉糊剂作指示剂,滴定终点时淀粉糊剂显_______ 色。
③用该法测定含 Ar-NH2(Mr=173)药物样品的纯度,每次取0.400g样品,用0.100mol/L NaNO2标准溶液进行滴定,实验结果如下:
则该样品中对氨基苯磺酸的纯度是__________ 。
第二次实验数据出现异常,造成这种异常的原因可能是________ (填代号)。
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.装标准溶液的滴定管未用标准溶液润洗
(4)已知298K时,H2CO3的Ka1=4.2×10-7、Ka2=5.61×10-11。将浓度均为0.1mol/L的Na2CO3及 HNO2溶液等体积混合,溶液中阴离子浓度由大到小的顺序为_______ 。
(1)常温下,0.1 mol/L的NaNO2溶液呈
(2)0.1 mol/LNaNO2溶液中部分微粒组分及浓度如图所示,X表示的是

(3)NaNO2用于测药物中对氨基苯磺酸(Ar-NH2)的含量。测定原理为:酸性环境中,NaNO2先转化为HNO2:HX + NaNO2 = HNO2 + NaX,HNO2再与Ar-NH2以物质的量比1:1发生反应。
①下列酸中,能作为HX来使用的是
A.醋酸(Ka=1.8×10-5) B.盐酸 C.次氯酸(Ka=4.0×10-8)
②反应体系中,Ar-NH2和少量KI共存时,HNO2会先与Ar-NH2完全反应后,再氧化KI。滴定时用KI-淀粉糊剂作指示剂,滴定终点时淀粉糊剂显
③用该法测定含 Ar-NH2(Mr=173)药物样品的纯度,每次取0.400g样品,用0.100mol/L NaNO2标准溶液进行滴定,实验结果如下:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗NaNO2溶液体积/mL | 20.12 | 20.90 | 20.00 | 19.88 |
第二次实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.装标准溶液的滴定管未用标准溶液润洗
(4)已知298K时,H2CO3的Ka1=4.2×10-7、Ka2=5.61×10-11。将浓度均为0.1mol/L的Na2CO3及 HNO2溶液等体积混合,溶液中阴离子浓度由大到小的顺序为
您最近一年使用:0次



