名校
解题方法
1 . 高铁酸钠 微溶于
微溶于 溶液,在碱性溶液中较稳定,溶液呈紫色,在酸性或中性溶液中快速产生
溶液,在碱性溶液中较稳定,溶液呈紫色,在酸性或中性溶液中快速产生 。某化学兴趣小组利用如图所示装置(夹持装置略),制取
。某化学兴趣小组利用如图所示装置(夹持装置略),制取 并探究有关性质。回答下列问题:
并探究有关性质。回答下列问题:___________ 。
(2)检查装置B气密性的方法:关闭 ,
, ,
,___________ ,则装置气密性良好。
(3)盛放氯酸钾的仪器名称为___________ ,装置B中试剂的作用为___________ 。
(4)装置C中产生 的离子方程式为
的离子方程式为___________ 。
(5)充分反应后,将装置C中所得混合物经净化处理后得到产品 ,进行如下性质探究:
,进行如下性质探究:
①净水作用:取适量样品溶于蒸馏水后,用一束光照射出现丁达尔效应,用离子方程式解释该出现该现象的原因:___________ 。
②强氧化性:将样品溶于 制成稀溶液,取该溶液滴入
制成稀溶液,取该溶液滴入 和足量
和足量 的混合溶液中,振荡后溶液呈浅紫色,证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,证明氧化性 。判断该实验设计是否合理并说明理由:
。判断该实验设计是否合理并说明理由:___________ 。
 微溶于
微溶于 溶液,在碱性溶液中较稳定,溶液呈紫色,在酸性或中性溶液中快速产生
溶液,在碱性溶液中较稳定,溶液呈紫色,在酸性或中性溶液中快速产生 。某化学兴趣小组利用如图所示装置(夹持装置略),制取
。某化学兴趣小组利用如图所示装置(夹持装置略),制取 并探究有关性质。回答下列问题:
并探究有关性质。回答下列问题: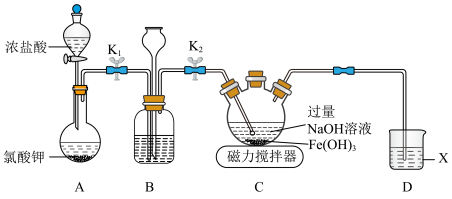
(2)检查装置B气密性的方法:关闭
 ,
, ,
,(3)盛放氯酸钾的仪器名称为
(4)装置C中产生
 的离子方程式为
的离子方程式为(5)充分反应后,将装置C中所得混合物经净化处理后得到产品
 ,进行如下性质探究:
,进行如下性质探究:①净水作用:取适量样品溶于蒸馏水后,用一束光照射出现丁达尔效应,用离子方程式解释该出现该现象的原因:
②强氧化性:将样品溶于
 制成稀溶液,取该溶液滴入
制成稀溶液,取该溶液滴入 和足量
和足量 的混合溶液中,振荡后溶液呈浅紫色,证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,证明氧化性 。判断该实验设计是否合理并说明理由:
。判断该实验设计是否合理并说明理由:
您最近一年使用:0次
2024-05-30更新
|
259次组卷
|
2卷引用:2023-2024学年广东省汕头市汕头金南实验学校三模化学试题
2 . 盐与碱的反应是水溶液中常见的反应,某学习小组展开相关探究。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=
①步骤a需要称量NaOH固体为______ g(保留一位小数)
②步骤b需要用到下图所示仪器中的______ (填名称)。______ mol·g-1
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关
(2)NH4Cl溶液显酸性,用离子方程式解释原因:______ 。
(3)小组同学设计实验探究[c )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
①实验结果显示,NaCl溶液不具备抗碱能力,即曲线______ (填曲线标号)表示溶液1.
②实验结果显示,当[c( )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液______ (填溶液组号)
③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=______ (精确至小数点后1位)。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=

①步骤a需要称量NaOH固体为
②步骤b需要用到下图所示仪器中的
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与
 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关(2)NH4Cl溶液显酸性,用离子方程式解释原因:
(3)小组同学设计实验探究[c
 )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示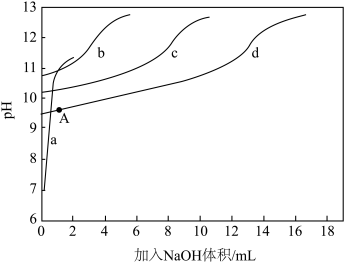
| 溶液组号 | 组成 | 体积/mL |
| 1 | 0.2mol·L-1NaCl溶液 | 15 |
| 2 | 0.1mol·L-1NH4Cl | 3 |
| 0.1mol·L-1氨水 | 12 | |
| 3 | 0.1mol·L-1NH4Cl | 7.5 |
| 0.1mol·L-1氨水 | 7.5 | |
| 4 | 0.1mol·L-1NH4Cl | 12 |
| 0.1mol·L-1氨水 | 3 |
②实验结果显示,当[c(
 )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=
您最近一年使用:0次
3 . 电解原理具有广泛的应用。某实验小组按照课本内容进行电解 溶液实验。
溶液实验。
(1)溶液配制:
①实验室在配制 溶液时需加入少许盐酸,目的是
溶液时需加入少许盐酸,目的是___________ ;氯化铜溶液中存在: (蓝色)
(蓝色) (黄色)
(黄色)
 ,加热盛有
,加热盛有 溶液的试管,试管中溶液颜色变为
溶液的试管,试管中溶液颜色变为___________ 。
②若要配制1000mL 2mol/L的 溶液,为使配制过程中不出现浑浊现象,至少需要滴加0.2mol/L的盐酸
溶液,为使配制过程中不出现浑浊现象,至少需要滴加0.2mol/L的盐酸___________ 滴。(已知: ,每滴溶液的体积约0.05mL,加入盐酸后溶液体积变化忽略不计)
,每滴溶液的体积约0.05mL,加入盐酸后溶液体积变化忽略不计)
(2)按下图装置进行电解饱和 溶液实验:阴极发生的电极反应为
溶液实验:阴极发生的电极反应为___________ ;阳极口放置湿润的淀粉 试纸可观察到
试纸可观察到___________ 。(填实验现象) 溶液一段时间后,阴极石墨棒上有异常现象:石墨棒上除有红色固体外还附着有大量白色固体。
溶液一段时间后,阴极石墨棒上有异常现象:石墨棒上除有红色固体外还附着有大量白色固体。
探究异常现象:
已知:ⅰ.相关物质颜色:铜(红色)、 (砖红色)、
(砖红色)、 (白色)、
(白色)、 (黄色,不稳定,易分解)。
(黄色,不稳定,易分解)。
ⅱ. 易溶于浓盐酸,
易溶于浓盐酸,
ⅲ. 在水中不稳定,易发生歧化反应。
在水中不稳定,易发生歧化反应。
经检验:红色固体中无 。
。
提出假设:红色固体是铜,白色固体是 。
。
验证假设:设计下表实验。
①上表中空格处应填写的内容是:Ⅰ___________ 、Ⅱ___________ 。
②实验B加水后出现白色沉淀的原因是___________ 。
结论:猜想正确。
(4)阴极生成 的电极反应式为
的电极反应式为___________ 。
 溶液实验。
溶液实验。(1)溶液配制:
①实验室在配制
 溶液时需加入少许盐酸,目的是
溶液时需加入少许盐酸,目的是 (蓝色)
(蓝色) (黄色)
(黄色)
 ,加热盛有
,加热盛有 溶液的试管,试管中溶液颜色变为
溶液的试管,试管中溶液颜色变为②若要配制1000mL 2mol/L的
 溶液,为使配制过程中不出现浑浊现象,至少需要滴加0.2mol/L的盐酸
溶液,为使配制过程中不出现浑浊现象,至少需要滴加0.2mol/L的盐酸 ,每滴溶液的体积约0.05mL,加入盐酸后溶液体积变化忽略不计)
,每滴溶液的体积约0.05mL,加入盐酸后溶液体积变化忽略不计)(2)按下图装置进行电解饱和
 溶液实验:阴极发生的电极反应为
溶液实验:阴极发生的电极反应为 试纸可观察到
试纸可观察到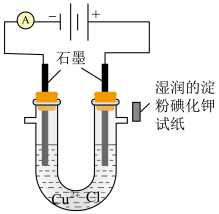
 溶液一段时间后,阴极石墨棒上有异常现象:石墨棒上除有红色固体外还附着有大量白色固体。
溶液一段时间后,阴极石墨棒上有异常现象:石墨棒上除有红色固体外还附着有大量白色固体。探究异常现象:
已知:ⅰ.相关物质颜色:铜(红色)、
 (砖红色)、
(砖红色)、 (白色)、
(白色)、 (黄色,不稳定,易分解)。
(黄色,不稳定,易分解)。ⅱ.
 易溶于浓盐酸,
易溶于浓盐酸,
ⅲ.
 在水中不稳定,易发生歧化反应。
在水中不稳定,易发生歧化反应。经检验:红色固体中无
 。
。提出假设:红色固体是铜,白色固体是
 。
。验证假设:设计下表实验。
| 序号 | 实验操作 | 实验现象 |
| A | 将有固体析出的石墨棒一端插入盛2mL稀硝酸试管中,反应完后取出,再向试管中滴加几滴 溶液 溶液 | 石墨棒上红色和白色物质都消失;无色溶液变Ⅰ,并有无色气体产生,在接近试管口处变红色;加入 溶液产生白色沉淀。 溶液产生白色沉淀。 |
| B | 将有固体析出的石墨棒一端插入盛2mLⅡ的试管中,反应完后取出,再向试管中加入一定量的水 | 石墨棒上红色固体不溶,白色固体消失,溶液无色;加水后出现白色沉淀。 |
②实验B加水后出现白色沉淀的原因是
结论:猜想正确。
(4)阴极生成
 的电极反应式为
的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . 高砷煤中含有砷硫铁(FeAsS)等物质。燃煤产生的烟气中含NO、 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
(1)燃煤固硫
①燃用高砷煤时加入生石灰将大部分硫元素转化为___________ (填化学式)留在煤渣中。
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为________________ 。
(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将 、NO、
、NO、 转化为
转化为 。烟气中含有的
。烟气中含有的 会使钒氧化物催化剂中毒。
会使钒氧化物催化剂中毒。
①在SCR脱硝的反应中还原剂为_______________ (填化学式)。
②研究发现砷中毒机理主要是 分子破坏了催化剂的Lewis酸位点,使
分子破坏了催化剂的Lewis酸位点,使 数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构
数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构__________ 。 不易使催化剂中毒。但与
不易使催化剂中毒。但与 相比,
相比, 更不利于脱硝反应的进行,其原因是
更不利于脱硝反应的进行,其原因是_______________ 。
(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量( 或铵盐)会影响水泥的性能。
或铵盐)会影响水泥的性能。
①取50.00 g粉煤灰加入NaOH蒸出 ,用20 mL 0.1000 mol⋅L
,用20 mL 0.1000 mol⋅L 的
的 溶液吸收
溶液吸收 ,用0.2000mol⋅L
,用0.2000mol⋅L NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以 计的氨含量
计的氨含量___________ (用mg⋅g 表示,写出计算过程)。
表示,写出计算过程)。
②相同烟气所得脱硝粉煤灰(经过SCR脱硝后获得)与未脱硝粉煤灰(直接沉降获得)加水后溶解后,所得浆液pH随时间的变化如图所示。脱硝粉煤灰pH始终比未脱硝粉煤灰低的原因是___________ 。
 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。(1)燃煤固硫
①燃用高砷煤时加入生石灰将大部分硫元素转化为
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成
 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将
 、NO、
、NO、 转化为
转化为 。烟气中含有的
。烟气中含有的 会使钒氧化物催化剂中毒。
会使钒氧化物催化剂中毒。①在SCR脱硝的反应中还原剂为
②研究发现砷中毒机理主要是
 分子破坏了催化剂的Lewis酸位点,使
分子破坏了催化剂的Lewis酸位点,使 数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构
数量减少(产物中As化合价为+3、+5)。请补充完整产物的结构
 不易使催化剂中毒。但与
不易使催化剂中毒。但与 相比,
相比, 更不利于脱硝反应的进行,其原因是
更不利于脱硝反应的进行,其原因是(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量(
 或铵盐)会影响水泥的性能。
或铵盐)会影响水泥的性能。①取50.00 g粉煤灰加入NaOH蒸出
 ,用20 mL 0.1000 mol⋅L
,用20 mL 0.1000 mol⋅L 的
的 溶液吸收
溶液吸收 ,用0.2000mol⋅L
,用0.2000mol⋅L NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00 mL,计算粉煤灰中的以 计的氨含量
计的氨含量 表示,写出计算过程)。
表示,写出计算过程)。②相同烟气所得脱硝粉煤灰(经过SCR脱硝后获得)与未脱硝粉煤灰(直接沉降获得)加水后溶解后,所得浆液pH随时间的变化如图所示。脱硝粉煤灰pH始终比未脱硝粉煤灰低的原因是

您最近一年使用:0次
2024-03-24更新
|
752次组卷
|
3卷引用:2023-2024学年广东省汕头市汕头金南实验学校三模化学试题
5 . 铜及其化合物在生产及生活中应用广泛。
(1)铜-铁催化剂可用于电催化还原 为
为 ,完成下列离子方程式:
,完成下列离子方程式:__________ 。
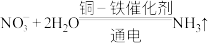 +______+______
+______+______
(2)铜-铁催化剂还可以催化 分解转化为燃料氢气,反应为
分解转化为燃料氢气,反应为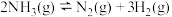
 。往体积为
。往体积为 的密闭容器中加入
的密闭容器中加入 分解制
分解制 。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下,
。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下, 时
时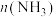 及
及 时
时 随时间的变化;曲线
随时间的变化;曲线 表示在铜-铁催化剂Ⅱ的作用下,
表示在铜-铁催化剂Ⅱ的作用下, 时
时 随时间的变化。
随时间的变化。
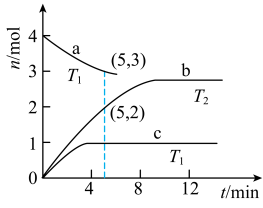
①
______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
②在铜-铁催化剂I的作用下, 时,
时, 内平均反应速率
内平均反应速率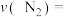
______  。
。
③上述三种条件下,分解反应的平衡常数 的大小关系为
的大小关系为______
(3)工业合成氨中,常用亚铜盐的氨水溶液除去原料气中的 ,反应的离子方程式为
,反应的离子方程式为 ,该反应的
,该反应的 。其他条件不变时,下列说法正确的有______(填字母)。
。其他条件不变时,下列说法正确的有______(填字母)。
(4)工业生产中采用水解中和法处理含铜废水。常温下,水溶贸中含铜微粒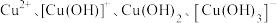 和
和 的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随
的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随 的变化曲线如图所示。
的变化曲线如图所示。
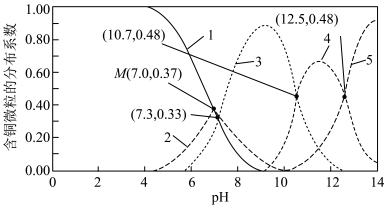
①曲线2代表的含铜微粒为____ 。
② 的平衡常数K=
的平衡常数K=____ 。
③若CuSO4溶液起始浓度为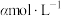 ,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度
,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度____ (写出计算过程,结果用含 的式子表示)。
的式子表示)。
(1)铜-铁催化剂可用于电催化还原
 为
为 ,完成下列离子方程式:
,完成下列离子方程式: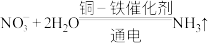 +______+______
+______+______(2)铜-铁催化剂还可以催化
 分解转化为燃料氢气,反应为
分解转化为燃料氢气,反应为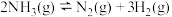
 。往体积为
。往体积为 的密闭容器中加入
的密闭容器中加入 分解制
分解制 。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下,
。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下, 时
时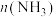 及
及 时
时 随时间的变化;曲线
随时间的变化;曲线 表示在铜-铁催化剂Ⅱ的作用下,
表示在铜-铁催化剂Ⅱ的作用下, 时
时 随时间的变化。
随时间的变化。
①

 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。②在铜-铁催化剂I的作用下,
 时,
时, 内平均反应速率
内平均反应速率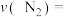
 。
。③上述三种条件下,分解反应的平衡常数
 的大小关系为
的大小关系为(3)工业合成氨中,常用亚铜盐的氨水溶液除去原料气中的
 ,反应的离子方程式为
,反应的离子方程式为 ,该反应的
,该反应的 。其他条件不变时,下列说法正确的有______(填字母)。
。其他条件不变时,下列说法正确的有______(填字母)。A. 与 与 的浓度相等时,反应达到平衡 的浓度相等时,反应达到平衡 |
B.平衡后增大 的浓度, 的浓度, 的转化率增大 的转化率增大 |
C.平衡后加水稀释, 与 与 的浓度之比增大 的浓度之比增大 |
D.可采用加热 溶液的方法实现 溶液的方法实现 的再生 的再生 |
(4)工业生产中采用水解中和法处理含铜废水。常温下,水溶贸中含铜微粒
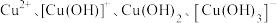 和
和 的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随
的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随 的变化曲线如图所示。
的变化曲线如图所示。
①曲线2代表的含铜微粒为
②
 的平衡常数K=
的平衡常数K=③若CuSO4溶液起始浓度为
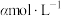 ,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度
,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度 的式子表示)。
的式子表示)。
您最近一年使用:0次
名校
6 . 工业排放的某些烟气中含有二氧化硫等大气污染物,对其进行脱硫治理不仅可以防止有害物质排放,还可以生产其他有用的产品。
(1) 分子的空间结构和分子的极性分别为___________。
分子的空间结构和分子的极性分别为___________。
(2)第一电离能: ,结合核外电子排布相关知识,说明其原因
,结合核外电子排布相关知识,说明其原因___________ 。
沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示: ,
, 的电离常数如下表所示:
的电离常数如下表所示:
(3)在吸收塔内,烟气应从吸收塔的___________ 通入,与塔顶喷淋的海水充分接触。
A.上部 B.中部 C.下部
(4)吸收塔内温度不宜过高,原因可能是___________ 。(列举1条)吸收塔内 和海水中
和海水中 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(5)若煤电厂排放烟气量为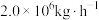 ,其中含
,其中含 为0.15%,该烟气经海水脱硫处理后
为0.15%,该烟气经海水脱硫处理后 为
为 ,则脱硫率
,则脱硫率
___________ 。( )
)
(6)离子液体(ILs)也可以用来处理工业烟气。ILs的负离子吸收 后生成
后生成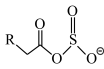 。欲确定
。欲确定 中虚线框内基团的结构,可采用的分析方法有___________。
中虚线框内基团的结构,可采用的分析方法有___________。
工业上还可用 溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
(7)为使 再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
(8)使用 溶液脱硫时,溶液的pH通常需控制在
溶液脱硫时,溶液的pH通常需控制在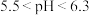 。结合
。结合 的性质和下图,分析pH不宜过小和过大的原因
的性质和下图,分析pH不宜过小和过大的原因___________ 。
(1)
 分子的空间结构和分子的极性分别为___________。
分子的空间结构和分子的极性分别为___________。| A.直线形,非极性 | B.直线形,极性 | C.角形,非极性 | D.角形,极性 |
(2)第一电离能:
 ,结合核外电子排布相关知识,说明其原因
,结合核外电子排布相关知识,说明其原因沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示:
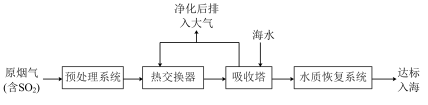
 ,
, 的电离常数如下表所示:
的电离常数如下表所示:| 弱酸 |  |  |
 | 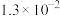 | 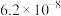 |
 | 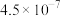 | 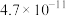 |
(3)在吸收塔内,烟气应从吸收塔的
A.上部 B.中部 C.下部
(4)吸收塔内温度不宜过高,原因可能是
 和海水中
和海水中 发生反应的离子方程式为
发生反应的离子方程式为(5)若煤电厂排放烟气量为
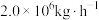 ,其中含
,其中含 为0.15%,该烟气经海水脱硫处理后
为0.15%,该烟气经海水脱硫处理后 为
为 ,则脱硫率
,则脱硫率
 )
)(6)离子液体(ILs)也可以用来处理工业烟气。ILs的负离子吸收
 后生成
后生成 。欲确定
。欲确定 中虚线框内基团的结构,可采用的分析方法有___________。
中虚线框内基团的结构,可采用的分析方法有___________。| A.原子发射光谱 | B.红外光谱 | C.核磁共振氢谱 | D.晶体X射线衍射 |
工业上还可用
 溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。(7)为使
 再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。A. | B.CaO | C. | D.NaOH |
(8)使用
 溶液脱硫时,溶液的pH通常需控制在
溶液脱硫时,溶液的pH通常需控制在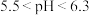 。结合
。结合 的性质和下图,分析pH不宜过小和过大的原因
的性质和下图,分析pH不宜过小和过大的原因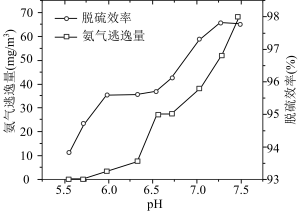
您最近一年使用:0次
2024-01-13更新
|
302次组卷
|
3卷引用:2023-2024学年广东省汕头市汕头金南实验学校三模化学试题
7 . Ⅰ.某化学兴趣小组的同学学了金属的电化学腐蚀,对教材叙述[钢铁在酸性环境中发生析氢腐蚀;在酸性很弱或呈中性,溶有 的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
(1)用图1所示装置进行实验:打开a________ (填仪器名称)的活塞,加入1mL溶液,测得压强随时间变化曲线如图2。
(2)同学乙认为甲的结论不科学,锥形瓶内压强变大还可能是___________ ,提出改进措施___________ 。改进后,再次实验,证明甲、乙的猜想均正确,请在图2绘制出改进后的曲线___________ 。
(3)同学丙认为甲、乙的实验不具代表性,建议用不同浓度的酸进行实验。在改进后的装置中分别用 、
、 的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是
的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是___________ 。
(4)对于图3中 时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中
时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中 浓度随时间的变化曲线如图4。
浓度随时间的变化曲线如图4。 时,压强几乎不随时间改变是因为
时,压强几乎不随时间改变是因为___________ 。
综上,小组同学得出结论:教材表述科学严谨。
Ⅱ.拓展研究:
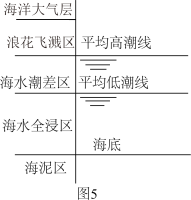
(5)侯保荣院士专门研究海洋钢架结构桥海洋大气层梁腐蚀,他发现腐蚀最严重的是浪花飞溅区浪花飞溅区(海洋环境分区如图5),请你解释原因___________ 。 浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的
浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的 完全转化为FeS,请写出该铁合金腐蚀的总反应
完全转化为FeS,请写出该铁合金腐蚀的总反应___________ (离子方程式)。___________ (任写一点即可)。
 的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。
的环境中发生吸氧腐蚀;钢铁等金属的腐蚀主要为吸氧腐蚀]产生疑问,决定用数字化实验模拟探究钢铁在酸性环境下的腐蚀情况。(1)用图1所示装置进行实验:打开a
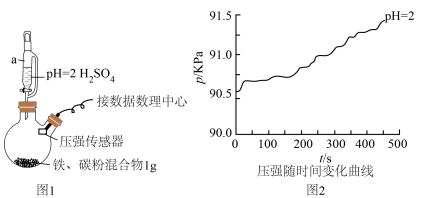
(2)同学乙认为甲的结论不科学,锥形瓶内压强变大还可能是
(3)同学丙认为甲、乙的实验不具代表性,建议用不同浓度的酸进行实验。在改进后的装置中分别用
 、
、 的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是
的硫酸实验,测定压强随时间变化情况,结果如图3.同学丙得出:酸性较弱时,铁会发生吸氧腐蚀,其依据是(4)对于图3中
 时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中
时,铁是否发生了腐蚀?同学们意见不统一,经讨论,他们把压强传感器换成氧气传感器,得出不同pH时装置中 浓度随时间的变化曲线如图4。
浓度随时间的变化曲线如图4。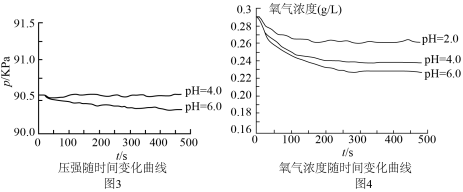
 时,压强几乎不随时间改变是因为
时,压强几乎不随时间改变是因为综上,小组同学得出结论:教材表述科学严谨。
Ⅱ.拓展研究:
(5)侯保荣院士专门研究海洋钢架结构桥海洋大气层梁腐蚀,他发现腐蚀最严重的是浪花飞溅区浪花飞溅区(海洋环境分区如图5),请你解释原因
 浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的
浓度很小的海底也有厌氧微生物(如硫酸盐还原菌SRB)对海洋钢制部件的腐蚀,其原理如图6,已知溶液中的 完全转化为FeS,请写出该铁合金腐蚀的总反应
完全转化为FeS,请写出该铁合金腐蚀的总反应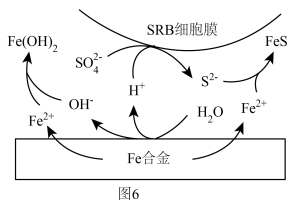
您最近一年使用:0次
2024-01-05更新
|
961次组卷
|
3卷引用:2024届广东东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学六校高三上学期第三次联考化学
名校
8 . 铁的化合物在水溶液中呈现丰富的颜色,这与其水解平衡和配位平衡有关。
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
(2)实验室用 溶液制备
溶液制备 胶体的化学反应方程式为
胶体的化学反应方程式为___________ 。
(3)实验小组为探究溶液 对
对 水解平衡的影响,在常温下设计了下列实验,通过测定透光率进行研究。
水解平衡的影响,在常温下设计了下列实验,通过测定透光率进行研究。
已知:① 水解程度越大,颜色越深
水解程度越大,颜色越深
②颜色越深,透光率越低
①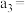
___________ ,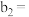
___________ 。
②由
___________  ,可证明:
,可证明: 减小,
减小, 的水解平衡逆向移动。(选填“>”“<”或“=”)
的水解平衡逆向移动。(选填“>”“<”或“=”)
③分析实验结果: ,同学甲推测原因可能是:
,同学甲推测原因可能是: (较深的黄色),并做了如下实验:
(较深的黄色),并做了如下实验:
试剂 为
为___________ ,可由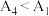 ,证实同学甲的推测。
,证实同学甲的推测。
通过对比___________ (填字母)的实验结果,证明 对
对 的水解平衡的影响。
的水解平衡的影响。
A.组别4与组别1 B.组别4与组别2 C.组别4与组别3
(4)为了探究 的热效应,同学乙设计了下列四组实验方案:
的热效应,同学乙设计了下列四组实验方案:
若实验结果为___________ ,则可证明: 为吸热反应。
为吸热反应。
(5)写出一种强酸弱碱盐(除 )及其用途:
)及其用途:___________ 。
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
| A | B | C | D |
配制 溶液 溶液 | 制备 胶体 胶体 | 观察胶体的丁达尔效应 | 分离 胶体与溶液 胶体与溶液 |
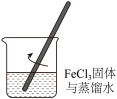 |  | 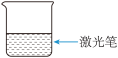 |  |
| A.A | B.B | C.C | D.D |
 溶液制备
溶液制备 胶体的化学反应方程式为
胶体的化学反应方程式为(3)实验小组为探究溶液
 对
对 水解平衡的影响,在常温下设计了下列实验,通过测定透光率进行研究。
水解平衡的影响,在常温下设计了下列实验,通过测定透光率进行研究。已知:①
 水解程度越大,颜色越深
水解程度越大,颜色越深②颜色越深,透光率越低
| 组别 |  溶液 溶液 | 蒸馏水 | 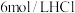 溶液 溶液 | 透光率 |
| 1 |  |  | 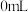 |  |
| 2 |  |  | 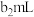 |  |
| 3 |  |  |  |  |
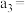
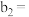
②由

 ,可证明:
,可证明: 减小,
减小, 的水解平衡逆向移动。(选填“>”“<”或“=”)
的水解平衡逆向移动。(选填“>”“<”或“=”)③分析实验结果:
 ,同学甲推测原因可能是:
,同学甲推测原因可能是: (较深的黄色),并做了如下实验:
(较深的黄色),并做了如下实验:| 组别 |  溶液 溶液 | 蒸馏水 | 试剂 | 透光率 |
| 4 |  |  |  |  |
 为
为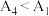 ,证实同学甲的推测。
,证实同学甲的推测。通过对比
 对
对 的水解平衡的影响。
的水解平衡的影响。A.组别4与组别1 B.组别4与组别2 C.组别4与组别3
(4)为了探究
 的热效应,同学乙设计了下列四组实验方案:
的热效应,同学乙设计了下列四组实验方案:| 组别 | 温度 | 试剂 | 透光率 |
| 5 |  |  溶液 溶液 | 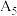 |
| 6 |  |  溶液 溶液 | 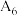 |
| 7 |  | 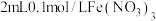 溶液 溶液 | 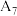 |
| 8 |  | 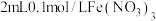 溶液 溶液 | 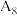 |
 为吸热反应。
为吸热反应。(5)写出一种强酸弱碱盐(除
 )及其用途:
)及其用途:
您最近一年使用:0次
2023-05-29更新
|
621次组卷
|
3卷引用:广东省华南师范大学附属中学2023届高三下学期第三次模拟考试化学试题
名校
9 . 以钛铁矿(主要成分为 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如图:
)的工艺流程如图:

已知:“溶浸”后的溶液中含金属元素的离子主要包括 、
、 、
、 、
、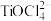 ;富铁元素主要以
;富铁元素主要以 形式存在;富钛渣中钛元素主要以
形式存在;富钛渣中钛元素主要以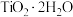 形式存在。
形式存在。
回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是___________ (答1条即可);“溶浸”过程 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为___________ 。
(3)“沉铁”过程中需控制 ,其目的是
,其目的是___________ (答1条即可)。
(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:___________ 。

(5) 的晶胞结构如图1所示,设该晶胞的边长为a nm,
的晶胞结构如图1所示,设该晶胞的边长为a nm, 为阿伏伽德罗常数的值。Ti的价电子排布式为
为阿伏伽德罗常数的值。Ti的价电子排布式为___________ ,该晶体的密度
___________ (填含a的计算式)g⋅cm-3; 的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。________

 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如图:
)的工艺流程如图:
已知:“溶浸”后的溶液中含金属元素的离子主要包括
 、
、 、
、 、
、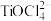 ;富铁元素主要以
;富铁元素主要以 形式存在;富钛渣中钛元素主要以
形式存在;富钛渣中钛元素主要以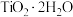 形式存在。
形式存在。回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是
 发生反应的离子方程式为
发生反应的离子方程式为(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为
(3)“沉铁”过程中需控制
 ,其目的是
,其目的是(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:

(5)
 的晶胞结构如图1所示,设该晶胞的边长为a nm,
的晶胞结构如图1所示,设该晶胞的边长为a nm, 为阿伏伽德罗常数的值。Ti的价电子排布式为
为阿伏伽德罗常数的值。Ti的价电子排布式为
 的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。
您最近一年使用:0次
2023-05-20更新
|
471次组卷
|
2卷引用:广东省部分学校2023届高三5月联合考试化学试题
名校
10 . 铜及其化合物有着广泛的应用。某实验小组探究 的性质。
的性质。
I.实验准备:
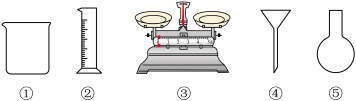
(1)由 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有_________ (填序号)。
实验任务:探究 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应
查阅资料:
已知:a.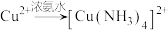 (深蓝色溶液)
(深蓝色溶液)
b. (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)
设计方案并完成实验:
现象分析与验证:
(2)推测实验B产生的无色气体为 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到__________ 。
(3)推测实验B中的白色沉淀为 ,实验验证步骤如下:
,实验验证步骤如下:
①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量________ ,观察到沉淀溶解,得到无色溶液,此反应的离子方程式为__________ ;露置在空气中一段时间,观察到溶液变为深蓝色。
(4)对比实验A、B,提出假设: 增强了
增强了 的氧化性。
的氧化性。
①若假设合理,实验B反应的离子方程式为
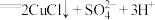 和
和__________ 。
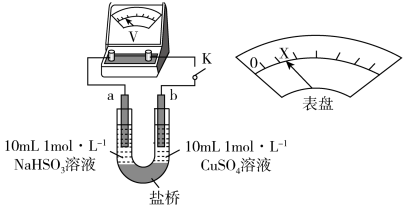
②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形__________ (补全实验操作及现象)。
Ⅱ. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子_________ (填化学式)。
(6)常见配合物的形成实验
 的性质。
的性质。I.实验准备:
(1)由
 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有
实验任务:探究
 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应查阅资料:
已知:a.
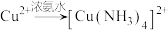 (深蓝色溶液)
(深蓝色溶液)b.
 (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)设计方案并完成实验:
实验 | 装置 | 试剂x | 操作及现象 |
A |
| 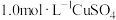 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 未见明显变化。 未见明显变化。 |
B | 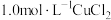 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
(2)推测实验B产生的无色气体为
 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到(3)推测实验B中的白色沉淀为
 ,实验验证步骤如下:
,实验验证步骤如下:①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量
(4)对比实验A、B,提出假设:
 增强了
增强了 的氧化性。
的氧化性。①若假设合理,实验B反应的离子方程式为

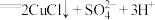 和
和②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形

Ⅱ.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子
(6)常见配合物的形成实验
实验操作 | 实验现象 | 有关离子方程式 |
| 滴加氨水后,试管中首先出现蓝色沉淀,氨水过量后沉淀逐渐 |  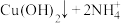   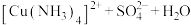 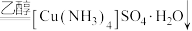 |
您最近一年使用:0次
2023-05-16更新
|
859次组卷
|
2卷引用:广东省梅州市2023届高三下学期第二次质检测试化学试题



 溶液
溶液