1 . 黄铜矿(CuFeS2)是工业炼铜,炼铁和制硫酸的重要原料。回答下列问题:
(1)铜元素位于元素周期表___________ 区,基态Fe2+的价层电子排布图(轨道表示式)是___________ 。
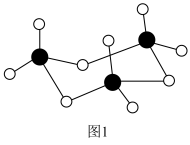
(2)气态SO3以单分子形式存在,其分子的空间结构为___________ 。固体:SO3中存在如图1所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。___________ 。
②该配离子中H—O—H的键角___________ (填“大于”、“小于”或“等于”)单个水分子中H—O——H的键角。
(4)①改性Fe3O4是一种优良的磁性材料,Fe3O4晶胞的 的结构如图3所示,研究发现结构中的Fe2+只可能出现在图中某一“▲”所示位置上,请确定Fe2+在晶胞中的位置是
的结构如图3所示,研究发现结构中的Fe2+只可能出现在图中某一“▲”所示位置上,请确定Fe2+在晶胞中的位置是___________ (填“a”或“b”或“c”)。
②普鲁士蓝晶体属于立方晶系,晶胞结构如图4所示(CN⁻在图中省略),该晶体的化学式为___________ 。
(1)铜元素位于元素周期表
(2)气态SO3以单分子形式存在,其分子的空间结构为

②该配离子中H—O—H的键角
(4)①改性Fe3O4是一种优良的磁性材料,Fe3O4晶胞的
 的结构如图3所示,研究发现结构中的Fe2+只可能出现在图中某一“▲”所示位置上,请确定Fe2+在晶胞中的位置是
的结构如图3所示,研究发现结构中的Fe2+只可能出现在图中某一“▲”所示位置上,请确定Fe2+在晶胞中的位置是②普鲁士蓝晶体属于立方晶系,晶胞结构如图4所示(CN⁻在图中省略),该晶体的化学式为

您最近一年使用:0次
2024-05-08更新
|
318次组卷
|
2卷引用:2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学
名校
解题方法
2 . 材料的发展水平始终是时代进步和人类文明的标志。当前含铁的磁性材料在国防、电子信息等领域中具有广泛应用。请回答下列问题:
(1)基态铁原子的价电子排布图为_______ ,基态铁原子核外电子的空间运动状态有_______ 种, 其处在最高能层的电子的电子云形状为_______ 。
(2)一种新研发出的铁磁性材料M的分子结构如图1所示。
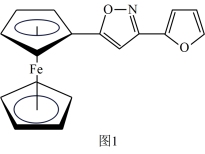
①M分子中C、N、O三种元素的电负性由大到小的顺序为_______ 。
②M分子中的Fe2+与上下两个五元碳环通过配位键相连且Fe2+共提供了6个杂化轨道,则铁原子最可能的杂化方式为_______ (填序号)。
A. sp2 B. sp3 C. dsp2 D.d2sp3
③分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ), 则M分子中由碳、氧组成的五元环中的大π键应表示为
), 则M分子中由碳、氧组成的五元环中的大π键应表示为_______ 。
(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如图2所示。

①若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为_______ 。
②该化合物的化学式为_______ ,若晶胞中距离最近的铁原子和氮原子的距离为apm,阿伏加德罗常数的值为NA,则该晶胞的密度为_______ g·cm-3 (列出计算式即可)。
(1)基态铁原子的价电子排布图为
(2)一种新研发出的铁磁性材料M的分子结构如图1所示。

①M分子中C、N、O三种元素的电负性由大到小的顺序为
②M分子中的Fe2+与上下两个五元碳环通过配位键相连且Fe2+共提供了6个杂化轨道,则铁原子最可能的杂化方式为
A. sp2 B. sp3 C. dsp2 D.d2sp3
③分子中的大π键可用符号π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ), 则M分子中由碳、氧组成的五元环中的大π键应表示为
), 则M分子中由碳、氧组成的五元环中的大π键应表示为(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如图2所示。

①若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为
②该化合物的化学式为
您最近一年使用:0次
2022-05-31更新
|
934次组卷
|
5卷引用:内蒙古自治区赤峰市2022届高三下学期4月模拟考试理综合化学试题
内蒙古自治区赤峰市2022届高三下学期4月模拟考试理综合化学试题(已下线)易错点13 原子结构与核外电子排布-备战2023年高考化学考试易错题(已下线)第十二章 物质结构与性质(测)-2023年高考化学一轮复习讲练测(全国通用)河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题湖北省武汉市武钢三中2023-2024学年高二下学期3月月考化学试题
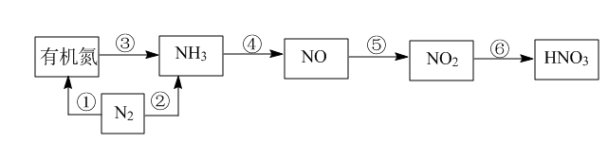
3 . 硝酸是用途广泛的重要化工原料,自然界和化工生产中合成硝酸各物质转化关系如下图所示,请结合你所学的知识回答以下问题:
(1) 在自然界中能稳定存在的原因是
在自然界中能稳定存在的原因是___________ ;
(2)上图①~⑥各步转化中,属于氮的固定的是___________ (填序号);
(3)氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比___________ ;
(4)为提高NO→ 的转化率,可采取的措施是
的转化率,可采取的措施是___________ ;
(5)工业制硝酸时含有NO、 等大气污染物。用尿素[
等大气污染物。用尿素[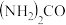 ]水溶液吸收氮氧化物是一种可行的方法。NO和
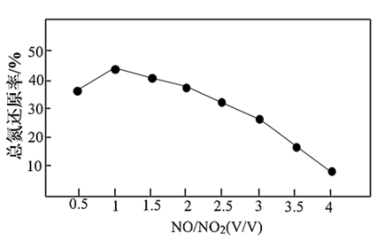
]水溶液吸收氮氧化物是一种可行的方法。NO和 不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
①用尿素[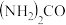 ]水溶液吸收体积比为1:1的NO和
]水溶液吸收体积比为1:1的NO和 混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式
混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式___________ ;
②随着NO和 配比的提高,总氮还原率降低的主要原因是
配比的提高,总氮还原率降低的主要原因是___________ 。

(1)
 在自然界中能稳定存在的原因是
在自然界中能稳定存在的原因是(2)上图①~⑥各步转化中,属于氮的固定的是
(3)氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比
(4)为提高NO→
 的转化率,可采取的措施是
的转化率,可采取的措施是(5)工业制硝酸时含有NO、
 等大气污染物。用尿素[
等大气污染物。用尿素[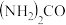 ]水溶液吸收氮氧化物是一种可行的方法。NO和
]水溶液吸收氮氧化物是一种可行的方法。NO和 不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
①用尿素[
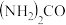 ]水溶液吸收体积比为1:1的NO和
]水溶液吸收体积比为1:1的NO和 混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式
混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式②随着NO和
 配比的提高,总氮还原率降低的主要原因是
配比的提高,总氮还原率降低的主要原因是
您最近一年使用:0次
名校
解题方法
4 . 二烯烃与溴反应制备多卤代物,反应的区域选择性在有机合成中具有重要意义。1,3–丁二烯(g) (CH2=CH—CH=CH2)和Br2(g)反应原理如下:
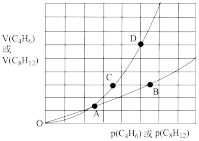
①CH2=CH-CH=CH2(g)+Br2(g)→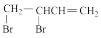 (g) △H1=akJ·mol-1
(g) △H1=akJ·mol-1
②CH2=CH-CH=CH2(g)+Br2(g)→ (g) △H2=bkJ·mol-1
(g) △H2=bkJ·mol-1
③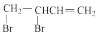 (g)⇌
(g)⇌ 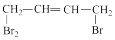 (g) △H3
(g) △H3
回答下列问题:
(1)△H3=_____________ 。
(2)1,3-丁二烯和Br2反应的能量随反应过程的变化关系如图所示:
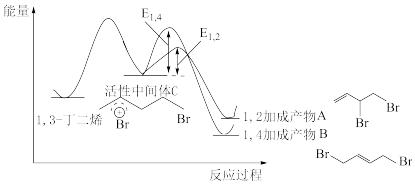
1,3-丁二烯和Br2反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为_________
(3)T℃时在2L刚性密闭容器中充入1,3-丁二烯(g)(CH2=CH-CH=CH2)和Br2(g)各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
在0 ~20min内,反应体系中1,4-加成产物的平均反应速率v(1,4加成产物)=_______ 。
(4)对于反应③,若要提高1,4-加成产物 (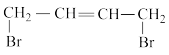 )平衡体系中的物质量分数,可以采取的措施有
)平衡体系中的物质量分数,可以采取的措施有_____
A.适当升高温度 B.使用合适的催化剂
C.增大体系的压强 D.将1,4加成产物及时从体系分离
(5)反应 1,3-丁二烯二聚体的解聚为可逆反应:
 (g)
(g) 2
2 (g) △H>0
(g) △H>0
在一定条件下,C4H6和C8H12的消耗速率与各自分压有如下关系:v(C8H12)=k1·p(C8H12),v(C4H6)=k2·p2(C4H6)。相应的速率与其分压关系如图所示,一定温度下k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=_____ ;在图中标出点(A、B、C、D)中,能表示反应达到平衡状态的点是______ ,理由是________ 。
①CH2=CH-CH=CH2(g)+Br2(g)→
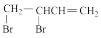 (g) △H1=akJ·mol-1
(g) △H1=akJ·mol-1②CH2=CH-CH=CH2(g)+Br2(g)→
 (g) △H2=bkJ·mol-1
(g) △H2=bkJ·mol-1③
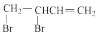 (g)⇌
(g)⇌ 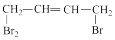 (g) △H3
(g) △H3回答下列问题:
(1)△H3=
(2)1,3-丁二烯和Br2反应的能量随反应过程的变化关系如图所示:

1,3-丁二烯和Br2反应会生成两种产物,一种称为动力学产物,由速率更快的反应生成;一种称为热力学产物,由产物更加稳定的反应生成。则动力学产物结构简式为
(3)T℃时在2L刚性密闭容器中充入1,3-丁二烯(g)(CH2=CH-CH=CH2)和Br2(g)各2mol,发生反应。1,3-丁二烯及产物的物质的量分数随时间的变化如下表:
| 时间(min) | 0 | 10 | 20 | 30 | 40 |
| 1,3-丁二烯 | 100% | 72% | 0% | 0% | 0% |
| 1,2加成产物 | 0% | 26% | 10% | 4% | 4% |
| 1,4加成产物 | 0% | 2% | 90% | 96% | 96% |
在0 ~20min内,反应体系中1,4-加成产物的平均反应速率v(1,4加成产物)=
(4)对于反应③,若要提高1,4-加成产物 (
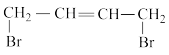 )平衡体系中的物质量分数,可以采取的措施有
)平衡体系中的物质量分数,可以采取的措施有A.适当升高温度 B.使用合适的催化剂
C.增大体系的压强 D.将1,4加成产物及时从体系分离
(5)反应 1,3-丁二烯二聚体的解聚为可逆反应:
 (g)
(g) 2
2 (g) △H>0
(g) △H>0在一定条件下,C4H6和C8H12的消耗速率与各自分压有如下关系:v(C8H12)=k1·p(C8H12),v(C4H6)=k2·p2(C4H6)。相应的速率与其分压关系如图所示,一定温度下k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=

您最近一年使用:0次
2020-06-23更新
|
376次组卷
|
2卷引用:内蒙古包头市2020届高三普通高等学校招生全国统一考试(第二次模拟考试)理科综合化学试题
解题方法
5 . 据报道复旦大学修发贤教授课题组成功制备出砷化铌纳米带,并观测到其表面态具有百倍于金属铜薄膜和千倍于石墨烯的导电性。相关研究论文已在线发表于权威科学期刊《自然》。回答下列问题:
(1)铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d55s1。下列是Nb的不同微粒的核外电子排布式,其中失去最外层1个电子所需能量最小的是___ (填标号)。
a.[Kr]4d35s15p1b.[Kr]4d45s1c.Kr]4d2d.Kr]4d3
(2)砷为第VA族元素,砷可以与某些有机基团形成有机化合物,如(ClCH=CH)2AsCl,其中As原子与2个C原子、1个Cl原子形成的VSEPR模型为____ 。
(3)英国曼彻斯特大学物理学家安德烈·盖姆和康斯坦丁诺沃肖洛夫用微机械剥离法成功从石墨中分离出石墨烯,因此共同获得2010年诺贝尔物理学奖;而石墨烯具有优异的光学、电学、力学特性在材料学、微纳加工、能源、生物医学和药物传递等方面具有重要的应用前景,被认为是一种未来革命性的材料。
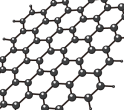
已知“石墨烯”的平面结构如图所示,一定条件下石墨烯与H2发生加成反应生成石墨烷,石墨烷中碳原子杂化类型是___ ,石墨烯导电的原因是____ 。
(4)石墨烯也可采用化学方法进行制备如采用六氯苯、六溴苯作为原料可制备石墨烯。下表给出了六氯苯、六溴苯、苯六酸俗名为蜜石酸的熔点和水溶性:
六溴苯的熔点比六氯苯高的原因是____ ,苯六酸与六溴苯、六氯苯的水溶性存在明显的差异本质原因是___ 。
(5)出于以更高效率利用太阳光等目的研制出金红石型铌氧氮化物(NbON),比以往的光学半导体更能够吸收长波长侧的光,作为光学半导体的新材料。该化合物的晶胞有如图所示的两种构型,若晶胞的边长为apm,该晶体的密度为__ g·cm-3。(NA是阿伏加 德罗常数的值,相关原子量:Nb—93)

(1)铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d55s1。下列是Nb的不同微粒的核外电子排布式,其中失去最外层1个电子所需能量最小的是
a.[Kr]4d35s15p1b.[Kr]4d45s1c.Kr]4d2d.Kr]4d3
(2)砷为第VA族元素,砷可以与某些有机基团形成有机化合物,如(ClCH=CH)2AsCl,其中As原子与2个C原子、1个Cl原子形成的VSEPR模型为
(3)英国曼彻斯特大学物理学家安德烈·盖姆和康斯坦丁诺沃肖洛夫用微机械剥离法成功从石墨中分离出石墨烯,因此共同获得2010年诺贝尔物理学奖;而石墨烯具有优异的光学、电学、力学特性在材料学、微纳加工、能源、生物医学和药物传递等方面具有重要的应用前景,被认为是一种未来革命性的材料。
已知“石墨烯”的平面结构如图所示,一定条件下石墨烯与H2发生加成反应生成石墨烷,石墨烷中碳原子杂化类型是

(4)石墨烯也可采用化学方法进行制备如采用六氯苯、六溴苯作为原料可制备石墨烯。下表给出了六氯苯、六溴苯、苯六酸俗名为蜜石酸的熔点和水溶性:
| 物质 | 六氯苯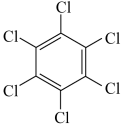 | 六溴苯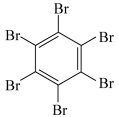 | 苯六酸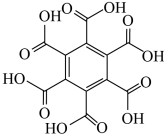 |
| 熔点/℃ | 231 | 325 | 287 |
| 水溶性 | 不溶 | 不溶 | 易溶 |
六溴苯的熔点比六氯苯高的原因是
(5)出于以更高效率利用太阳光等目的研制出金红石型铌氧氮化物(NbON),比以往的光学半导体更能够吸收长波长侧的光,作为光学半导体的新材料。该化合物的晶胞有如图所示的两种构型,若晶胞的边长为apm,该晶体的密度为

您最近一年使用:0次
解题方法
6 . 某反应中反应物与生成物FeCl2、FeCl3、CuCl2、Cu;
(1)将上述反应设计成的原电池如图甲所示请回答下列问题:
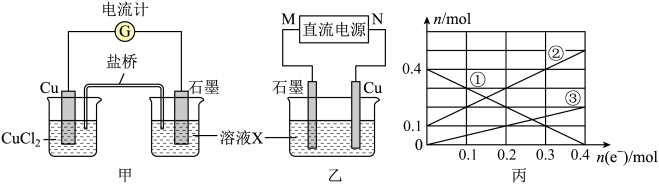
①图中X溶液是__ ;
②Cu电极上发生的电极反应式为__ ;
③原电池工作时,盐桥中的__ 填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成电解池如图乙所示乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是电源的__ 极;
②图丙中的②线是__ 的变化;
③当电子转移为0.2mol时向乙烧杯中加入__ L5mol/LNaOH溶液才能使所有的金属阳离子沉淀完全。
(1)将上述反应设计成的原电池如图甲所示请回答下列问题:

①图中X溶液是
②Cu电极上发生的电极反应式为
③原电池工作时,盐桥中的
(2)将上述反应设计成电解池如图乙所示乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是电源的
②图丙中的②线是
③当电子转移为0.2mol时向乙烧杯中加入
您最近一年使用:0次
2013·全国·一模
7 . 甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
(1)反应②是_______ (填“吸热”或“放热”)反应。
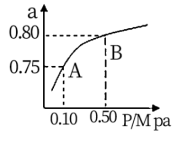
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______ (用K1、K2表示)。
(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______ 。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_______ 。
(4)甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼 雷电池,其原理如图所示。该电池的负极反应式是_______

(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为_______ 。
| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)⇌CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)⇌ H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)⇌CH3OH(g)+H2O (g) | K3 | ||
(1)反应②是
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3=

(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是
(4)甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼 雷电池,其原理如图所示。该电池的负极反应式是

(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为
您最近一年使用:0次
名校
8 . A、B、C、D、E、F为前四周期原子序数依次增大的六种元素,A、C、D原子均有两个未成对电子,A、B、C同周期,A与D、B与F分别同主族,E是生活中用量最大的金属。请回答下列问题:
(1)E比较稳定的离子核外电子排布式_____________________________ .
(2)A、B、C的第一电离能由小到大的顺序为_________________  用元素符号表示
用元素符号表示 、B、C的简单氢化物中最易汽化的物质的化学式
、B、C的简单氢化物中最易汽化的物质的化学式___________ .
(3)C与D形成的物质的晶体类型是____________ ,IT产业中该晶体用于生产____________ .
(4)由A、B、C三种元素中的一种或两种元素形成的分子中,有的互为等电子体,写出其中一组等电子体的化学式:______  并写出对应的结构式
并写出对应的结构式_______________ .
(5)B的单质晶胞与 的相似,则一个晶胞中含B的原子个数为
的相似,则一个晶胞中含B的原子个数为____  与氢形成的分子空间构型是
与氢形成的分子空间构型是_______ .
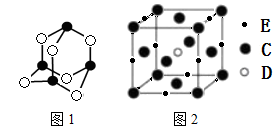
(6)“砒霜”是一种含C,F的化合物,其分子结构如图1所示,该化合物的分子式为F4C6,F原子采取______ 杂化;C,D,E组成的化合物的晶胞如图2,其晶胞参数为a pm,则其密度为___________________ g/cm3(列出式子即可,阿伏伽德罗常数为NAmol-1)。
(1)E比较稳定的离子核外电子排布式
(2)A、B、C的第一电离能由小到大的顺序为
 用元素符号表示
用元素符号表示 、B、C的简单氢化物中最易汽化的物质的化学式
、B、C的简单氢化物中最易汽化的物质的化学式(3)C与D形成的物质的晶体类型是
(4)由A、B、C三种元素中的一种或两种元素形成的分子中,有的互为等电子体,写出其中一组等电子体的化学式:
 并写出对应的结构式
并写出对应的结构式(5)B的单质晶胞与
 的相似,则一个晶胞中含B的原子个数为
的相似,则一个晶胞中含B的原子个数为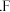 与氢形成的分子空间构型是
与氢形成的分子空间构型是(6)“砒霜”是一种含C,F的化合物,其分子结构如图1所示,该化合物的分子式为F4C6,F原子采取

您最近一年使用:0次
名校
解题方法
9 . 水钴矿中除SiO2外,还有9.24% CoO、2.78% Fe2O3、0.96% MgO、0.084%CaO。
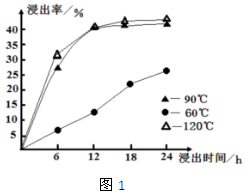
(1)在一定浓度的 溶液中,钴的浸出率随时间、温度的变化如图1所示
溶液中,钴的浸出率随时间、温度的变化如图1所示 考虑生产成本和效率,最佳的浸出时间为
考虑生产成本和效率,最佳的浸出时间为______ 小时,最佳的浸出温度为______ 
(2)请配平下列除铁的化学方程式:____________
_ _Fe2(SO4)3+ H2O + Na2CO3 == Na2Fe6(SO4)4(OH)12↓+ Na2SO4 + CO2↑
(3) “除钙、镁”的原理反应为: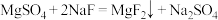 ;
; 已知
已知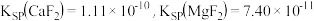 ,加入过量NaF溶液反应完全后过滤,则滤液中
,加入过量NaF溶液反应完全后过滤,则滤液中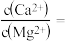
____________________ .
(4) “沉淀”中含杂质离子主要有 、
、 、
、_________ 和__________ ;“操作X”包括_________ 和_________ 。
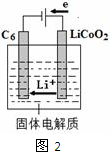
(5)某锂离子电池正极是 ,含
,含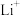 导电固体为电解质
导电固体为电解质 充电时,
充电时,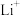 还原为Li,并以原子形式嵌入电池负极材料碳
还原为Li,并以原子形式嵌入电池负极材料碳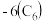 中
中 如图2所示
如图2所示 电池反应为
电池反应为
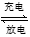
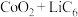 ,写出该电池放电时的正极反应式
,写出该电池放电时的正极反应式 ________________________________________ .



(1)在一定浓度的
 溶液中,钴的浸出率随时间、温度的变化如图1所示
溶液中,钴的浸出率随时间、温度的变化如图1所示 考虑生产成本和效率,最佳的浸出时间为
考虑生产成本和效率,最佳的浸出时间为
(2)请配平下列除铁的化学方程式:
_ _Fe2(SO4)3+ H2O + Na2CO3 == Na2Fe6(SO4)4(OH)12↓+ Na2SO4 + CO2↑
(3) “除钙、镁”的原理反应为:
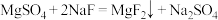 ;
; 已知
已知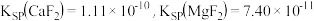 ,加入过量NaF溶液反应完全后过滤,则滤液中
,加入过量NaF溶液反应完全后过滤,则滤液中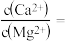
(4) “沉淀”中含杂质离子主要有
 、
、 、
、(5)某锂离子电池正极是
 ,含
,含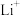 导电固体为电解质
导电固体为电解质 充电时,
充电时,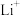 还原为Li,并以原子形式嵌入电池负极材料碳
还原为Li,并以原子形式嵌入电池负极材料碳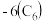 中
中 如图2所示
如图2所示 电池反应为
电池反应为
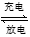
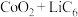 ,写出该电池放电时的正极反应式
,写出该电池放电时的正极反应式
您最近一年使用:0次
10 . 碳及其化合物在有机合成、能源开发等工农业方面具有十分广泛的应用。
I.工业生产精细化工产品乙二醛(OHC-CHO)
(1)乙醇(CH3CH2OH)液相硝酸氧化法:在Cu(NO3)2催化下,用稀硝酸氧化乙醇制取乙二醛,此反应的化学方程式为_______________ 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点____________ 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
已知:2H2(g)+O2(g) 2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
OHC-CHO(g)+2H2(g) HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
则乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC-CHO(g)+2H2O(g)的ΔH=
OHC-CHO(g)+2H2O(g)的ΔH=______ ;相同温度下,该反应的化学平衡常数K=______ (用含K1、K2的代数式表示)。
Ⅱ.CO2的综合利用
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生反应C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是______ (填字母)。
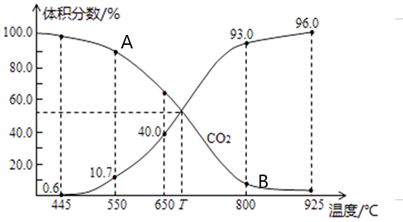
a.反应达平衡状态时,混合气体的平均相对分子质量保持不变
b.A点的正反应速率比B点正反应速率小
C.550℃时,若充入氦气,则V正、V逆均减小,平衡不移动
d.T℃时,反应达平衡后CO2的转化率为66.7%
e. T℃时,若再充入1molCO2和1molCO,平衡不移动
(4)氨气、CO2在一定条件下可合成尿素,其反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
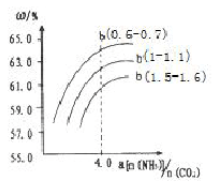
①b应控制在______
a.1.5-1.6 b.1-1.1 c.0.6-0.7
②a应控制在4.0的理由是_________
I.工业生产精细化工产品乙二醛(OHC-CHO)
(1)乙醇(CH3CH2OH)液相硝酸氧化法:在Cu(NO3)2催化下,用稀硝酸氧化乙醇制取乙二醛,此反应的化学方程式为
(2)乙二醇(HOCH2CH2OH)气相氧化法
已知:2H2(g)+O2(g)
 2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1
2H2O(g) ΔH=-484kJ/mol,化学平衡常数为K1OHC-CHO(g)+2H2(g)
 HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2
HOCH2CH2OH(g) ΔH=-78kJ/mol,化学平衡常数为K2则乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g)
 OHC-CHO(g)+2H2O(g)的ΔH=
OHC-CHO(g)+2H2O(g)的ΔH=Ⅱ.CO2的综合利用
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生反应C(s)+CO2(g)
 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示,则下列说法正确的是
a.反应达平衡状态时,混合气体的平均相对分子质量保持不变
b.A点的正反应速率比B点正反应速率小
C.550℃时,若充入氦气,则V正、V逆均减小,平衡不移动
d.T℃时,反应达平衡后CO2的转化率为66.7%
e. T℃时,若再充入1molCO2和1molCO,平衡不移动
(4)氨气、CO2在一定条件下可合成尿素,其反应为2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
CO(NH2)2(s)+H2O(g),右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为{n(NH3)/n(CO2)},b为水碳比{n(H2O)/n(CO2)}。则
①b应控制在
a.1.5-1.6 b.1-1.1 c.0.6-0.7
②a应控制在4.0的理由是
您最近一年使用:0次
2018-05-01更新
|
524次组卷
|
3卷引用:【全国市级联考】内蒙古呼和浩特市2018届高三第二次模拟考试理科综合化学试题
【全国市级联考】内蒙古呼和浩特市2018届高三第二次模拟考试理科综合化学试题四川省泸县第四中学2020届高三下学期第四次学月考试理综化学试题(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(精练)-2022年高考化学一轮复习讲练测



