名校
1 . 氮的化合物种类繁多,性质也各不相同。请回答下列问题:
(1)已知:
①SO3(g)+NO(g)=NO2(g)+SO2(g) ∆H1=+41.8kJ·mol-1
②2SO2(g)+O2(g)=2SO3(g) ∆H2=-196.6kJ·mol-1
则2NO2(g)=2NO(g)+O2(g)的∆H=_______ 。
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
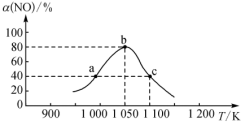
图中a、b、c三点中,达到平衡的点是_______ ;温度为1100K时,N2的平衡体积分数为_______ 。
(3)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g) ∆H<0。
3H2O(g)+2N2(g) ∆H<0。
①实际生产中NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g)的反应温度不宜过高的原因是
3H2O(g)+2N2(g)的反应温度不宜过高的原因是_______ 。
②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,8min时反应达到平衡,此时NH3的转化率为40%,体系压强为p0MPa,则0~8min内用N2表示的平均反应速率v(N2)=_______ mol·L-1·min-1,500℃时该反应的平衡常数Kp=_______ MPa(用含p0的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)已知:
①SO3(g)+NO(g)=NO2(g)+SO2(g) ∆H1=+41.8kJ·mol-1
②2SO2(g)+O2(g)=2SO3(g) ∆H2=-196.6kJ·mol-1
则2NO2(g)=2NO(g)+O2(g)的∆H=
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)⇌N2(g)+CO2(g) ∆H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:

图中a、b、c三点中,达到平衡的点是
(3)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g) ∆H<0。
3H2O(g)+2N2(g) ∆H<0。①实际生产中NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g)的反应温度不宜过高的原因是
3H2O(g)+2N2(g)的反应温度不宜过高的原因是②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,8min时反应达到平衡,此时NH3的转化率为40%,体系压强为p0MPa,则0~8min内用N2表示的平均反应速率v(N2)=
您最近一年使用:0次
2021-07-13更新
|
3548次组卷
|
8卷引用:青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题
名校
2 . 回答下列问题:
(1)已知室温下CO的燃烧热为283 kJ/mol,则CO的燃烧热的热化学方程式为___________________________________ 。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为:CO(g)+2H2(g) CH3OH(g) ΔH=-116kJ/mol
CH3OH(g) ΔH=-116kJ/mol
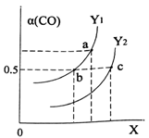
如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是_____________ ,Y1_____ Y2(填“<”、“=”、“>”)。
(3)合成甲醇的反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在1L的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),在1L的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
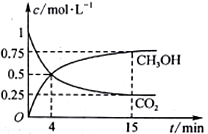
①反应进行到4min时,v(正)____ v(逆)(填“>”“<”或“=”)。0~4min,CO2的平均反应速率v(CO2)=____________ mol·L−1·min−1。
②该温度下平衡常数为_____________ 。
③下列能说明该反应已达到平衡状态的是______________ 。
A.v正(CH3OH)=3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1∶3∶1∶1
C.恒温恒压下,气体的体积不再变化
D.恒温恒容下,气体的密度不再变化
(4)为提高燃料的能量利用率,常将其设计为燃料电池。某电池以甲烷为燃料,空气为氧化剂,KOH溶液为电解质溶液,以具有催化作用和导电性能的稀土金属为电极。写出该燃料电池的负极反应式:_____________________________ 。
(1)已知室温下CO的燃烧热为283 kJ/mol,则CO的燃烧热的热化学方程式为
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为:CO(g)+2H2(g)
 CH3OH(g) ΔH=-116kJ/mol
CH3OH(g) ΔH=-116kJ/mol如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是

(3)合成甲醇的反应原理为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),在1L的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),在1L的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
①反应进行到4min时,v(正)
②该温度下平衡常数为
③下列能说明该反应已达到平衡状态的是
A.v正(CH3OH)=3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1∶3∶1∶1
C.恒温恒压下,气体的体积不再变化
D.恒温恒容下,气体的密度不再变化
(4)为提高燃料的能量利用率,常将其设计为燃料电池。某电池以甲烷为燃料,空气为氧化剂,KOH溶液为电解质溶液,以具有催化作用和导电性能的稀土金属为电极。写出该燃料电池的负极反应式:
您最近一年使用:0次
2018-12-29更新
|
1246次组卷
|
4卷引用:【全国百强校】青海省西宁市第四高级中学2019届高三上学期第四次模拟考试理科综合化学试题
【全国百强校】青海省西宁市第四高级中学2019届高三上学期第四次模拟考试理科综合化学试题【市级联考】陕西省榆林市2019届高三下学期模拟考试化学试题(已下线)【南昌新东方】2019 南大附中 高二上 期中甘肃省静宁县第一中学2021届高三上学期第四次模拟考试化学试题
名校
解题方法
3 . 根据题意完成下列问题:
(1)做实验时皮肤上不小心粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为: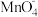 +
+ 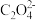 + H+ → CO2↑+ Mn2+ +
+ H+ → CO2↑+ Mn2+ + 
①该反应的氧化剂是_____ 右边方框内的产物是_____
②完成并配平该离子方程式__________________ 电子转移总数是_____ e-
(2)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。单质A能与某气态单质化合生成化合物B。
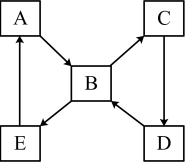
若化合物B是造成酸雨的主要污染物,化合物D是组成单质A元素的最高价氧化物对应水化物,则单质A是_________ (物质名称),将化合物B通入溴水中观察到的现象是_________ ,该现象说明化合物B具有_______ 性。
(1)做实验时皮肤上不小心粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:
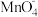 +
+ 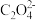 + H+ → CO2↑+ Mn2+ +
+ H+ → CO2↑+ Mn2+ + 
①该反应的氧化剂是
②完成并配平该离子方程式
(2)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。单质A能与某气态单质化合生成化合物B。

若化合物B是造成酸雨的主要污染物,化合物D是组成单质A元素的最高价氧化物对应水化物,则单质A是
您最近一年使用:0次
4 . 由Mg、P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,请回答下列问题。
(1)基态Mg原子L层电子排布式为_____ ,P、S、Cl的第一电离能由大到小顺序为_______ 。
(2)PH4Cl的电子式为_________ ,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为__________ 。
(3)SCl2分子中的中心原子杂化轨道类型是_______ ,该分子构型为_________ 。
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69 pm。则熔点:MgO_____ NiO(填“>”、“<”或“=”),理由是_____________ 。
(5)如图1所示,NiO晶胞中离子坐标参数A为(0,0,0),B为(1,0,1),则C离子坐标参数为___________ 。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______ g。(用a、NA表示)
(1)基态Mg原子L层电子排布式为
(2)PH4Cl的电子式为
(3)SCl2分子中的中心原子杂化轨道类型是
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69 pm。则熔点:MgO
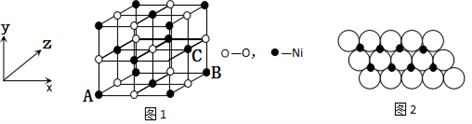
(5)如图1所示,NiO晶胞中离子坐标参数A为(0,0,0),B为(1,0,1),则C离子坐标参数为
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为
您最近一年使用:0次
2017-04-06更新
|
425次组卷
|
2卷引用:青海省西宁市2017届高三下学期复习检测二(二模)理综化学试题
5 . 砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
I.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) 2AsS33-(aq);
2AsS33-(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为________ ;砷酸的第一步电离方程式为_____________ 。
(2)“一级沉砷”中FeSO4的作用是___________ ;“二级沉砷”中H2O2与含砷物质反应的化学方程式为_____________ 。
(3)沉淀X为___________ (填化学式)。
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的 最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
(4)AsH3的电子式为_______________ 。
(5)步骤2的离子方程式为_________________ 。
(6)固体废弃物的排放标准中,砷元素不得高于4.0×10-5g·kg-1,请通过计算说明该排放的废渣中砷元素的含量_______ (填“符合”、“不符合”)排放标准,原因是__________
I.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq)
 2AsS33-(aq);
2AsS33-(aq);②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为
(2)“一级沉砷”中FeSO4的作用是
(3)沉淀X为
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的 最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
(4)AsH3的电子式为
(5)步骤2的离子方程式为
(6)固体废弃物的排放标准中,砷元素不得高于4.0×10-5g·kg-1,请通过计算说明该排放的废渣中砷元素的含量
您最近一年使用:0次
2017-03-15更新
|
681次组卷
|
6卷引用:青海省西宁市2017届高三下学期复习检测二(二模)理综化学试题
青海省西宁市2017届高三下学期复习检测二(二模)理综化学试题2017届广东省肇庆市高三上学期二模化学试卷2017届山东省泰安市高三第一轮复习质量检测(一模)理科综合化学试卷广东省汕头市2017届高三普通高考第二次模拟考试化学试题(已下线)《考前20天终极攻略》6月3日 专项三 化学计算(已下线)微专题34 非金属及其化合物制备流程与实验探究(Si、N、P、As)-备战2022年高考化学考点微专题
6 . 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式______ ,它位于周期表______ 区。
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为_______ ;1 mol C60分子中σ键的数目为_____ 个。

(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As____ Ga(填“>”、“<”或“=”)。
②SeO2分子的空间构型为________ 。
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应的化学方程式为3F2+4 NH3 Cu NF3+3 NH4F,该反应中NH3的沸点_____ (填“>”、“<”或“=”)HF的沸点,NH4F固体属于________ 晶体。往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是___________________________ 。图乙为一个金属铜的晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为

(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As
②SeO2分子的空间构型为
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应的化学方程式为3F2+4 NH3 Cu NF3+3 NH4F,该反应中NH3的沸点

您最近一年使用:0次
2016-12-09更新
|
126次组卷
|
2卷引用:2016届青海省平安一中高三下高考冲刺一理综化学试卷
2014高三·全国·专题练习
7 . 1.按要求填空
1.(1)火山喷发所产生的硫磺可用于生产重要的化工原料硫酸。某企业用下图所示的工艺流程生产硫酸:
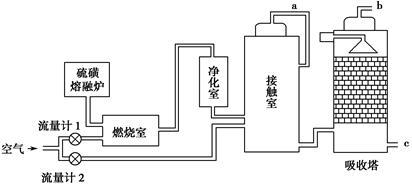
①为充分利用反应放出的热量,接触室中应安装______ (填设备名称)。吸收塔中填充有许多瓷管,其作用是______ 。
②为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为______ 。假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为______ (空气中氧气的体积分数按0.2计),该尾气的处理方法是______ 。
③与以黄铁矿为原料的生产工艺相比,该工艺的特点是______ (可多选)。
A. 耗氧量减少
B. 二氧化硫的转化率提高
C. 生产的废渣减少
D. 不需要使用催化剂
(1)硫酸的用途非常广泛,可应用于下列哪些方面______(可多选)。
(2)矿物燃料的燃烧是产生大气中SO2的主要原因之一、在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式______ 。
1.(1)火山喷发所产生的硫磺可用于生产重要的化工原料硫酸。某企业用下图所示的工艺流程生产硫酸:

①为充分利用反应放出的热量,接触室中应安装
②为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为
③与以黄铁矿为原料的生产工艺相比,该工艺的特点是
A. 耗氧量减少
B. 二氧化硫的转化率提高
C. 生产的废渣减少
D. 不需要使用催化剂
(1)硫酸的用途非常广泛,可应用于下列哪些方面______(可多选)。
| A.橡胶的硫化 |
| B.表面活性剂“烷基苯磺酸钠”的合成 |
| C.铅蓄电池的生产 |
| D.过磷酸钙的制备 |
您最近一年使用:0次
2016-12-09更新
|
1161次组卷
|
13卷引用:2013-2014青海西宁五中片区大联考高三5月高考模拟理综化学试卷
(已下线)2013-2014青海西宁五中片区大联考高三5月高考模拟理综化学试卷2013-2014河北衡水中学第二学期高三第一次模拟化学试卷2016届重庆市巴蜀中学高三三诊理综化学试卷(已下线)2014高考化学二轮复习限时集训 专题15化学与技术练习卷(已下线)2014年高二化学人教版选修二 1单元综合检测练习卷2015届宁夏银川九中高三上学期期中化学试卷2015届江西省重点中学协作体高三下学期联考理科综合化学试卷2015届江西省上饶市六校重点中学高三上学期第一次联考化学试卷2015届江西省高三九校3月联考理综化学试卷2015届辽宁省丹东市高三总复习质量测试(一)理综化学试卷2016届辽宁省五校协作体高三上学期期初考试化学试卷2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷2015-2016学年辽宁庄河高中高二下期末化学试卷
8 . 分析下列水处理方法,完成下列问题:
(1)处理含Cr2O72-工业废水的工艺:
①工艺一:含Cr2O72-的工业废水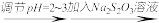 Cr3+、SO42-
Cr3+、SO42- 。
。
为了进一步除去上述流程中生成的Cr3+,请你设计一个处理方案:________________ 。
②工艺二:向废水中加入过量的FeSO4溶液,经过一系列反应后,FeSO4溶液和Cr2O72-可形成铁氧体沉淀,从而除去铬元素。若使含1mol Cr2O72-的废水中的Cr2O72-完全转化为一种化学式为Cr0.5Fe2.5O4的铁氧体(其中的铬元素为+3价),理论上需要绿矾(FeSO4·7H2O)的质量不少于______ g,上述得到的铁氧体中,Fe3+和Fe2+的个数之比_____ 。
(2)如下是处理含氰(主要以CN—形式存在)废水工艺流程的一部分:含氰废水
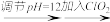 。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为—1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为
。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为—1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为__________ kg(结果保留两位有效数字)。
(3)监测水中氯化物含量可采用硝酸汞滴定法,酸化的水样用硝酸汞滴定时可生成难电离的氯化汞,滴定到终点时过量的汞离子可与指示剂作用使溶液显示紫色。饮用水中的其他物质在通常浓度下对滴定不产生干扰,但水的色质、高价铁、六价铬、硫化物(如S2-)对实验有干扰。
①滴定前常用氢氧化铝悬浊液处理水样,其目的是__________________ 。
②若水中含有Cr2O72—,常在滴定前向水样中加入一定量的对苯二酚,其目的是______ 。
(1)处理含Cr2O72-工业废水的工艺:
①工艺一:含Cr2O72-的工业废水
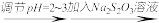 Cr3+、SO42-
Cr3+、SO42- 。
。为了进一步除去上述流程中生成的Cr3+,请你设计一个处理方案:
②工艺二:向废水中加入过量的FeSO4溶液,经过一系列反应后,FeSO4溶液和Cr2O72-可形成铁氧体沉淀,从而除去铬元素。若使含1mol Cr2O72-的废水中的Cr2O72-完全转化为一种化学式为Cr0.5Fe2.5O4的铁氧体(其中的铬元素为+3价),理论上需要绿矾(FeSO4·7H2O)的质量不少于
(2)如下是处理含氰(主要以CN—形式存在)废水工艺流程的一部分:含氰废水
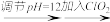 。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为—1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为
。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为—1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为(3)监测水中氯化物含量可采用硝酸汞滴定法,酸化的水样用硝酸汞滴定时可生成难电离的氯化汞,滴定到终点时过量的汞离子可与指示剂作用使溶液显示紫色。饮用水中的其他物质在通常浓度下对滴定不产生干扰,但水的色质、高价铁、六价铬、硫化物(如S2-)对实验有干扰。
①滴定前常用氢氧化铝悬浊液处理水样,其目的是
②若水中含有Cr2O72—,常在滴定前向水样中加入一定量的对苯二酚,其目的是
您最近一年使用:0次
2016-12-09更新
|
131次组卷
|
2卷引用:2016届青海省平安一中高三下高考冲刺一理综化学试卷
9 . 在一个容积不变的密闭容器中,发生反应:2NO(g)+O2(g) 2NO2(g)
2NO2(g)
(1)当n(NO):n(O2)=4:1时,O2的转化率随时间的变化关系如下图所示。
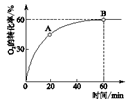
①A点的逆反应速率v逆(O2)_____ B点的正反应速率v正(O2)(填“大于”、“小于”或“等于” )。
②NO的平衡转化率为______ ;当达到B点后往容器中再以4:1 加入些NO和 O2,当达到新平衡时,则NO的百分含量_______ B点NO的百分含量(填“大于”、“小于”或“等于” )。
③到达B点后,下列关系正确的是( )
(2)在下图1和图2中出现的所有物质都为气体,分析图1和图2,可推测:4NO(g)+3O2(g)=2N2O5(g) △H=_________ 。


(3)降低温度,NO2(g)将转化为N2O4(g),以N2O4、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨I电极反应生成一种氧化物Y,Y为______ ,有关石墨I电极反应式可表示为:___________________ 。
 2NO2(g)
2NO2(g)(1)当n(NO):n(O2)=4:1时,O2的转化率随时间的变化关系如下图所示。

①A点的逆反应速率v逆(O2)
②NO的平衡转化率为
③到达B点后,下列关系正确的是
| A.容器内气体颜色不再变化 | B.v正(NO)=2 v正(O2) |
| C.气体平均摩尔质量在此条件下达到最大 | D.容器内气体密度不再变化 |
(2)在下图1和图2中出现的所有物质都为气体,分析图1和图2,可推测:4NO(g)+3O2(g)=2N2O5(g) △H=


(3)降低温度,NO2(g)将转化为N2O4(g),以N2O4、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨I电极反应生成一种氧化物Y,Y为
您最近一年使用:0次
2016-12-09更新
|
214次组卷
|
3卷引用:2016届青海省平安一中高三下高考冲刺一理综化学试卷
10 . 钡盐生产过程中排出大量钡泥[主要含有BaCO3、BaSO3、Ba(FeO2)2等],某工厂本着资源利用和降低生产成本的目的。在生产BaCO3同时,充分利用钡泥来制取Ba(NO3)2晶体及其它副产品,其部分工艺流程如下:

已知: ①Fe(OH)3和Fe(OH)2完全沉淀时溶液的pH分别为3.2和9.7
②Ba(NO3)2在热水中的溶解度大,在冷水中的溶解度小
③Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=5.1×10-9
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量饱和的Na2CO3溶液中充分搅拌、过滤、洗涤。用离子方程式说明该提纯的原理___________________________ 。
(2)上述流程中Ba(FeO2)2与HNO3溶液反应生成两种盐,反应的化学方程式为________________ 。
(3)结合本厂生产实际,X试剂应选下列中的_____________ 。
(4)废渣2为_____________ 。
(5)操作III为_____________ 。
(6)过滤III后的母液应循环到容器_______ 中(选填a、b、c) 。
(7)称取w克的晶体样品溶于蒸馏水中加入足量的稀硫酸,反应后经一系列操作称重所得沉淀质量为m克,则该晶体的纯度可表示为______________ 。

已知: ①Fe(OH)3和Fe(OH)2完全沉淀时溶液的pH分别为3.2和9.7
②Ba(NO3)2在热水中的溶解度大,在冷水中的溶解度小
③Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=5.1×10-9
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量饱和的Na2CO3溶液中充分搅拌、过滤、洗涤。用离子方程式说明该提纯的原理
(2)上述流程中Ba(FeO2)2与HNO3溶液反应生成两种盐,反应的化学方程式为
(3)结合本厂生产实际,X试剂应选下列中的
| A.BaCl2 | B.BaCO3 | C.Ba(NO3)2 | D.Ba(OH)2 |
(4)废渣2为
(5)操作III为
(6)过滤III后的母液应循环到容器
(7)称取w克的晶体样品溶于蒸馏水中加入足量的稀硫酸,反应后经一系列操作称重所得沉淀质量为m克,则该晶体的纯度可表示为
您最近一年使用:0次
2016-12-09更新
|
110次组卷
|
3卷引用:2016届青海省平安一中高三下高考冲刺一理综化学试卷



