名校
1 . 研究有机物的结构和性质对生产生活意义深远。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。___________ ,B物质的分子式为:___________ 。
(2)按官能团分类,D所属的类别是___________ 。
(3)1molE与足量的金属钠反应产生___________ L氢气(标况下)。
(4)实验室制取C的化学方程式___________ 。
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。___________ (填名称)。
(6)脱氢维生素C中,键角①___________ 键角②(填“>”、“=”或“<”)。
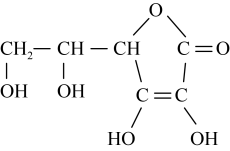
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是___________ 。
(8)标出维生素C中所有的手性碳原子(用*标注)___________ 。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。A. 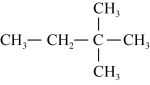 B.
B. 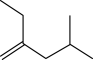 C.
C. D.
D. 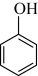 E.
E.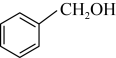
(2)按官能团分类,D所属的类别是
(3)1molE与足量的金属钠反应产生
(4)实验室制取C的化学方程式
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。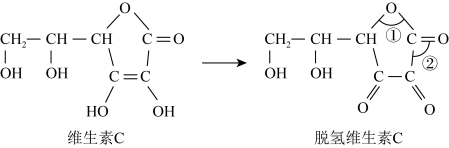
(6)脱氢维生素C中,键角①
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是
(8)标出维生素C中所有的手性碳原子(用*标注)
您最近一年使用:0次
名校
解题方法
2 . 硫、硒、碲的化合物在农药、石油工业、矿物开采、萃取及有机合成等领域的应用广泛。回答下列问题:
(1)基态Se原子的价层电子排布式为___________ 。
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
(3)类卤素 分子结构式为
分子结构式为___________ ,1mol 中含有π键的数目为
中含有π键的数目为___________ ,HSCN结构有两种,已知硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是___________ 。
(4)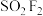 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
___________  (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是___________ 。
(1)基态Se原子的价层电子排布式为
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
A.氧族元素气态氢化物的稳定性按 、 、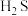 、 、 、 、 的顺序依次减弱 的顺序依次减弱 |
| B.其氢化物中的键长按O―H、S―H、Se―H、Te―H的顺序依次减小 |
C.其阴离子的还原性按 、 、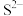 、 、 、 、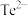 的顺序依次增强 的顺序依次增强 |
D.其最高价氧化物的水化物酸性按 、 、 、 、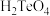 顺序依次增强 顺序依次增强 |
(3)类卤素
 分子结构式为
分子结构式为 中含有π键的数目为
中含有π键的数目为 )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是(4)
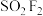 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是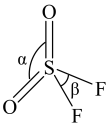

 (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是
您最近一年使用:0次
3 . 科学家开发了“氧化裂解技术”,将废弃物中的聚苯乙烯(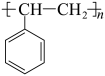 )转变为有用的苯甲酸(
)转变为有用的苯甲酸(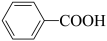 ),变废为宝。转变反应如下:
),变废为宝。转变反应如下: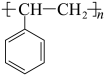
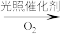
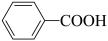 。结合上述材料,回答下列问题:
。结合上述材料,回答下列问题:
| A.属于氧化反应 | B.属于加聚反应 |
| C.发生了碳碳键的断裂 | D.反应物和产物都含有苯分子 |
(2)关于聚苯乙烯的说法正确的是___________。
| A.其单体是乙烯 | B.难溶于水 |
| C.可以制成泡沫包装材料 | D.难以自然降解,应回收处理 |
(3)苯乙烯的一些性质类似于乙烯。苯乙烯___________。
| A.属于烷烃 | B.属于不饱和烃 |
C.不能使溴的 溶液褪色 溶液褪色 | D.能使酸性 溶液褪色 溶液褪色 |
(4)苯甲酸的一些性质类似于乙酸。苯甲酸___________。
| A.可与Na反应 | B.可与NaOH反应 |
| C.一定条件下可与乙醇反应 | D.是一种常见的食品防腐剂 |
(5)一些苯环上有取代基的聚苯乙烯类高分子,也能利用上述的“氧化裂解技术”发生类似的反应。已知一种高分子R的结构如图。下列有关R的说法正确的是___________。
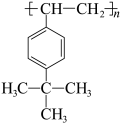
| A.能发生取代反应 | B.能在空气中燃烧 |
C.分子式为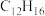 | D.能氧化裂解生成含羧基的物质 |
您最近一年使用:0次
名校
解题方法
4 . 下表是某些短周期元素的电负性(x)值:
(1)根据上表试推测,元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为___________ 。
(2)已知: 。
。
①若 最初水解产物是
最初水解产物是 和HClO,根据
和HClO,根据 的化合价推测
的化合价推测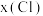 的范围是
的范围是___________ (填表中数值);
② 水解的化学反应方程式是
水解的化学反应方程式是___________ 。
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(2)①进行分析, 属于
属于___________ (填“离子化合物”或“共价化合物”),可设计实验证明,如测定___________ 。
| 元素符号 | Li | Be | N | O | F | Na | Mg | Al | P | S |
| x值 | 1.0 | 1.5 | 3.0 | a | 4.0 | 0.9 | 1.2 | 1.5 | 2.1 | 2.5 |
(2)已知:
 。
。①若
 最初水解产物是
最初水解产物是 和HClO,根据
和HClO,根据 的化合价推测
的化合价推测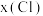 的范围是
的范围是②
 水解的化学反应方程式是
水解的化学反应方程式是(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(2)①进行分析,
 属于
属于
您最近一年使用:0次
5 . “民以食为天”,对元素周期表中有关元素的认识可使我们更好地了解食品的营养和安全。
结合上述材料,回答下列问题:
(1)仅含a、b、d三种元素的营养物质有___________。
(2)成熟水果会释放出由a和b按原子数目比 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。
(3)某些元素的单质或化合物常用于食品加工和保存。下列说法正确的是___________。
(4)土豆中富含淀粉。淀粉___________。
(5)由a、b、d和e四种元素形成的物质可用作糕点膨松剂。下列说法正确的是___________。
| 周期 | ⅠA | 0 | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h |
(1)仅含a、b、d三种元素的营养物质有___________。
| A.脂肪 | B.葡萄糖 | C.蛋白质 | D.氨基酸 |
 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。A.分子式为 | B.呈四面体结构 |
| C.呈三角锥形结构 | D.所有原子共平面 |
| A.a的单质可与植物油发生加成反应 | B.c的单质充入食品包装袋中可防腐 |
| C.f的单质制作的容器可用于贮存酸菜 | D.e和h形成的化合物可用于腌制食品 |
| A.遇碘溶液变色 | B.可水解得到乙醇 |
| C.由a、b、g三种元素组成 | D.水解的最终产物能发生银镜反应 |
| A.非金属性:b>a>d | B.原子半径:e>b>d |
| C.e的最高价氧化物的水化物是强碱 | D.b、d、e原子具有相同的电子层数 |
您最近一年使用:0次
6 . “神舟十五号”载人飞船成功发射,创下了我国在超低温天气成功发射载人飞船的新纪录。肼(N2H4)是火箭常用高能燃料,可与O2发生反应:
N2H4(g)+O2(g)=N2(g)+2H2O(g)。
(1)已知上述反应的能量变化如图所示:___________ (填“吸收”或“放出”)能量。
②N2H4(g)完全燃烧生成1molH2O(g)的反应中放出___________ 能量。
(2)反应N2H4(g)+O2(g)=N2(g)+2H2O(l)可设计为燃料电池,电池中用惰性电极铂(Pt),装置如图所示:___________ (填化学式),该装置工作时, 移向电极
移向电极 ___________ (填“Pt1”或“Pt2”)。
②电极Pt1为___________ (填“负极”或“正极”),发生的电极反应为 ___________ 。
N2H4(g)+O2(g)=N2(g)+2H2O(g)。
(1)已知上述反应的能量变化如图所示:
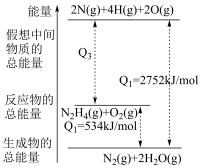
②N2H4(g)完全燃烧生成1molH2O(g)的反应中放出
(2)反应N2H4(g)+O2(g)=N2(g)+2H2O(l)可设计为燃料电池,电池中用惰性电极铂(Pt),装置如图所示:
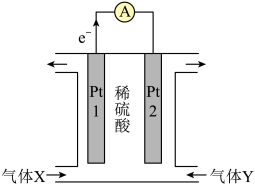
 移向电极
移向电极 ②电极Pt1为
您最近一年使用:0次
解题方法
7 . 按要求回答下列问题:
(1)下列过程中,既属于氧化还原反应,又属于放热反应的是 ___________(填字母)。
(2)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应(反应物、产物均为气体),反应中各物质物质的量的变化如图所示。___________ 。
②在0~6s内,B的平均反应速率为___________ 。
③6s后容器内的压强与开始时压强之比为___________ 。
(3)已知CH3OCH3的结构式为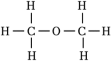 。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是
。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是 ___________ (填字母)。
a.密闭容器中CO的体积分数不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变
d.密闭容器中混合气体的平均相对分子质量不变
e.单位时间内,断裂4molH-H键,同时生成2molH-O键
(1)下列过程中,既属于氧化还原反应,又属于放热反应的是 ___________(填字母)。
| A.甲烷的燃烧 |
| B.CO2通入灼热的炭层 |
| C.石灰石受热分解 |
| D.碘升华 |

②在0~6s内,B的平均反应速率为
③6s后容器内的压强与开始时压强之比为
(3)已知CH3OCH3的结构式为
 。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是
。一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g),下列选项不能作为判断该反应达到平衡状态的依据的是 a.密闭容器中CO的体积分数不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变
d.密闭容器中混合气体的平均相对分子质量不变
e.单位时间内,断裂4molH-H键,同时生成2molH-O键
您最近一年使用:0次
8 . 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序___________ 。
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:___________ 。
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为___________ mL。
(5)某学生根据三次实验分别记录有关数据如表:
请选用其中合理数据求出该氢氧化钠溶液物质的量浓度:c(NaOH)=___________ mol/L。(计算结果保留4位有效数字)
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为

A. | B. | C. | D. |
(5)某学生根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
| A.中和滴定到达终点时俯视滴定管内液面读数 |
| B.碱式滴定管用蒸馏水洗净后立即取用25.00mL待测碱溶液注入锥形瓶进行滴定 |
| C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定 |
| D.锥形瓶用待测液润洗 |
您最近一年使用:0次
名校
9 . I、按要求写出下列方程式:
(1)FeCl3水解的离子方程式:___________ 。
(2)NaHCO3水解的离子方程式:___________ 。
(3)NH3•H2O的电离方程式:___________ 。
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:___________ 。
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=___________ ;由水电离出c(H+)=___________ mol/L。
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH___________ 4(填“大于”“小于”或“等于”)。
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=___________ mol/L
(1)FeCl3水解的离子方程式:
(2)NaHCO3水解的离子方程式:
(3)NH3•H2O的电离方程式:
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.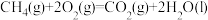
b.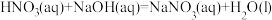
c.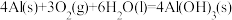
d.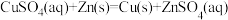
(2)某小组为探究 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。___________ ,B电极的电极反应方程式为___________ 。 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式___________ 。
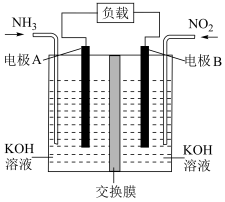
(5)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示: 电极为
电极为___________ (填“正极”或“负极), 电极上发生的电极反应式为
电极上发生的电极反应式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.
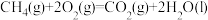
b.
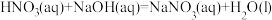
c.
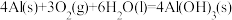
d.
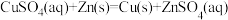
(2)某小组为探究
 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为 向
向
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式(5)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近一年使用:0次



