名校
解题方法
1 . L亚砷酸( )可以用作防腐剂、杀虫剂和除草剂,
)可以用作防腐剂、杀虫剂和除草剂, 是三元弱酸,在溶液中存在多种含砷微粒。25℃时各种微粒物质的量分数与溶液pH的关系如图所示。其中a点横坐标值为9.3.回答下列问题。
是三元弱酸,在溶液中存在多种含砷微粒。25℃时各种微粒物质的量分数与溶液pH的关系如图所示。其中a点横坐标值为9.3.回答下列问题。___________ 。
(2)将NaOH溶液滴加到 溶液中,当pH从12调至13时,发生的主要反应的离子方程式是
溶液中,当pH从12调至13时,发生的主要反应的离子方程式是
___________ °
(3) 可写成
可写成 ,
, 的前两步电离是通过和水中
的前两步电离是通过和水中 结合实现的,如第一步电离可以表示为:
结合实现的,如第一步电离可以表示为: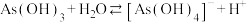 ,第二步电离方程式为:
,第二步电离方程式为:___________ 。
(4)将 和
和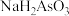 固体按照一定物质的量关系完全溶解在水中,当溶液中离子浓度满足
固体按照一定物质的量关系完全溶解在水中,当溶液中离子浓度满足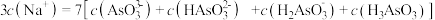 关系时,向水中加入的
关系时,向水中加入的 和
和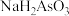 固体的物质的量之比为
固体的物质的量之比为___________ 。
(5)25℃,亚砷酸( )的第一步电离平衡常数
)的第一步电离平衡常数
___________ ,当 时,溶液pH为10.7,则该温度下亚砷酸的第二步电离常数为
时,溶液pH为10.7,则该温度下亚砷酸的第二步电离常数为___________ 。
 )可以用作防腐剂、杀虫剂和除草剂,
)可以用作防腐剂、杀虫剂和除草剂, 是三元弱酸,在溶液中存在多种含砷微粒。25℃时各种微粒物质的量分数与溶液pH的关系如图所示。其中a点横坐标值为9.3.回答下列问题。
是三元弱酸,在溶液中存在多种含砷微粒。25℃时各种微粒物质的量分数与溶液pH的关系如图所示。其中a点横坐标值为9.3.回答下列问题。
(2)将NaOH溶液滴加到
 溶液中,当pH从12调至13时,发生的主要反应的离子方程式是
溶液中,当pH从12调至13时,发生的主要反应的离子方程式是(3)
 可写成
可写成 ,
, 的前两步电离是通过和水中
的前两步电离是通过和水中 结合实现的,如第一步电离可以表示为:
结合实现的,如第一步电离可以表示为: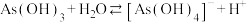 ,第二步电离方程式为:
,第二步电离方程式为:(4)将
 和
和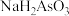 固体按照一定物质的量关系完全溶解在水中,当溶液中离子浓度满足
固体按照一定物质的量关系完全溶解在水中,当溶液中离子浓度满足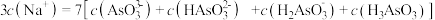 关系时,向水中加入的
关系时,向水中加入的 和
和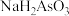 固体的物质的量之比为
固体的物质的量之比为(5)25℃,亚砷酸(
 )的第一步电离平衡常数
)的第一步电离平衡常数
 时,溶液pH为10.7,则该温度下亚砷酸的第二步电离常数为
时,溶液pH为10.7,则该温度下亚砷酸的第二步电离常数为
您最近一年使用:0次
解题方法
2 . 写出下列反应的离子反应方程式。
(1)氧化铜与硫酸反应:___________ ;
(2)铁与稀盐酸反应:___________ ;
(3)氯气与NaOH溶液反应:___________ ;
(4)过氧化钠与水反应:___________ ;
(5)氢氧化钡溶液与稀硫酸反应:___________ ;
(6)二氧化氮通入水中反应:___________ ;
(7)稀硝酸与Cu的反应:___________ 。
(1)氧化铜与硫酸反应:
(2)铁与稀盐酸反应:
(3)氯气与NaOH溶液反应:
(4)过氧化钠与水反应:
(5)氢氧化钡溶液与稀硫酸反应:
(6)二氧化氮通入水中反应:
(7)稀硝酸与Cu的反应:
您最近一年使用:0次
解题方法
3 . 硫元素具有广泛的应用。
(1)S的原子结构示意图为_______ 。一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是_______ ,两种化合物均含有的化学键为_______ 。
(2)煅烧黄铁矿( )的原理为:
)的原理为: 。该反应中氧化剂和氧化产物的物质的量之比为
。该反应中氧化剂和氧化产物的物质的量之比为_______ 。产生的 可用
可用 溶液吸收,该反应的离子方程式是
溶液吸收,该反应的离子方程式是_______ 。
(3)过二硫酸钠( )在较高温度完全分解,
)在较高温度完全分解,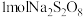 分解生成
分解生成 焦硫酸钠和标况下
焦硫酸钠和标况下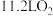 ,则焦硫酸钠的化学式为
,则焦硫酸钠的化学式为_______ 。
(4) 溶液可降解有机污染物4-CP。原因是
溶液可降解有机污染物4-CP。原因是 溶液在一定条件下可产生强氧化性自由基(
溶液在一定条件下可产生强氧化性自由基( ),通过测定4-CP降解率可判断
),通过测定4-CP降解率可判断 溶液产生
溶液产生 的量。某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生
的量。某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生 的影响。
的影响。
①溶液酸碱性的影响:已知 +H+=
+H+= +
+ ,由此判断,溶液酸性增强,降解4-CP的效果
,由此判断,溶液酸性增强,降解4-CP的效果_______ (填“越好”、“越差”或“无影响”)
②Fe2+浓度的影响:相同条件下,将不同浓度 溶液分别加入
溶液分别加入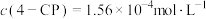 、
、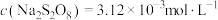 的混合溶液中。反应
的混合溶液中。反应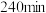 后测得实验结果如图所示。
后测得实验结果如图所示。 +Fe2+=
+Fe2+= +
+ +Fe3+。则由图示可知下列说法正确的是:
+Fe3+。则由图示可知下列说法正确的是:_______ (填序号)
A.反应开始一段时间内,4-CP降解率随Fe2+浓度的增大而增大,其原因是Fe2+能使Na2S2O8产生更多的 。
。
B.Fe2+是4-CP降解反应的催化剂
C.当c(Fe2+)过大时,4-CP降解率反而下降,原因可能是Fe2+会与 发生反应,消耗部分
发生反应,消耗部分
D.4-CP降解率反而下降,原因可能是生成的Fe3+水解使溶液的酸性增强,不利于降解反应的进行
③当c(Fe2+)=3.2×10-3mol/L时,4-CP降解的降解率为_______ ,4-CP降解平均反应速率的计算表达式为_______ 。
(1)S的原子结构示意图为
(2)煅烧黄铁矿(
 )的原理为:
)的原理为: 。该反应中氧化剂和氧化产物的物质的量之比为
。该反应中氧化剂和氧化产物的物质的量之比为 可用
可用 溶液吸收,该反应的离子方程式是
溶液吸收,该反应的离子方程式是(3)过二硫酸钠(
 )在较高温度完全分解,
)在较高温度完全分解,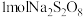 分解生成
分解生成 焦硫酸钠和标况下
焦硫酸钠和标况下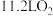 ,则焦硫酸钠的化学式为
,则焦硫酸钠的化学式为(4)
 溶液可降解有机污染物4-CP。原因是
溶液可降解有机污染物4-CP。原因是 溶液在一定条件下可产生强氧化性自由基(
溶液在一定条件下可产生强氧化性自由基( ),通过测定4-CP降解率可判断
),通过测定4-CP降解率可判断 溶液产生
溶液产生 的量。某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生
的量。某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生 的影响。
的影响。①溶液酸碱性的影响:已知
 +H+=
+H+= +
+ ,由此判断,溶液酸性增强,降解4-CP的效果
,由此判断,溶液酸性增强,降解4-CP的效果②Fe2+浓度的影响:相同条件下,将不同浓度
 溶液分别加入
溶液分别加入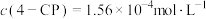 、
、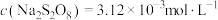 的混合溶液中。反应
的混合溶液中。反应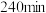 后测得实验结果如图所示。
后测得实验结果如图所示。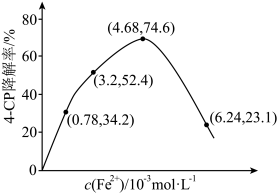
 +Fe2+=
+Fe2+= +
+ +Fe3+。则由图示可知下列说法正确的是:
+Fe3+。则由图示可知下列说法正确的是:A.反应开始一段时间内,4-CP降解率随Fe2+浓度的增大而增大,其原因是Fe2+能使Na2S2O8产生更多的
 。
。B.Fe2+是4-CP降解反应的催化剂
C.当c(Fe2+)过大时,4-CP降解率反而下降,原因可能是Fe2+会与
 发生反应,消耗部分
发生反应,消耗部分
D.4-CP降解率反而下降,原因可能是生成的Fe3+水解使溶液的酸性增强,不利于降解反应的进行
③当c(Fe2+)=3.2×10-3mol/L时,4-CP降解的降解率为
您最近一年使用:0次
4 . 工业合成氨的反应为N2(g)+3H2(g)=2NH3(g)  H=-92.2kJ/mol,其部分工艺流程如图所示。
H=-92.2kJ/mol,其部分工艺流程如图所示。
反应体系中各组分的部分性质如表所示。
回答下列问题:
(1)该反应随着温度升高,K值_______ (填“增大”“减小”或“不变”)。
(2)合成氨反应的平衡常数很小,所以在工业上将气体循环利用,即反应后通过把混合气体的温度降低到略低于_______ ℃,将_______ 分离出来;继续循环利用的气体是_______ ;
(3)请你运用平衡移动的原理结合合成氨反应特点对合成氨采用高温条件的合理性进行分析_______ 。
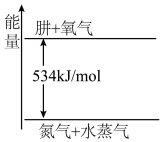
(4)氮元素的另一种氢化物肼的熔点 1℃,沸点 113℃。可视为NH3分子中的一个氢原子被 -NH2(氨基)取代形成的。已知 25℃时,32 克肼在空气中完全燃烧时的能量变化如图所示,则该反应的热化学方程式为_______ 。
 H=-92.2kJ/mol,其部分工艺流程如图所示。
H=-92.2kJ/mol,其部分工艺流程如图所示。反应体系中各组分的部分性质如表所示。
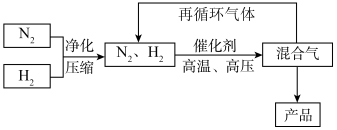
| 气体 | N2 | H2 | NH3 |
| 熔点/℃ | -210.0 | -252.8 | -77.7 |
| 沸点/℃ | -195.8 | -259.2 | -33.4 |
(1)该反应随着温度升高,K值
(2)合成氨反应的平衡常数很小,所以在工业上将气体循环利用,即反应后通过把混合气体的温度降低到略低于
(3)请你运用平衡移动的原理结合合成氨反应特点对合成氨采用高温条件的合理性进行分析
(4)氮元素的另一种氢化物肼的熔点 1℃,沸点 113℃。可视为NH3分子中的一个氢原子被 -NH2(氨基)取代形成的。已知 25℃时,32 克肼在空气中完全燃烧时的能量变化如图所示,则该反应的热化学方程式为
您最近一年使用:0次
解题方法
5 . 如表是 25℃时某些弱酸的电离平衡常数。
(1)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,用离子方程式解释其主要原因_______ 。
(2)pH相同的NaC1O和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COOK_______ NaC1O,两溶液中:[c(Na+)-c(ClO-)]_______ [c(K+)-c(CH3COO-)](填“>”“<” 或“=”)。
(3)25℃时,向0.1mol·L-1CH3COOH 溶液中滴加 NaOH 溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液的 pH=_______ 。
(4)H2CO3与含等物质的量的 KOH 的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序_______ 。
| 化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
| Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(2)pH相同的NaC1O和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COOK
(3)25℃时,向0.1mol·L-1CH3COOH 溶液中滴加 NaOH 溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液的 pH=
(4)H2CO3与含等物质的量的 KOH 的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序
您最近一年使用:0次
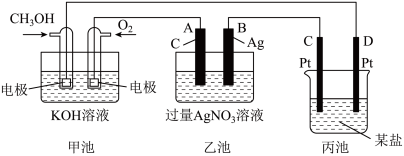
6 . 如图是一个电化学过程的示意图。_______ 装置(填“电解池”或“原电池”),CH3OH 所在电极上发生的电极反应式为_______ 。
(2)乙池中石墨电极A上发生的电极反应式_______ 。
(3)若丙池内为足量 NaCl 溶液,则随着反应进行,丙池中 Cl-_______ (填“向左”,“向右”,“不”)移动,当甲池内通入11.2LO2(标准状况下),则丙池中产生的气体的体积为_______ L(标准状况下),若此时测得乙池体积为500ml。取出2.5ml稀释到1L,则其pH=_______ 。
(2)乙池中石墨电极A上发生的电极反应式
(3)若丙池内为足量 NaCl 溶液,则随着反应进行,丙池中 Cl-
您最近一年使用:0次
7 . I.已知:①H₂O(g)=H₂(g)+ O₂(g) ΔH =+241.8kJ/mol
O₂(g) ΔH =+241.8kJ/mol
②C(s)+ O₂(g) =CO(g) ΔH =-110.5kJ/mol
O₂(g) =CO(g) ΔH =-110.5kJ/mol
③C(s)+O₂(g)=CO₂(g) ΔH=-393.5kJ/mol
请填写下列空白。
(1)上述反应中属于吸热反应的是_________ (填号)。
(2)表示C燃烧的热化学方程式为_______ (填号)
(3)10g H₂完全燃烧生成水蒸气,放出的热量为____________ .
(4)比较②的ΔH_____ ③的ΔH大小 (填“大于”“等于”或“小于”)。
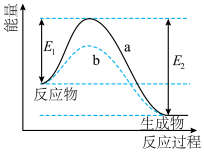
Ⅱ.如图所示,某反应在不同条件下的反应历程分别为a、b。_______ (填“>“<”或”=”)生成物的总键能,则该反应的反应热ΔH=_______________ (用E1,E2表示)。
 O₂(g) ΔH =+241.8kJ/mol
O₂(g) ΔH =+241.8kJ/mol②C(s)+
 O₂(g) =CO(g) ΔH =-110.5kJ/mol
O₂(g) =CO(g) ΔH =-110.5kJ/mol ③C(s)+O₂(g)=CO₂(g) ΔH=-393.5kJ/mol
请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)表示C燃烧的热化学方程式为
(3)10g H₂完全燃烧生成水蒸气,放出的热量为
(4)比较②的ΔH
Ⅱ.如图所示,某反应在不同条件下的反应历程分别为a、b。
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据上表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同_______ 。
(2)实验2中负极减少54g,则电路中转移_______ mol电子。
(3)实验3中铝为_______ 极,电极反应式为_______ 。
(4)实验4中铝电极的电极反应式为_______ 。
(5)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响_______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)实验1、2中Al电极的作用是否相同
(2)实验2中负极减少54g,则电路中转移
(3)实验3中铝为
(4)实验4中铝电极的电极反应式为
(5)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响
您最近一年使用:0次
解题方法
9 . 回答下列问题。
Ⅰ.一定条件下,在2L密闭容器中发生反应:3A(g)+B(g) 2C(g),开始时加入4molA、6molB、2molC、2min末测得C的物质的量是3mol。
2C(g),开始时加入4molA、6molB、2molC、2min末测得C的物质的量是3mol。
(1)用A的浓度变化表示的反应速率是_______ ;
(2)在2min末,B的浓度为_______ ;
(3)将容器的体积变为3L,化学反应速率_______ (填变大、变小或不变)。
Ⅱ. 粗盐中除含有泥沙等难溶性杂质外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质,现欲得到纯净的氯化钠晶体,需经过多步操作。试回答:
(4)将粗盐溶于水,得到悬浊液,为除去难溶性杂质,需要选用的玻璃仪器有_______ 。
(5)欲除去粗盐溶液中的Mg2+、Ca2+、SO ,应向粗盐溶液中依次加入过量的NaOH溶液、
,应向粗盐溶液中依次加入过量的NaOH溶液、_______ (填化学式)溶液、_______ (填化学式)溶液,然后过滤。
(6)向(5)中所得滤液中滴加_______ 至无气泡产生。再经蒸发结晶得到氯化钠晶体。
Ⅰ.一定条件下,在2L密闭容器中发生反应:3A(g)+B(g)
 2C(g),开始时加入4molA、6molB、2molC、2min末测得C的物质的量是3mol。
2C(g),开始时加入4molA、6molB、2molC、2min末测得C的物质的量是3mol。(1)用A的浓度变化表示的反应速率是
(2)在2min末,B的浓度为
(3)将容器的体积变为3L,化学反应速率
Ⅱ. 粗盐中除含有泥沙等难溶性杂质外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质,现欲得到纯净的氯化钠晶体,需经过多步操作。试回答:
(4)将粗盐溶于水,得到悬浊液,为除去难溶性杂质,需要选用的玻璃仪器有
(5)欲除去粗盐溶液中的Mg2+、Ca2+、SO
 ,应向粗盐溶液中依次加入过量的NaOH溶液、
,应向粗盐溶液中依次加入过量的NaOH溶液、(6)向(5)中所得滤液中滴加
您最近一年使用:0次
名校
解题方法
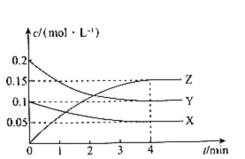
10 . 实验小组对可逆反应aX(g)+bY(g)=pZ(g)进行探究。T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y 、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
(1)a:b:p=_____________ 。
(2)Y的平衡转化率为_______ 。
(3)0~4min内的反应速率v(Z)=_______________ 。
(4)下列事实能说明反应达到平衡状态的是________ (填选项字母)。
A.容器内气体压强不再改变
B.混合气体密度不再改变
C.X的体积分数不再改变
(5)该温度下,该反应的平衡常数K的数值为:_________ 。
(6)若在不同条件下进行上述反应,测得反应速率分别为:①v(X)=0.1mol·L-1·min-1、②v(Y)=0.4 mol·L-1·min-1、③v(Z)=0.5 mol·L-1·min-1,其中反应速率最快的是________ (填序号)
(1)a:b:p=
(2)Y的平衡转化率为
(3)0~4min内的反应速率v(Z)=
(4)下列事实能说明反应达到平衡状态的是
A.容器内气体压强不再改变
B.混合气体密度不再改变
C.X的体积分数不再改变
(5)该温度下,该反应的平衡常数K的数值为:
(6)若在不同条件下进行上述反应,测得反应速率分别为:①v(X)=0.1mol·L-1·min-1、②v(Y)=0.4 mol·L-1·min-1、③v(Z)=0.5 mol·L-1·min-1,其中反应速率最快的是
您最近一年使用:0次



