名校
解题方法
1 . I.某有机物M分子的结构式如图所示:
(1)写出M的结构简式和键线式:___________ 、___________ 。
(2)下列给出了四种有机物的结构简式:A.HOCH2CH2CH=CH2;B.CH3OCH2CH=CH2;C.CH3CH2CH2CHO;D.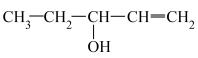 ;E.
;E. ;
;
与M属于同系物的是___________ (填选项字母,下同),互为同分异构体且官能团种类不同的是___________ ,互为同分异构体且官能团种类相同的是___________ 。
Ⅱ.利用核磁共振技术测定有机物分子三维结构的研究获得了2002年诺贝尔化学奖。某研究小组为测定某有机化合物A的结构,进行如下实验:
(3)①将有机物A置于氧气流中充分燃烧,实验测得:生成18.0gH2O和44.0gCO2,消耗氧气28.0L(标准状况),则该物质的实验式是___________ 。
②使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如图所示:___________ ,根据图2、图3(只有一组吸收峰)推测:A的结构简式为___________ (分子中有1个六元环)。
③写出化合物A属于酯类的同分异构体的结构简式:___________ (任写一种即可)。

(1)写出M的结构简式和键线式:
(2)下列给出了四种有机物的结构简式:A.HOCH2CH2CH=CH2;B.CH3OCH2CH=CH2;C.CH3CH2CH2CHO;D.
 ;E.
;E. ;
;与M属于同系物的是
Ⅱ.利用核磁共振技术测定有机物分子三维结构的研究获得了2002年诺贝尔化学奖。某研究小组为测定某有机化合物A的结构,进行如下实验:
(3)①将有机物A置于氧气流中充分燃烧,实验测得:生成18.0gH2O和44.0gCO2,消耗氧气28.0L(标准状况),则该物质的实验式是
②使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如图所示:
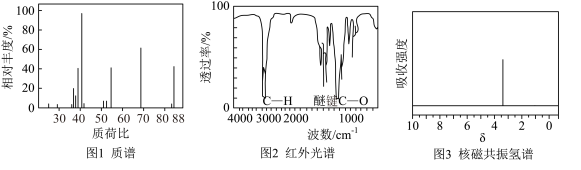
③写出化合物A属于酯类的同分异构体的结构简式:
您最近一年使用:0次
名校
2 . 根据已学知识,请回答下列问题
(1)物质A的结构简式为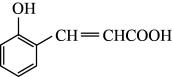 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称_____________________________ 。
(2)有机化合物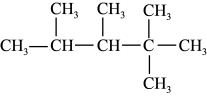 的名称是
的名称是_________________ ,其在核磁共振氢谱上有_________ 组峰。
(3)键线式 表示的有机物的分子式为
表示的有机物的分子式为 _________ ,其中等效氢个数比为_________________ 。
(4)写出1,3一丁二烯与 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:_________________________________________________ 。
(5)与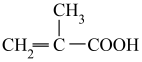 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为_____________________ 。
(1)物质A的结构简式为
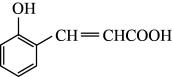 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称(2)有机化合物
 的名称是
的名称是(3)键线式
 表示的有机物的分子式为
表示的有机物的分子式为 (4)写出1,3一丁二烯与
 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:(5)与
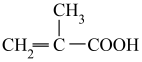 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为
您最近一年使用:0次
3 . 硫的氧化物、氮的氧化物、硅的氧化物都是重要的化工原料。将其合理利用,既能减少污染,又能充分利用资源,创造价值。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是_______ (填化学式),该物质的类别属于_______ 氧化物(填“碱性”、 “酸性”或“两性”),实验室中不能用带玻璃塞的试剂瓶盛放NaOH溶液,原因是_______________ (用离子方程式表示)。
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有________ 、_______ 、_______ ,工艺师常用_________ (填物质名称)来雕刻玻璃,其作用过程产生________ 气体。
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料_________ (写该材料名称)的主要原料
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_________________ 。
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是_______________ (用化学方程式表示)。硝酸是一种易挥发性的酸,用蘸浓硝酸和蘸浓氨水的玻璃棒靠近会产生大量白烟,白烟的成分是__________ 。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
| A.碳酸钠 | B.氢氧化钠 | C.氢氧化钾 | D.氯化钠 |
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是
您最近一年使用:0次
名校
解题方法
4 . 酸碱中和滴定法在工农业生产和医药卫生等方面都有非常重要的作用。
I.某学生用0.2000mol·L 的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
(1)以上步骤有错误的是___________ (填编号)。
(2)判断滴定终点的现象:___________ 。
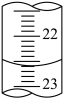
(3)如图是某次滴定时的滴定管中的液面,其读数为___________ mL。___________ mol⋅L-1。
II.温度t℃时,某NaOH稀溶液中 mol⋅L-1,
mol⋅L-1, mol⋅L-1,已知
mol⋅L-1,已知 ,请回答下列问题:
,请回答下列问题:
(5)该NaOH溶液中NaOH的物质的量浓度为___________ ,该NaOH溶液中由水电离出的 为
为___________ 。
(6)给该NaOH溶液加热时,pH___________ (填“变大”、“变小”或“不变”)。
I.某学生用0.2000mol·L
 的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
(1)以上步骤有错误的是
(2)判断滴定终点的现象:
(3)如图是某次滴定时的滴定管中的液面,其读数为
| 滴定次数 | 待测体积(mL) | 标准烧碱溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.402 | 0.40 |
| 第二次 | 20.00 | 2.002 | 4.10 |
| 第三次 | 20.00 | 4.002 | 4.00 |
II.温度t℃时,某NaOH稀溶液中
 mol⋅L-1,
mol⋅L-1, mol⋅L-1,已知
mol⋅L-1,已知 ,请回答下列问题:
,请回答下列问题:(5)该NaOH溶液中NaOH的物质的量浓度为
 为
为(6)给该NaOH溶液加热时,pH
您最近一年使用:0次
解题方法
5 . 某烃A的相对分子质量为84。回答下列问题:
(1)物质的量相同,下列物质充分燃烧与A消耗氧气的量不相等的是(填序号)_______。
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为_______ 。
(3)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为_______ 。
(4)有机物B可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的B为无色黏稠液体,易溶于水。为研究B的组成与结构,进行了如下实验:
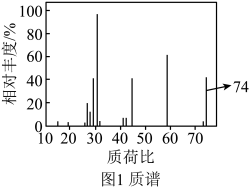
①B的质谱如图1,则B的相对分子质量为:_______ 。_______ 。
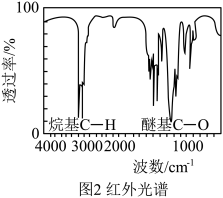
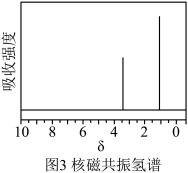
③B的红外光谱如图2,写出B中含有的官能团_______ 。_______ 。
(1)物质的量相同,下列物质充分燃烧与A消耗氧气的量不相等的是(填序号)_______。
| A.C7H12O2 | B.C6H14 | C.C6H14O | D.C7H14O3 |
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为
(3)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为
(4)有机物B可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的B为无色黏稠液体,易溶于水。为研究B的组成与结构,进行了如下实验:
①B的质谱如图1,则B的相对分子质量为:
③B的红外光谱如图2,写出B中含有的官能团
您最近一年使用:0次
6 . 按要求回答下列问题
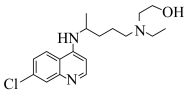
(1)2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎,其中羟基氯喹结构如图所示。_______ 。
②羟基氯喹分子中基态Cl原子核外电子有_______ 种空间运动状态。
③羟基氯喹分子中C原子的杂化类型为_______ 。
④所有N原子的VSEPR模型为_______ 。
⑤请在答题卡中,用*标出羟基氯喹分子中的手性碳原子_______ 。
⑥下列现代分析手段中,可用于检测羟基氯的晶体结构是_______ 。
A.X射线衍射 B.原子光谱 C.元素分析 D.红外光谱
(2)“立方烷”是合成的一种烃,其分子为正方体结构,其碳骨架结构如下图所示,则:_______ 。
②立方烷的二氯代物有_______ 种同分异构体。
(1)2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎,其中羟基氯喹结构如图所示。
②羟基氯喹分子中基态Cl原子核外电子有
③羟基氯喹分子中C原子的杂化类型为
④所有N原子的VSEPR模型为
⑤请在答题卡中,用*标出羟基氯喹分子中的手性碳原子
⑥下列现代分析手段中,可用于检测羟基氯的晶体结构是
A.X射线衍射 B.原子光谱 C.元素分析 D.红外光谱
(2)“立方烷”是合成的一种烃,其分子为正方体结构,其碳骨架结构如下图所示,则:
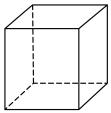
②立方烷的二氯代物有
您最近一年使用:0次
名校
解题方法
7 . 火箭发射时可以用肼( )作为燃料,其燃烧过程中的能量变化如图所示。回答下列问题:
)作为燃料,其燃烧过程中的能量变化如图所示。回答下列问题: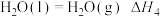 。
。
(1)由图可知,
______ (填“ ”或“
”或“ ”)0,理由为
”)0,理由为_____________ 。
(2)基态氮原子的电子排布式为______ 。
(3)0.1mol 分子中含有
分子中含有______ mol极性共价键, 分子中氮原子的杂化方式为
分子中氮原子的杂化方式为______ 。
(4) 分子中,
分子中, 键和
键和 键的数目之比为
键的数目之比为______ 。
(5)稳定性:
______ (填“ ”或“
”或“ ”)
”) 。
。
(6)由图可知,每转移0.2mol电子,消耗 的体积为
的体积为______ L(标准状况下)。
(7)表示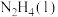 燃烧热的热化学方程式为
燃烧热的热化学方程式为______________ (焓变用含 和
和 的代数式表示)。
的代数式表示)。
 )作为燃料,其燃烧过程中的能量变化如图所示。回答下列问题:
)作为燃料,其燃烧过程中的能量变化如图所示。回答下列问题: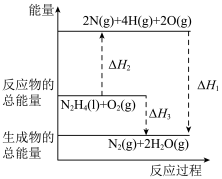
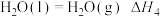 。
。(1)由图可知,

 ”或“
”或“ ”)0,理由为
”)0,理由为(2)基态氮原子的电子排布式为
(3)0.1mol
 分子中含有
分子中含有 分子中氮原子的杂化方式为
分子中氮原子的杂化方式为(4)
 分子中,
分子中, 键和
键和 键的数目之比为
键的数目之比为(5)稳定性:

 ”或“
”或“ ”)
”) 。
。(6)由图可知,每转移0.2mol电子,消耗
 的体积为
的体积为(7)表示
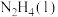 燃烧热的热化学方程式为
燃烧热的热化学方程式为 和
和 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
8 . X、Y、Z、W四种元素的部分信息如下表所示。回答下列问题:
(1)W的基态原子电子排布式为_______ ,X、Z两种元素简单氢化物的稳定性顺序为_______ (用化学式填写)。
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型分子构型是正四面体的是_______ (填化学式,下同),不是sp3杂化的是_______ ,ZX3属于_______ (极性分子、非极性分子)。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为_______ 。
(4)Z原子的价电子轨道表示式为_______ 。
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为_______ ;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的晶胞密度可表示为_______ g/cm3(列出计算式)。
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,WX2溶液呈浅绿色、WX3溶液呈黄色 |
(1)W的基态原子电子排布式为
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型分子构型是正四面体的是
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为
(4)Z原子的价电子轨道表示式为
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为

您最近一年使用:0次
名校
解题方法
9 . 硫、硒、碲的化合物在农药、石油工业、矿物开采、萃取及有机合成等领域的应用广泛。回答下列问题:
(1)基态Se原子的价层电子排布式为___________ 。
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
(3)类卤素 分子结构式为
分子结构式为___________ ,1mol 中含有π键的数目为
中含有π键的数目为___________ ,HSCN结构有两种,已知硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是___________ 。
(4)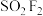 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
___________  (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是___________ 。
(1)基态Se原子的价层电子排布式为
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
A.氧族元素气态氢化物的稳定性按 、 、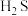 、 、 、 、 的顺序依次减弱 的顺序依次减弱 |
| B.其氢化物中的键长按O―H、S―H、Se―H、Te―H的顺序依次减小 |
C.其阴离子的还原性按 、 、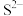 、 、 、 、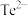 的顺序依次增强 的顺序依次增强 |
D.其最高价氧化物的水化物酸性按 、 、 、 、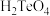 顺序依次增强 顺序依次增强 |
(3)类卤素
 分子结构式为
分子结构式为 中含有π键的数目为
中含有π键的数目为 )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是(4)
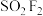 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是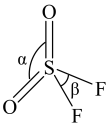

 (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是
您最近一年使用:0次
名校
解题方法
10 . 晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钴、钙等多种化学物质。请回答下列问题:
(1)科学家常利用仪器进行___________ 实验来区分晶体硼和无定形硼,二者之间的关系互为___________ 。第二周期元素的第一电离能按由小到大的顺序排列,B元素排在第___________ 位,其基态能量最高的能级电子云轮廓图为___________ 形。
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为___________ ,Si原子的杂化类型为___________ 。 的几何构型为正八面体形,Co在中心。
的几何构型为正八面体形,Co在中心。 中,1个Co提供
中,1个Co提供___________ 个空轨道。该配位离子的作用力为___________ (填序号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
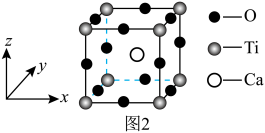
(4)一种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。与Ti紧邻的Ca有___________ 个。晶胞中Ca原子坐标参数为___________ 。
(1)科学家常利用仪器进行
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为

 的几何构型为正八面体形,Co在中心。
的几何构型为正八面体形,Co在中心。 中,1个Co提供
中,1个Co提供A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
(4)一种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。与Ti紧邻的Ca有
您最近一年使用:0次



