名校
1 . 按要求填空:
Ⅰ.下列各组中的两种有机物,可能是:
(A)相同的物质,(B)同系物,(C)同分异构体。
(1)请判断它们之间的关系(用a、B、C填空)
①2-甲基丁烷和丁烷___________ ,
②正戊烷和2,2-二甲基丙烷___________ ,
③对二甲苯和1,4—二甲苯___________ ,
④1-己烯和环己烷___________ 。
Ⅱ.按官能团的不同,可以对有机物进行分类,将符合要求的答案(用序号填空)填在横线上。___________ ,
②醛:___________ ,
③酯:___________ 。
Ⅰ.下列各组中的两种有机物,可能是:
(A)相同的物质,(B)同系物,(C)同分异构体。
(1)请判断它们之间的关系(用a、B、C填空)
①2-甲基丁烷和丁烷
②正戊烷和2,2-二甲基丙烷
③对二甲苯和1,4—二甲苯
④1-己烯和环己烷
Ⅱ.按官能团的不同,可以对有机物进行分类,将符合要求的答案(用序号填空)填在横线上。
①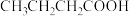 ②
②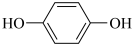 ③
③ 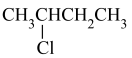 ④
④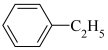 ⑤
⑤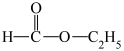 ⑥
⑥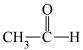
②醛:
③酯:
您最近一年使用:0次
解题方法
2 . 认识有机物组成和结构对有机物的学习非常重要。
Ⅰ.根据下列有机物的空间填充模型,填空。_______ 种;
(2)乙中σ键与π键的个数比为_______ ;
(3)丙中碳原子的杂化方式_______ ;
(4)丁的结构简式为_______ ;
(5)分子中所有原子一定在同一平面内的是_______ (填序号)。
Ⅱ.中药小柴胡可以用来治疗感冒发烧,其主要成分之一是山奈酚,结构如图所示。_______ mol  。
。
Ⅲ.以下是几种烃分子的球棍模型:_______ 。
(8)写出D的键线式_______ 。
Ⅰ.根据下列有机物的空间填充模型,填空。
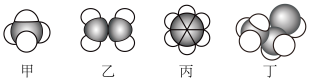
(2)乙中σ键与π键的个数比为
(3)丙中碳原子的杂化方式
(4)丁的结构简式为
(5)分子中所有原子一定在同一平面内的是
Ⅱ.中药小柴胡可以用来治疗感冒发烧,其主要成分之一是山奈酚,结构如图所示。
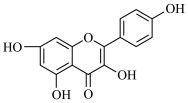
 。
。Ⅲ.以下是几种烃分子的球棍模型:
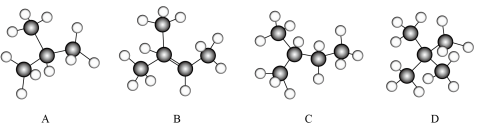
(8)写出D的键线式
您最近一年使用:0次
3 . 用系统命名法命名下列物质:
①
____________ 
____________
①

②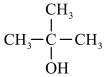
③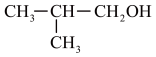
④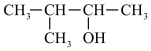

您最近一年使用:0次
名校
4 . 环境保护与绿色发展是新时代人们关心的共同话题。NO、 是大气主要污染物,因此对工业烟气(主要成分为
是大气主要污染物,因此对工业烟气(主要成分为 ,
, 、
、 )脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。
)脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。
(1)碱液吸收:NaOH溶液可吸收工业烟气,获得副产品 。
。
①等物质的量的NO与 被NaOH溶液吸收,反应的离子方程式为
被NaOH溶液吸收,反应的离子方程式为____________ 。
②若吸收时NO与 的比例控制不当,则吸收液经浓缩结晶、过滤得到的
的比例控制不当,则吸收液经浓缩结晶、过滤得到的 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是______ (填化学式)。
(2)目前常见方法是采用酸化处理的NaClO溶液液相氧化法脱除烟气中的 ,其主要过程如下:
,其主要过程如下:
Ⅰ.
 kJ/mol
kJ/mol
Ⅱ.
 kJ/mol
kJ/mol
①写出 转化为
转化为 的热化学方程式:
的热化学方程式:____________ 。
②研究不同温度下对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是______ 。
(3)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和 共7mol的混合气体完全转化为
共7mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为______ 。
方法1:直接使用尿素 溶液吸收烟气中的
溶液吸收烟气中的 。
。
方法2:先用合适的氧化剂将 中的NO氧化为
中的NO氧化为 ,再用
,再用 溶液还原吸收。
溶液还原吸收。
还原吸收等量的 ,消耗尿素较少的是
,消耗尿素较少的是______ (填“方法1”或“方法2”)。工业上选择方法2处理 的原因是
的原因是____________ 。
 是大气主要污染物,因此对工业烟气(主要成分为
是大气主要污染物,因此对工业烟气(主要成分为 ,
, 、
、 )脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。
)脱硝是工业生产中的重要一环。脱除的方法有多种,比较常见的有水吸收法、酸吸收法、碱吸收法、氧化吸收法、还原吸收法和综合吸收法等。(1)碱液吸收:NaOH溶液可吸收工业烟气,获得副产品
 。
。①等物质的量的NO与
 被NaOH溶液吸收,反应的离子方程式为
被NaOH溶液吸收,反应的离子方程式为②若吸收时NO与
 的比例控制不当,则吸收液经浓缩结晶、过滤得到的
的比例控制不当,则吸收液经浓缩结晶、过滤得到的 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是(2)目前常见方法是采用酸化处理的NaClO溶液液相氧化法脱除烟气中的
 ,其主要过程如下:
,其主要过程如下:Ⅰ.

 kJ/mol
kJ/molⅡ.

 kJ/mol
kJ/mol①写出
 转化为
转化为 的热化学方程式:
的热化学方程式:②研究不同温度下对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
(3)氨气催化吸收处理尾气法:已知6mol氨气恰好能将含NO和
 共7mol的混合气体完全转化为
共7mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为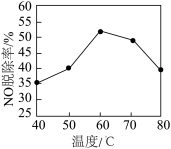
方法1:直接使用尿素
 溶液吸收烟气中的
溶液吸收烟气中的 。
。方法2:先用合适的氧化剂将
 中的NO氧化为
中的NO氧化为 ,再用
,再用 溶液还原吸收。
溶液还原吸收。还原吸收等量的
 ,消耗尿素较少的是
,消耗尿素较少的是 的原因是
的原因是
您最近一年使用:0次
名校
5 . 氮族元素是位于元素周期表ⅤA族的元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)等,这一族元素在化合物中可以呈现-3、+1、+2、+3、+4、+5等多种化合价,它们的原子最外层都有5个电子。回答下列问题:
(1)白磷( )分子为正四面体结构,
)分子为正四面体结构, 键角为
键角为______ 。
(2)第三周期元素中第一电离能比P小的元素有______ 种。
(3)写出基态As原子核外简化电子排布式:______ 。
(4)根据铋(Bi)核外电子排布,得知Bi属于周期表______ 区。
(5)五氧化二锑( )可由
)可由 通过水解制得,写出该反应的化学方程式:
通过水解制得,写出该反应的化学方程式:____________ ;为提高水解率可采取的措施有______ 。
(1)白磷(
 )分子为正四面体结构,
)分子为正四面体结构, 键角为
键角为(2)第三周期元素中第一电离能比P小的元素有
(3)写出基态As原子核外简化电子排布式:
(4)根据铋(Bi)核外电子排布,得知Bi属于周期表
(5)五氧化二锑(
 )可由
)可由 通过水解制得,写出该反应的化学方程式:
通过水解制得,写出该反应的化学方程式:
您最近一年使用:0次
6 . 完成下列问题。
(1) 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):________ 。
(2)室温时, 的
的 溶液中由水电离出的
溶液中由水电离出的
______  。
。
(3)室温时, 的Ba(OH)2溶液,
的Ba(OH)2溶液,
________ 。
(4)室温下pH=3的 水溶液水电离的c(H+)
水溶液水电离的c(H+)______  。
。
(5)常温下pH=13的 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=______ 。
(6)常温下0.1 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb=_______ ,常温下0.1 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=_______ 。
(1)
 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):(2)室温时,
 的
的 溶液中由水电离出的
溶液中由水电离出的
 。
。(3)室温时,
 的Ba(OH)2溶液,
的Ba(OH)2溶液,
(4)室温下pH=3的
 水溶液水电离的c(H+)
水溶液水电离的c(H+) 。
。(5)常温下pH=13的
 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=(6)常温下0.1
 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb= 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=
您最近一年使用:0次
7 . 已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,pH相同的三种溶液①NaF溶液;②NaClO溶液;③Na2CO3溶液,其物质的量浓度由大到小的顺序是_______ 。(填序号)
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_______ 。
(3)室温下,经测定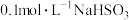 溶液
溶液 ,则
,则
_______  (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(4) 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显_______ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(5)将含 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
_______ 。
| 化学式 |  |  |  |  |  |
| 电离常数 |  |  |  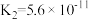 |   |  |
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(3)室温下,经测定
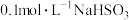 溶液
溶液 ,则
,则
 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(4)
 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显 的电离平衡常数
的电离平衡常数
(5)将含
 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
您最近一年使用:0次
8 . 研究有机化学反应的机理,有利于揭示反应过程中化学键变化情况,有利于人们控制反应变化设计合成产品。
(1) 与
与 在光照条件下发生链式反应。氯自由基(
在光照条件下发生链式反应。氯自由基( )碰撞
)碰撞 生成甲基自由基(
生成甲基自由基(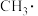 ),反应方程式为
),反应方程式为 ,甲基自由基碰撞
,甲基自由基碰撞 时可生成
时可生成 ,该步反应方程式为
,该步反应方程式为___________ 。
(2)已知乙醇在铜催化下可被氧化生成乙醛,具有a-H的醛或酮,在酸或碱的催化作用下,与另一分子醛或酮发生缩合,生成β-羟基醛或β-羟基酮。以乙醛为例,其过程表示如下:___________ 。
(3)化工原料Z是X与 反应的主产物,X→Z的反应机理如图:
反应的主产物,X→Z的反应机理如图:___________ 。
(4)对羟基苯甲醛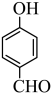 的沸点比邻羟基苯甲醛
的沸点比邻羟基苯甲醛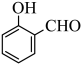 的沸点高,原因是
的沸点高,原因是___________ 。
(5)MgO催化 合成碳酸乙烯酯
合成碳酸乙烯酯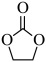 ,反应机理如下图,根据元素电负性变化规律,步骤
,反应机理如下图,根据元素电负性变化规律,步骤 可描述为“环氧乙烷中的O原子吸附在
可描述为“环氧乙烷中的O原子吸附在 上”,步骤
上”,步骤 可描述为
可描述为___________ 。
(1)
 与
与 在光照条件下发生链式反应。氯自由基(
在光照条件下发生链式反应。氯自由基( )碰撞
)碰撞 生成甲基自由基(
生成甲基自由基(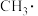 ),反应方程式为
),反应方程式为 ,甲基自由基碰撞
,甲基自由基碰撞 时可生成
时可生成 ,该步反应方程式为
,该步反应方程式为(2)已知乙醇在铜催化下可被氧化生成乙醛,具有a-H的醛或酮,在酸或碱的催化作用下,与另一分子醛或酮发生缩合,生成β-羟基醛或β-羟基酮。以乙醛为例,其过程表示如下:
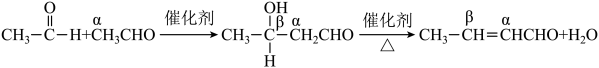
(3)化工原料Z是X与
 反应的主产物,X→Z的反应机理如图:
反应的主产物,X→Z的反应机理如图: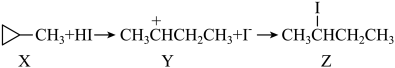
(4)对羟基苯甲醛
 的沸点比邻羟基苯甲醛
的沸点比邻羟基苯甲醛 的沸点高,原因是
的沸点高,原因是(5)MgO催化
 合成碳酸乙烯酯
合成碳酸乙烯酯 ,反应机理如下图,根据元素电负性变化规律,步骤
,反应机理如下图,根据元素电负性变化规律,步骤 可描述为“环氧乙烷中的O原子吸附在
可描述为“环氧乙烷中的O原子吸附在 上”,步骤
上”,步骤 可描述为
可描述为
您最近一年使用:0次
9 . 请按要求回答下列问题。
(1)用括号内的试剂和操作除去下列各物质中的少量杂质,其中正确的是________ 。
A.乙酸乙酯中的乙酸(饱和 、分液)
、分液)
B.苯中的苯酚(浓溴水、过滤)
C.苯甲酸中的氯化钠(水、重结晶)
D.溴苯中的溴(四氯化碳、萃取分液)
E.苯甲酸中的苯甲醛[新制的 悬浊液、蒸馏]
悬浊液、蒸馏]
(2)双酚(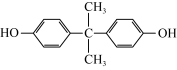 )是一种重要的化工原料,它的一种合成路线如下:
)是一种重要的化工原料,它的一种合成路线如下:________ 。写出G→双酚A的化学方程式:________ 。
(3)有机物A(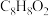 )的红外光谱图如下图所示,A能发生水解反应,分子中不同化学环境的氢原子数目比为
)的红外光谱图如下图所示,A能发生水解反应,分子中不同化学环境的氢原子数目比为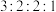 ,其结构简式为
,其结构简式为________ 。A有多种同分异构体,同时满足下列条件(①属于芳香族化合物;②属于酯类;③分子中含有一个甲基)的同分异构体有________ 种。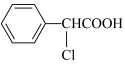 )与足量NaOH溶液加热时反应的化学方程式为
)与足量NaOH溶液加热时反应的化学方程式为________ 。B的同分异构体(不考虑立体异构)中属于酯类且氯原子直接连在苯环上的有________ 种。
(1)用括号内的试剂和操作除去下列各物质中的少量杂质,其中正确的是
A.乙酸乙酯中的乙酸(饱和
 、分液)
、分液) B.苯中的苯酚(浓溴水、过滤)
C.苯甲酸中的氯化钠(水、重结晶)
D.溴苯中的溴(四氯化碳、萃取分液)
E.苯甲酸中的苯甲醛[新制的
 悬浊液、蒸馏]
悬浊液、蒸馏](2)双酚(
 )是一种重要的化工原料,它的一种合成路线如下:
)是一种重要的化工原料,它的一种合成路线如下: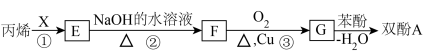
(3)有机物A(
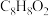 )的红外光谱图如下图所示,A能发生水解反应,分子中不同化学环境的氢原子数目比为
)的红外光谱图如下图所示,A能发生水解反应,分子中不同化学环境的氢原子数目比为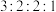 ,其结构简式为
,其结构简式为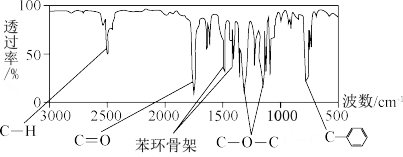
 )与足量NaOH溶液加热时反应的化学方程式为
)与足量NaOH溶液加热时反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 元素周期表中第四周期的某些过渡元素(如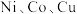 等)在生产、生活中有着广泛的应用.
等)在生产、生活中有着广泛的应用.
(1) 能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下: 核外电子排布式
核外电子排布式_________ ;
② 元素的第一电离能由大到小的顺序为
元素的第一电离能由大到小的顺序为__________ . 的晶胞如图1所示,距离每个
的晶胞如图1所示,距离每个 最近的
最近的 的个数为
的个数为_________ .
(3)已知: 结构如图2所示,该反应
结构如图2所示,该反应________ (选填“是”或“不是”)氧化还原反应,理由是__________ .
(4)有机净化剂的基本组分为大分子立体网格结构的聚合物,可用于工业废水“除钴镍”.其净化原理可表示为: ”表示出
”表示出 参与的配位键
参与的配位键_________ .
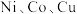 等)在生产、生活中有着广泛的应用.
等)在生产、生活中有着广泛的应用.(1)
 能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
 核外电子排布式
核外电子排布式②
 元素的第一电离能由大到小的顺序为
元素的第一电离能由大到小的顺序为③对羟基苯甲醛( )的沸点为
)的沸点为 ,而水杨醛(
,而水杨醛(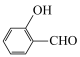 )的沸点为
)的沸点为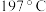 ,请从结构角度解释二者沸点差异原因
,请从结构角度解释二者沸点差异原因
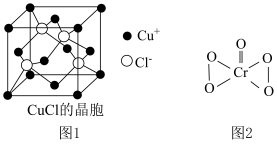
 的晶胞如图1所示,距离每个
的晶胞如图1所示,距离每个 最近的
最近的 的个数为
的个数为(3)已知:
 结构如图2所示,该反应
结构如图2所示,该反应(4)有机净化剂的基本组分为大分子立体网格结构的聚合物,可用于工业废水“除钴镍”.其净化原理可表示为:
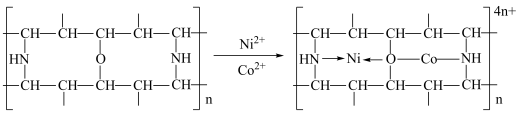
 ”表示出
”表示出 参与的配位键
参与的配位键
您最近一年使用:0次
2024-05-04更新
|
228次组卷
|
2卷引用:江苏省扬州市新华中学2023-2024学年高二下学期4月期中考试化学试题



