1 . 已知  时
时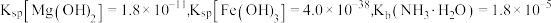 ,下列叙述中不正确的是
,下列叙述中不正确的是
 时
时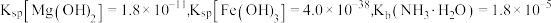 ,下列叙述中不正确的是
,下列叙述中不正确的是A. 时,向等浓度的 时,向等浓度的 和 和 混合溶液中逐滴加入氨水,先出现红褐色沉淀 混合溶液中逐滴加入氨水,先出现红褐色沉淀 |
B. 时, 时, 溶液中有少量 溶液中有少量 时,可以加入 时,可以加入 进行除杂 进行除杂 |
C. 时, 时,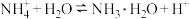 的平衡常数为 的平衡常数为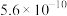 |
D. 时,加大量水稀释氨水,溶液中粒子的浓度均减小 时,加大量水稀释氨水,溶液中粒子的浓度均减小 |
您最近一年使用:0次
名校
解题方法
2 . Ⅰ.硅材料在生活中古有重要地位。请回答:
(1) 分子的空间结构(以Si为中心)为
分子的空间结构(以Si为中心)为______ ,分子中氮原子的杂化轨道类型是______ 。
(2)由硅原子核形成的三种微粒,电子排布式分别为:①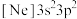 、②
、②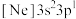 、③
、③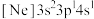 ,有关这些微粒的叙述,正确的是______。
,有关这些微粒的叙述,正确的是______。
(3)Si与P形成的某化合物晶体的晶胞如图。该化合物的化学式为______ 。 和硫铁矿(
和硫铁矿( )联合制备铁精粉(
)联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。
(4) 结构示意图如图1。
结构示意图如图1。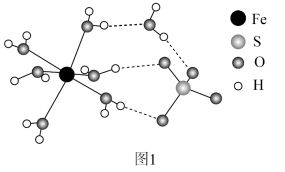
① 的价层电子排布式为
的价层电子排布式为______ 。
② 中O和
中O和 中S均为
中S均为 杂化,比较
杂化,比较 中
中 键角和
键角和 中
中 键角的大小并解释原因
键角的大小并解释原因______ 。
③ 中
中 与
与 、
、 与
与 的作用力类型分别是
的作用力类型分别是______ 。
(5) 晶体的晶胞形状为立方体,边长为a nm,结构如图2。
晶体的晶胞形状为立方体,边长为a nm,结构如图2。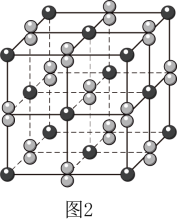
 的摩尔质量为
的摩尔质量为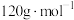 ,阿伏加德罗常数为
,阿伏加德罗常数为 。该晶体的密度为
。该晶体的密度为______  。(
。(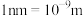 )
)
(1)
 分子的空间结构(以Si为中心)为
分子的空间结构(以Si为中心)为(2)由硅原子核形成的三种微粒,电子排布式分别为:①
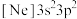 、②
、②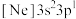 、③
、③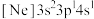 ,有关这些微粒的叙述,正确的是______。
,有关这些微粒的叙述,正确的是______。| A.微粒半径:③>①>② |
| B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.得电子能力:①>② |
(3)Si与P形成的某化合物晶体的晶胞如图。该化合物的化学式为

 和硫铁矿(
和硫铁矿( )联合制备铁精粉(
)联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。(4)
 结构示意图如图1。
结构示意图如图1。
①
 的价层电子排布式为
的价层电子排布式为②
 中O和
中O和 中S均为
中S均为 杂化,比较
杂化,比较 中
中 键角和
键角和 中
中 键角的大小并解释原因
键角的大小并解释原因③
 中
中 与
与 、
、 与
与 的作用力类型分别是
的作用力类型分别是(5)
 晶体的晶胞形状为立方体,边长为a nm,结构如图2。
晶体的晶胞形状为立方体,边长为a nm,结构如图2。
 的摩尔质量为
的摩尔质量为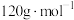 ,阿伏加德罗常数为
,阿伏加德罗常数为 。该晶体的密度为
。该晶体的密度为 。(
。(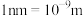 )
)
您最近一年使用:0次
名校
3 . 下列关于同分异构体数目的叙述不正确的是
| A.甲苯苯环上的1个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B.已知丙烷的二氯代物有4种同分异构体,则其六氯代物的同分异构体数目也为4种 |
C.菲的结构为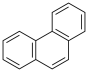 ,它与硝酸反应可生成5种一硝基取代物 ,它与硝酸反应可生成5种一硝基取代物 |
D.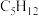 的一氯代物有3种 的一氯代物有3种 |
您最近一年使用:0次
名校
解题方法
4 . 利用甲烷可以除去 ,反应为
,反应为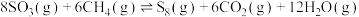 。下列说法正确的是
。下列说法正确的是
 ,反应为
,反应为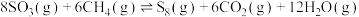 。下列说法正确的是
。下列说法正确的是A.上述反应的 |
B.上述反应的化学平衡常数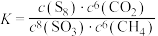 |
C.及时分离出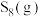 ,正反应速率增大,平衡向正反应方向移动 ,正反应速率增大,平衡向正反应方向移动 |
D.上述反应中生成1mol  ,转移电子的数目约为 ,转移电子的数目约为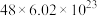 |
您最近一年使用:0次
5 . 下列有关硫及其化合物的性质与用途具有对应关系的是
| A.硫单质呈黄色,可用作橡胶硫化剂 |
B. 具有还原性,可用于漂白草编织物 具有还原性,可用于漂白草编织物 |
C. 具有还原性,可用于处理自来水中残留的 具有还原性,可用于处理自来水中残留的 |
| D.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
您最近一年使用:0次
名校
解题方法
6 .  易水解、易升华,是有机反应中常用的催化剂。实验室用如下图所示装置制备少量
易水解、易升华,是有机反应中常用的催化剂。实验室用如下图所示装置制备少量 。下列说法不正确的是
。下列说法不正确的是
 易水解、易升华,是有机反应中常用的催化剂。实验室用如下图所示装置制备少量
易水解、易升华,是有机反应中常用的催化剂。实验室用如下图所示装置制备少量 。下列说法不正确的是
。下列说法不正确的是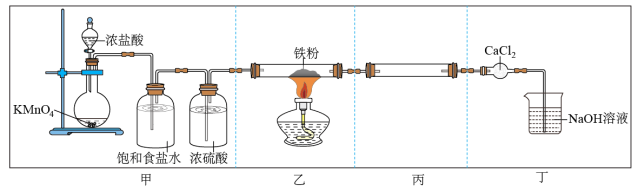
| A.实验开始,先滴加浓盐酸,再点燃酒精灯 | B.实验时若 不足量,则可能生成 不足量,则可能生成 |
C.装置丙的作用是收集 | D.装置丁中 的作用是防止水蒸气进入玻璃管 的作用是防止水蒸气进入玻璃管 |
您最近一年使用:0次
名校
解题方法
7 . 黑火药是中国古代四大发明之一。爆炸反应为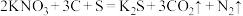 。下列说法不正确的是
。下列说法不正确的是
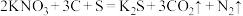 。下列说法不正确的是
。下列说法不正确的是A. 含离子键和共价键 含离子键和共价键 | B. 与 与 具有相同的电子层结构 具有相同的电子层结构 |
C. 的结构式为 的结构式为 | D.干冰的晶体类型为分子晶体 |
您最近一年使用:0次
名校
8 . 春季早晚温差大,空气中花粉多,是湿疹的高发季节,本维莫德(G)是治疗湿疹的非激素类外用药,其合成路线如下:______ 。
(2)下列有关说法正确的是______ 。
Ⅰ.B物质核磁共振氢谱有3组吸收峰,其峰面积之比为1∶1∶2;
Ⅱ.1mol A最多可以与1mol的 反应,最多可以消耗3mol的
反应,最多可以消耗3mol的 反应;
反应;
Ⅲ.1mol A中含有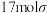 键,室温下,在水中的溶解度A比B大;
键,室温下,在水中的溶解度A比B大;
Ⅳ.G物质与足量 加成产物中有4个手性碳原子,G物质中C原子的杂化类型:
加成产物中有4个手性碳原子,G物质中C原子的杂化类型: 。
。
(3)合成路线中设置A到B,将A中酚羟基变为醚键的目的是____________ 。
(4)Y的分子式为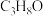 ,其结构简式为
,其结构简式为____________ ,欲确定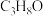 中存在C—O和O—H化学键,可采取的仪器分析方法为
中存在C—O和O—H化学键,可采取的仪器分析方法为______ (填选项)。
A.核磁共振氢谱 B.质谱 C.红外光谱 D.原子发射光谱
(5)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式____________ 。
Ⅰ.碱性条件下水解后酸化生成两种产物。
Ⅱ.一种产物含有苯环,其核磁共振氢谱只有3组峰,且峰面积之比为1∶2∶1,不能与 溶液显色;
溶液显色;
Ⅲ.另一种产物能与银氨溶液反应,被氧化为碳酸后分解生成二氧化碳和水。
(6)写出以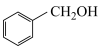 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图______________ (须用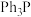 ,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
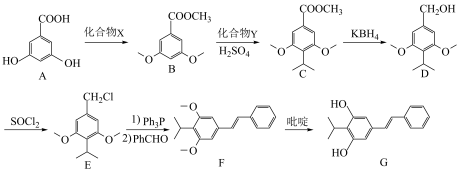
其中:—Ph为苯基(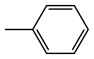 )。
)。
(2)下列有关说法正确的是
Ⅰ.B物质核磁共振氢谱有3组吸收峰,其峰面积之比为1∶1∶2;
Ⅱ.1mol A最多可以与1mol的
 反应,最多可以消耗3mol的
反应,最多可以消耗3mol的 反应;
反应;Ⅲ.1mol A中含有
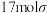 键,室温下,在水中的溶解度A比B大;
键,室温下,在水中的溶解度A比B大;Ⅳ.G物质与足量
 加成产物中有4个手性碳原子,G物质中C原子的杂化类型:
加成产物中有4个手性碳原子,G物质中C原子的杂化类型: 。
。(3)合成路线中设置A到B,将A中酚羟基变为醚键的目的是
(4)Y的分子式为
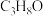 ,其结构简式为
,其结构简式为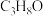 中存在C—O和O—H化学键,可采取的仪器分析方法为
中存在C—O和O—H化学键,可采取的仪器分析方法为A.核磁共振氢谱 B.质谱 C.红外光谱 D.原子发射光谱
(5)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
Ⅰ.碱性条件下水解后酸化生成两种产物。
Ⅱ.一种产物含有苯环,其核磁共振氢谱只有3组峰,且峰面积之比为1∶2∶1,不能与
 溶液显色;
溶液显色;Ⅲ.另一种产物能与银氨溶液反应,被氧化为碳酸后分解生成二氧化碳和水。
(6)写出以
 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图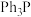 ,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
名校
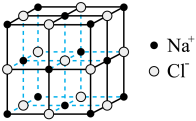
9 . 下列有关说法正确的是
A. 是由非极性共价键形成的极性分子 是由非极性共价键形成的极性分子 |
B.二氯化二硫 分子结构和 分子结构和 类似 类似 |
C. 和 和 的中心原子杂化轨道类型分别为 的中心原子杂化轨道类型分别为 和 和 |
D. 晶胞中氯离子周围最近且等距离的氯离子数为6 晶胞中氯离子周围最近且等距离的氯离子数为6 |
您最近一年使用:0次
名校
10 . 研究 、
、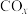 的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。
的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。
(1)采用 作还原剂催化还原
作还原剂催化还原 可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为:
可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为: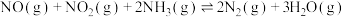 。以下说法正确的是______。
。以下说法正确的是______。
(2)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应用Rh做催化剂时该反应的过程示意图如图所示:__________ 。(填“极性键”、“非极性键”或“极性键和非极性键”)。过程Ⅱ为__________ 过程(填“吸热”或“放热”)。
②已知过程Ⅰ的焓变为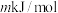 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为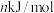 ,则该反应的热化学方程式为:
,则该反应的热化学方程式为:__________ 。
(3) 催化还原NO的物质转化如图所示。若参与反应的
催化还原NO的物质转化如图所示。若参与反应的 和
和 的物质的量之比为4∶1,则转化时
的物质的量之比为4∶1,则转化时 和NO物质的量之比为:
和NO物质的量之比为:__________ 。其中__________ 是催化剂(填化学符号)。______ (填选项)。(A.化学能转化为电能 B.电能转化为化学能),石墨Ⅰ是该电化学装置的______ (填选项)(A.正极 B.负极)石墨Ⅰ电极上发生的电极反应为__________ (提醒:介质为熔融 )。相同条件下,放电过程中消耗的
)。相同条件下,放电过程中消耗的 和
和 的体积比为
的体积比为__________ 。
 、
、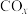 的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。
的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。(1)采用
 作还原剂催化还原
作还原剂催化还原 可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为:
可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为: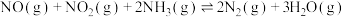 。以下说法正确的是______。
。以下说法正确的是______。A.使用催化剂更有利于提高 的平衡转化率 的平衡转化率 |
| B.及时吹脱水蒸气,可以提高脱氮率 |
| C.其他条件不变的条件下,改变压强对脱氮率没有影响 |
| D.烟气通过催化剂的流速越快,脱氮效果会越好 |
(2)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应用Rh做催化剂时该反应的过程示意图如图所示:

②已知过程Ⅰ的焓变为
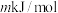 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为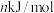 ,则该反应的热化学方程式为:
,则该反应的热化学方程式为:(3)
 催化还原NO的物质转化如图所示。若参与反应的
催化还原NO的物质转化如图所示。若参与反应的 和
和 的物质的量之比为4∶1,则转化时
的物质的量之比为4∶1,则转化时 和NO物质的量之比为:
和NO物质的量之比为: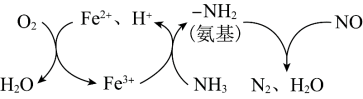
 )。相同条件下,放电过程中消耗的
)。相同条件下,放电过程中消耗的 和
和 的体积比为
的体积比为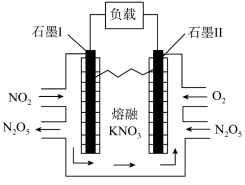
您最近一年使用:0次



