名校
解题方法
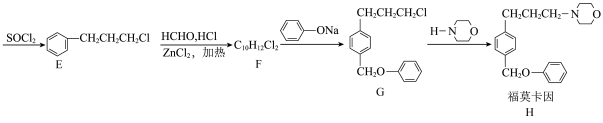
1 . 局部麻醉药福莫卡因的一种合成路线如下:
(1)C中所含官能团名称:___________ 。
(2)A与溴的四氯化碳溶液反应的产物名称:___________ 。
(3)B→C的反应方程式为:___________ 。
(4)D→E的反应类型为:___________ 。
(5)F的结构简式为:___________ 。
(6)F互为同分异构体之一X,满足条件①含有苯环②核磁共振氢谱只有1组吸收峰,则X的结构简式为:___________ 。(任写一种)
(7)G→H的反应方程式为:___________ 。

(1)C中所含官能团名称:
(2)A与溴的四氯化碳溶液反应的产物名称:
(3)B→C的反应方程式为:
(4)D→E的反应类型为:
(5)F的结构简式为:
(6)F互为同分异构体之一X,满足条件①含有苯环②核磁共振氢谱只有1组吸收峰,则X的结构简式为:
(7)G→H的反应方程式为:
您最近一年使用:0次
名校
解题方法
2 . 环己烯是有机合成的一种重要的化工原料。醇脱水是合成烯烃的常用方法,某实验小组以环己醇合成环己烯的制备流程如下:
Ⅰ.环己烯的制备与提纯
(1)操作1的装置如图所示。(加热和夹持装置已略去)
①A处所选仪器为___________ 。
A.蛇形冷凝管 B.球形冷凝管 C.直形冷凝管
②烧瓶B中进行的反应也可以用浓硫酸做催化剂,请写出在浓硫酸催化下制备环己烯的化学反应方程式:___________ 。该实验在选择催化剂时,选用 而不用浓硫酸的原因为
而不用浓硫酸的原因为___________ 。(写出一条合理即可)
③该实验在制备环己烯时,可能会生成的副产物为___________ 。(写出一个即可)
④操作1中装置韦氏分馏柱的作用为___________ 。
(2)操作2的名称为___________ 。
(3)操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和碎瓷片,___________ (填序号);弃去前馏分,收集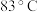 的馏分,当蒸馏结束后
的馏分,当蒸馏结束后___________ (填序号)。
A. 先通冷凝水,再加热 B. 先加热,再通冷凝水
C. 先撤掉酒精灯,再关闭冷凝水 D. 先关闭冷凝水,再撤掉酒精灯
(4)饱和食盐水的作用___________。
Ⅱ.环己烯的性质及含量的测定
(5)实验中,参加反应的环己醇的质量为 ,最终通过操作3蒸馏得到纯净环己烯为
,最终通过操作3蒸馏得到纯净环己烯为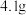 。本实验制得的环己烯的产率为
。本实验制得的环己烯的产率为___________ 。(结果精确至1%)

Ⅰ.环己烯的制备与提纯
(1)操作1的装置如图所示。(加热和夹持装置已略去)

①A处所选仪器为
A.蛇形冷凝管 B.球形冷凝管 C.直形冷凝管
②烧瓶B中进行的反应也可以用浓硫酸做催化剂,请写出在浓硫酸催化下制备环己烯的化学反应方程式:
 而不用浓硫酸的原因为
而不用浓硫酸的原因为③该实验在制备环己烯时,可能会生成的副产物为
④操作1中装置韦氏分馏柱的作用为
(2)操作2的名称为
(3)操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和碎瓷片,
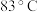 的馏分,当蒸馏结束后
的馏分,当蒸馏结束后A. 先通冷凝水,再加热 B. 先加热,再通冷凝水
C. 先撤掉酒精灯,再关闭冷凝水 D. 先关闭冷凝水,再撤掉酒精灯
(4)饱和食盐水的作用___________。
| A.增大水层密度,加速有机相与水相分层 |
| B.降低环己烯在水中的溶解度,便于分离 |
| C.洗涤,除去环己烯中的杂质 |
| D.增大环己烯在水中的溶解度,便于分离 |
Ⅱ.环己烯的性质及含量的测定
(5)实验中,参加反应的环己醇的质量为
 ,最终通过操作3蒸馏得到纯净环己烯为
,最终通过操作3蒸馏得到纯净环己烯为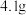 。本实验制得的环己烯的产率为
。本实验制得的环己烯的产率为
您最近一年使用:0次
名校
解题方法
3 . 按要求回答下列问题:
对甲氧基苯丙酰胺(相对分子质量为179)为难溶于冷水的白色晶体,且是一种医药中间体,可以由苯甲醚通过两步反应合成,合成路线如图1所示。
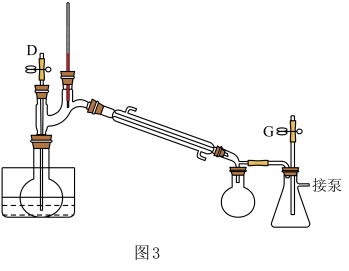
步骤一:用如图2所示装置合成对甲氧基苯丙腈
在500 mL三颈烧瓶中,加入108 g(1 mol)苯甲醚,室温下缓慢加入70 g(约0.52 mol)粉末状三氯化铝,加入过程中温度不超过25℃,加完后降温至5℃,然后逐滴加入130 g(约2.45 mol)丙烯腈(沸点77℃),滴加结束后再升温至90~95℃,反应2 h。将反应液倒入500 g冰水中,搅匀,静置分层,分出油相。减压蒸馏,收集2.67 kPa下150~160℃的馏分,得到对甲氧基苯丙腈。
步骤二:合成对甲氧基苯丙酰胺
将步骤一中合成的对甲氧基苯丙腈加入500 mL三颈烧瓶中,加入300 mL浓盐酸,再经过一系列操作后得到对甲氧基苯丙酰胺133.7 g。
(1)苯甲醚生成对甲氧基苯丙腈的反应类型为________________ 。
(2)对甲氧基苯丙腈的合成过程中宜采用的加热方式为________________ ,采取减压蒸馏收集对甲氧基苯丙腈的优点是________________________ 。
(3)图2中合成对甲氧基苯丙腈的装置有一缺陷,请提出改进方法并说明理由:________ 。
(4)用恒压滴液漏斗加丙烯腈的优点有________________ 、________________ (写出两条)。
(5)下列操作为合成对甲氧基苯丙酰胺的过程中加浓盐酸后的一系列操作,其合理顺序为__________ 。
①加入活性炭回流0.5 h ②趁热过滤 ③抽滤 ④升温至40~50℃,搅拌1 h ⑤将滤液慢慢倒入1000 g冷水中,析出晶体 ⑥洗涤、烘干
(6)下列关于实验操作的说法错误的是__________ 。
B.在对甲氧基苯丙酰胺的合成过程中,析出的晶体可以用冷水洗涤
C.减压过滤不宜用于过滤颗粒太小的沉淀,因为颗粒太小的沉淀在快速过滤时易透过滤纸
(7)本实验中对甲氧基苯丙酰胺的产率为________________________ %(保留两位小数)。
对甲氧基苯丙酰胺(相对分子质量为179)为难溶于冷水的白色晶体,且是一种医药中间体,可以由苯甲醚通过两步反应合成,合成路线如图1所示。
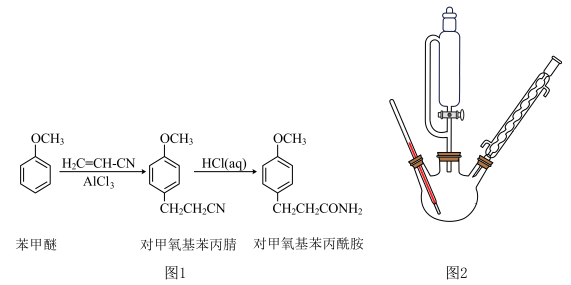
步骤一:用如图2所示装置合成对甲氧基苯丙腈
在500 mL三颈烧瓶中,加入108 g(1 mol)苯甲醚,室温下缓慢加入70 g(约0.52 mol)粉末状三氯化铝,加入过程中温度不超过25℃,加完后降温至5℃,然后逐滴加入130 g(约2.45 mol)丙烯腈(沸点77℃),滴加结束后再升温至90~95℃,反应2 h。将反应液倒入500 g冰水中,搅匀,静置分层,分出油相。减压蒸馏,收集2.67 kPa下150~160℃的馏分,得到对甲氧基苯丙腈。
步骤二:合成对甲氧基苯丙酰胺
将步骤一中合成的对甲氧基苯丙腈加入500 mL三颈烧瓶中,加入300 mL浓盐酸,再经过一系列操作后得到对甲氧基苯丙酰胺133.7 g。
(1)苯甲醚生成对甲氧基苯丙腈的反应类型为
(2)对甲氧基苯丙腈的合成过程中宜采用的加热方式为
(3)图2中合成对甲氧基苯丙腈的装置有一缺陷,请提出改进方法并说明理由:
(4)用恒压滴液漏斗加丙烯腈的优点有
(5)下列操作为合成对甲氧基苯丙酰胺的过程中加浓盐酸后的一系列操作,其合理顺序为
①加入活性炭回流0.5 h ②趁热过滤 ③抽滤 ④升温至40~50℃,搅拌1 h ⑤将滤液慢慢倒入1000 g冷水中,析出晶体 ⑥洗涤、烘干
(6)下列关于实验操作的说法错误的是
B.在对甲氧基苯丙酰胺的合成过程中,析出的晶体可以用冷水洗涤
C.减压过滤不宜用于过滤颗粒太小的沉淀,因为颗粒太小的沉淀在快速过滤时易透过滤纸
(7)本实验中对甲氧基苯丙酰胺的产率为
您最近一年使用:0次
名校
4 . 按要求填空
(1)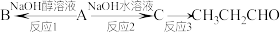
①反应1的反应类型___________ 。
②物质B的名称___________ 。
③反应3的条件___________ 。
(2)某有机物结构如下图所示,分子中处于同一直线的碳原子最多有___________ 个, 该烃与氢气反应最多消耗
该烃与氢气反应最多消耗___________ mol氢气。 ,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:
,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:___________ 。
(4)分子式为 且属于芳香族化合物的同分异构体有
且属于芳香族化合物的同分异构体有___________ 种。
(5)BN晶体的晶胞如下图,已知B原子半径为 ,N原子半径为
,N原子半径为 ,BN属于
,BN属于___________ 晶体,试表示BN晶体的空间利用率计算式___________ 。
(1)
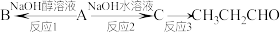
①反应1的反应类型
②物质B的名称
③反应3的条件
(2)某有机物结构如下图所示,分子中处于同一直线的碳原子最多有
 该烃与氢气反应最多消耗
该烃与氢气反应最多消耗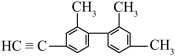
 ,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:
,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:(4)分子式为
 且属于芳香族化合物的同分异构体有
且属于芳香族化合物的同分异构体有(5)BN晶体的晶胞如下图,已知B原子半径为
 ,N原子半径为
,N原子半径为 ,BN属于
,BN属于
您最近一年使用:0次
名校
解题方法
5 . 研究含氮元素物质的反应对生产、生活、科研等方面都具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:① (1)
(1) 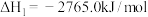
②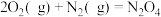 (1)
(1) 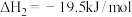
③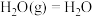 (1)
(1) 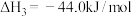
则反应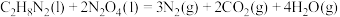 的
的 为
为________________ 。
(2)一种工业制硝酸的方法经历下列几个步骤:

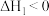
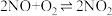
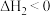

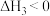
已知:NO在1000℃以上会发生分解反应。
①工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了给原料气预热节约能源之外,还有________________ ;
②实验发现,单位时间内NH3的氧化率 会随着温度的升高先增大后减小(如下图所示),分析出现这种变化的可能原因
会随着温度的升高先增大后减小(如下图所示),分析出现这种变化的可能原因________________________________________________ 。 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
①有关该过程说法正确的是________________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B点操作是向里快速推注射器活塞,E点操作是向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②求D点
________________ 。
③图像中C、E两点气体平均摩尔质量最大的点为________________ (填代号)。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①
 (1)
(1) 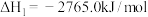
②
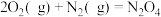 (1)
(1) 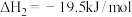
③
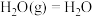 (1)
(1) 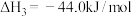
则反应
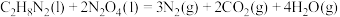 的
的 为
为(2)一种工业制硝酸的方法经历下列几个步骤:

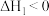
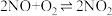
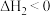

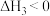
已知:NO在1000℃以上会发生分解反应。
①工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了给原料气预热节约能源之外,还有
②实验发现,单位时间内NH3的氧化率
 会随着温度的升高先增大后减小(如下图所示),分析出现这种变化的可能原因
会随着温度的升高先增大后减小(如下图所示),分析出现这种变化的可能原因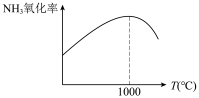
 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。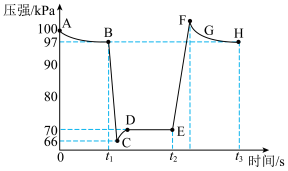
①有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B点操作是向里快速推注射器活塞,E点操作是向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②求D点

③图像中C、E两点气体平均摩尔质量最大的点为
您最近一年使用:0次
名校
解题方法
6 . 从海带中提取精品甘露醇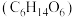 的流程如下,甘露醇是一种糖醇,易溶于水,且溶解度随温度的升高而增大,随乙醇的含量增大而骤减。下列说法正确的是
的流程如下,甘露醇是一种糖醇,易溶于水,且溶解度随温度的升高而增大,随乙醇的含量增大而骤减。下列说法正确的是
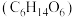 的流程如下,甘露醇是一种糖醇,易溶于水,且溶解度随温度的升高而增大,随乙醇的含量增大而骤减。下列说法正确的是
的流程如下,甘露醇是一种糖醇,易溶于水,且溶解度随温度的升高而增大,随乙醇的含量增大而骤减。下列说法正确的是
| A.为了提高甘露醇的提取效率,预处理时可以将海带灼烧成海带灰后再用水浸泡 |
| B.浓缩液中所加入的乙醇的作用是为了萃取甘露醇,且浓度越大越好 |
| C.浓缩和过滤操作都要用到玻璃棒,且作用相同 |
| D.操作①是降温冷却,粗品甘露醇经重结晶后析出 |
您最近一年使用:0次
名校
解题方法
7 . 下列有机物的命名正确的是
A.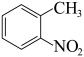 2-氨基甲苯 2-氨基甲苯 | B.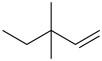 3,3-二甲基-1-戊烯 3,3-二甲基-1-戊烯 |
C. 2-乙基-1-氯乙烷 2-乙基-1-氯乙烷 | D.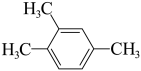 1,3,4-三甲苯 1,3,4-三甲苯 |
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语的使用正确的是
| A.氮化硅与金刚石结构相似,其分子式为:Si3N4 |
B.CH4分子的空间填充模型: |
C.HClO的电子式为 |
| D.乙炔的结构简式为CHCH |
您最近一年使用:0次
名校
解题方法
9 . 下列物质既能使酸性 溶液褪色,又能使溴的四氯化碳溶液因发生反应而褪色的是
溶液褪色,又能使溴的四氯化碳溶液因发生反应而褪色的是
 溶液褪色,又能使溴的四氯化碳溶液因发生反应而褪色的是
溶液褪色,又能使溴的四氯化碳溶液因发生反应而褪色的是①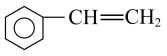 ②
②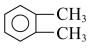 ③
③ ④
④ ⑤
⑤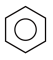 ⑥聚乙炔
⑥聚乙炔
| A.①②⑥ | B.②④⑥ | C.①③⑥ | D.①②④ |
您最近一年使用:0次
名校
解题方法
10 . 关同分异构体数目的判断错误的是
| A.异丁烷的二溴代物有3种 |
B.甲基环己烷(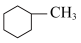 )的一氯代物有4种 )的一氯代物有4种 |
C.炔烃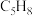 的同分异构体有3种 的同分异构体有3种 |
D.分子式为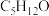 且能被氧化成醛的同分异构体有4种 且能被氧化成醛的同分异构体有4种 |
您最近一年使用:0次



