名校
解题方法
1 . 下列化学用语正确的是
A.-CH3的电子式: | B.丙烯的键线式: |
C.硝基苯的结构简式: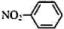 | D.铁原子价电子排布式3d54s2 |
您最近一年使用:0次
名校
解题方法
2 . 分子式为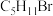 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
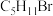 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)| A.3种 | B.2种 | C.5种 | D.4种 |
您最近一年使用:0次
名校
解题方法
3 . 秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料,直到近年来人们才研究出来其成分为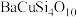 ,
,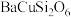 。试回答下列问题:
。试回答下列问题:
(1)“中国蓝”、“中国紫”中均具有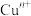 离子,
离子,
______ ,基态时该阳离子的价电子排布式为______ ,“中国蓝”的发色中心是以 为中心的配位化合物,形成该配位键,
为中心的配位化合物,形成该配位键, 提供
提供______ 。
(2)合成“中国蓝”、“中国紫”的原料有 、孔雀石[
、孔雀石[ ]和砂子(
]和砂子( )。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是
)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是______ 。
(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料——“埃及蓝”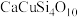 ,其合成原料中用
,其合成原料中用 代替了
代替了 ,其他和“中国蓝”一致。
,其他和“中国蓝”一致。 中键角为
中键角为______ 。从原料分解的角度判断,“埃及蓝”的合成温度比“中国蓝”更低,这是因为 比
比 更易形成。根据所学,试解释:
更易形成。根据所学,试解释:______ 。
(4) 和
和 同主族,但
同主族,但 与
与 的熔沸点差异很大,这是因为
的熔沸点差异很大,这是因为______ 。
(5)现代工业利用铜氨溶液溶解纤维制造人造丝。金属铜与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生反应得到深蓝色铜氨溶液,写出离子方程式:______ 。
(6)氯化亚铜的晶胞结构如图所示。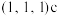 点坐标为
点坐标为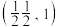 ,则b点的坐标为
,则b点的坐标为______ 。
②设 为阿伏加德罗常数的值,晶胞边长为
为阿伏加德罗常数的值,晶胞边长为 ,则该晶体的密度
,则该晶体的密度
______  (列出计算式即可)。
(列出计算式即可)。
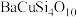 ,
,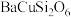 。试回答下列问题:
。试回答下列问题:(1)“中国蓝”、“中国紫”中均具有
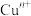 离子,
离子,
 为中心的配位化合物,形成该配位键,
为中心的配位化合物,形成该配位键, 提供
提供(2)合成“中国蓝”、“中国紫”的原料有
 、孔雀石[
、孔雀石[ ]和砂子(
]和砂子( )。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是
)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料——“埃及蓝”
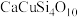 ,其合成原料中用
,其合成原料中用 代替了
代替了 ,其他和“中国蓝”一致。
,其他和“中国蓝”一致。 中键角为
中键角为 比
比 更易形成。根据所学,试解释:
更易形成。根据所学,试解释:(4)
 和
和 同主族,但
同主族,但 与
与 的熔沸点差异很大,这是因为
的熔沸点差异很大,这是因为(5)现代工业利用铜氨溶液溶解纤维制造人造丝。金属铜与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生反应得到深蓝色铜氨溶液,写出离子方程式:
(6)氯化亚铜的晶胞结构如图所示。
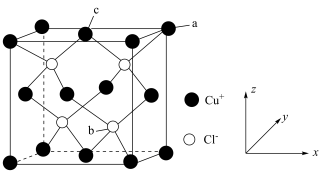
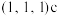 点坐标为
点坐标为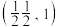 ,则b点的坐标为
,则b点的坐标为②设
 为阿伏加德罗常数的值,晶胞边长为
为阿伏加德罗常数的值,晶胞边长为 ,则该晶体的密度
,则该晶体的密度
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
4 . 左氧氟沙星是一种广谱抗菌药物,其结构简式如图,则对左氧氟沙星说法正确的是

A.分子式为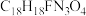 |
| B.左氧氟沙星含有3种含氧官能团 |
C.该有机物能使 溶液、溴水褪色,原理相同 溶液、溴水褪色,原理相同 |
D. 左氧氟沙星和足量 左氧氟沙星和足量 反应生成 反应生成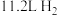 |
您最近一年使用:0次
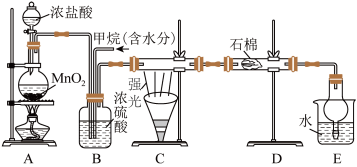
5 . 美国宇航局科学家确认火星大气中存在甲烷气体,可能来自火星火山活动或者生命活动,这一发现将为寻找火星生命带来希望。某课外活动小组利用如图所示装置探究烃类物质的性质,根据题意,回答下列问题:
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。______ 。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③______ 。
(3)写出装置C中 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式____________ 。
(4)装置D的石棉浸有足量 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是______ 。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法______ (填“正确”或“不正确”),理由是______ 。
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为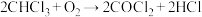 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是______ 。
A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为____________ 。
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是____________ 。
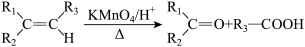
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:______ 。
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③
(3)写出装置C中
 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式(4)装置D的石棉浸有足量
 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
| A.结晶法 | B.蒸馏法 | C.萃取分液法 | D.水洗分液法 |
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为
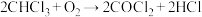 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
您最近一年使用:0次
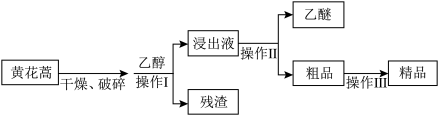
6 . 我国科学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔医学奖。青蒿素是烃的含氧衍生物,为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青素是高效的抗疟药。已知:乙醚沸点为35℃,与水不互溶,从黄花蒿中提取青蒿素的方法是乙醚浸取法,主要工艺流程为:
(1)先对黄花蒿进行干燥破碎后再加入乙醚的目的是______ 。
(2)操作Ⅰ的名称是______ ,操作Ⅱ的名称是______ ,既可以回收乙醚,又可以使提取液浓缩结晶,再经过滤可得到青蒿素粗品。操作Ⅲ的主要过程可能包括______ (填序号)。
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(3)用如图实验装置测定青蒿素实验式的方法如下:将一定质量的青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。______ ,装置D的作用是______ 。
②装置E、F中盛放的物质是分别是______ 。
a.碱石灰、无水氯化钙 b.浓硫酸、碱石灰 c.无水氯化钙、碱石灰
③某同学认为上述装置存在不足之处,请你指出该问题并提出改进的措施:______ 。
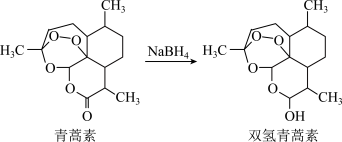
(4)科学家在青蒿素的研究中进一步发现,一定条件下可把青蒿素转化为双氢青蒿素______ 。
a.通过元素分析与质谱法可确定其分子式
b.青蒿素是芳香族化合物
c.青蒿素分子中含有过氧键、酯基和醚键
d.古有“青蒿一握,以水二升溃,绞取汁”,利用的是萃取原理
②双氢青蒿素比青蒿素水溶性更好,因而疗效更好。从结构与性质关系角度推测主要原因是______ 。
(1)先对黄花蒿进行干燥破碎后再加入乙醚的目的是
(2)操作Ⅰ的名称是
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%的乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(3)用如图实验装置测定青蒿素实验式的方法如下:将一定质量的青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
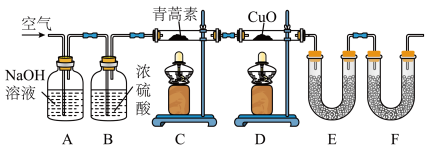
②装置E、F中盛放的物质是分别是
a.碱石灰、无水氯化钙 b.浓硫酸、碱石灰 c.无水氯化钙、碱石灰
③某同学认为上述装置存在不足之处,请你指出该问题并提出改进的措施:
(4)科学家在青蒿素的研究中进一步发现,一定条件下可把青蒿素转化为双氢青蒿素
a.通过元素分析与质谱法可确定其分子式
b.青蒿素是芳香族化合物
c.青蒿素分子中含有过氧键、酯基和醚键
d.古有“青蒿一握,以水二升溃,绞取汁”,利用的是萃取原理
②双氢青蒿素比青蒿素水溶性更好,因而疗效更好。从结构与性质关系角度推测主要原因是
您最近一年使用:0次
7 . 实验室提纯以下物质(括号内为杂质),所选用的除杂试剂和分离方法都正确的是
被提纯的物质 | 除杂试剂 | 分离方法 | |
A | 乙炔( | 酸性高锰酸钾溶液 | 洗气 |
B | 环己烷(环己烯) | 溴水 | 洗涤,分液 |
C | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
D | 戊烷(溴) | 氢氧化钠溶液 | 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 化学与科技、生活密切相关,下列说法正确的是
A.航天器使用的太阳能电池帆板的主要成分是 |
| B.通过红外光谱仪可以测定分子的相对分子质量 |
| C.可以用光谱分析的方法来确定太阳的组成元素是否含He |
| D.焰火、激光都与原子核外电子跃迁吸收能量有关 |
您最近一年使用:0次
解题方法
9 . 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。其材料除单晶硅外,还有铜、铟、镓、硒的化合物。
(1)镓的基态原子的核外电子排布式为___________ 。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的第一电离能从大到小顺序为___________ (用元素符号表示)。
(3)气态SeO3的空间结构为___________ 。
(4)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,则[B(OH)4]-中B原子的杂化类型为___________ ,该离子___________ (填“含有”或“不含有”)配位键,其空间结构是___________ 。
(5)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为___________ ,用价层电子对互斥模型分析,NH3分子和H2O分子的空间结构分别是___________ 、___________ 。
(1)镓的基态原子的核外电子排布式为
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的第一电离能从大到小顺序为
(3)气态SeO3的空间结构为
(4)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,则[B(OH)4]-中B原子的杂化类型为
(5)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为
您最近一年使用:0次
解题方法
10 . 一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)本题所涉及的物质中,只含极性键的非极性分子为_______ 。
a.CH2O b.CO2 c.CO d.H2Oe.Na2CO3
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O.
①写出一种与CO分子互为等电子体的离子(只由一种元素构成)的化学式________ 。
②HCHO分子中C原子轨道的杂化类型为_______ 。
③1mol CO2中含有的σ键数目为____________ 。
(3)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4.
①Mn2+基态的外围电子排布图可表示为_______ 。
② 的空间构型是
的空间构型是_______ 。
(1)本题所涉及的物质中,只含极性键的非极性分子为
a.CH2O b.CO2 c.CO d.H2Oe.Na2CO3
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O.
①写出一种与CO分子互为等电子体的离子(只由一种元素构成)的化学式
②HCHO分子中C原子轨道的杂化类型为
③1mol CO2中含有的σ键数目为
(3)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4.
①Mn2+基态的外围电子排布图可表示为
②
 的空间构型是
的空间构型是
您最近一年使用:0次

 )
)

