名校
1 . 在一定条件下,有下列分子数之比相同的可逆反应,其平衡常数K值分别是①H2+F2⇌2HF K=1047; ②H2+Cl2⇌2HCl K=1017;③H2+Br2⇌2HBr K=109; ④H2+I2⇌2HI K=1。比较K值大小,可知各反应的正反应进行的程度由大到小的顺序是
| A.①④③② | B.④②③① | C.①②③④ | D.无法确定 |
您最近一年使用:0次
2022-10-05更新
|
194次组卷
|
11卷引用:陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)
陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科) 陕西省咸阳市武功县2021--2022学年高二上学期质量调研化学试题四川省阆中中学2017-2018学年高二下学期第一次月考化学试题甘肃省陇南市徽县第三中学2020-2021学年高二上学期期末考试化学试题(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第09讲 化学平衡常数(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河南省濮阳市元龙高级中学2021-2022学年高二下学期第一次质量检测化学试题北京市首都师范大学附属密云中学2022-2023学年高二上学期10月阶段性练习化学试题海南省三亚华侨学校(南新校区)2021-2022学年高二上学期期中考试化学试题作业(十) 化学平衡常数平衡转化率(已下线)第3讲 化学平衡计算 平衡常数
11-12高二下·福建·阶段练习
名校
解题方法
2 . 为了配制 浓度与
浓度与 浓度比为
浓度比为 的溶液,可在
的溶液,可在 溶液中加入
溶液中加入
①适量的HCl ②适量的NaCl ③适量的氨水 ④适量的NaOH
 浓度与
浓度与 浓度比为
浓度比为 的溶液,可在
的溶液,可在 溶液中加入
溶液中加入①适量的HCl ②适量的NaCl ③适量的氨水 ④适量的NaOH
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
2022-02-20更新
|
214次组卷
|
35卷引用:陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)
陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)2015-2016学年陕西省黄陵中学高二上学期期末考试化学试卷陕西省吴起高级中学2019-2020学年高二上学期第一次月考(能力卷)化学试题(已下线)2011-2012学年福建省四地六校高二下学期第一次联考化学试卷(已下线)2012年苏教版高中化学选修4 3.3盐类的水解练习卷(已下线)2012-2013学年四川省雅安中学高二下学期期中考试化学试卷2014-2015云南省玉溪第一中学高二上学期期末考试化学试卷2014-2015四川省德阳市第五中学高二下学期第一次月考化学试卷2014-2015学年四川省雅安中学高二下期末模拟化学试卷2015-2016学年甘肃省天水一中高二上学期第一次段中考试化学试卷2015-2016学年浙江省绍兴一中高二上期中测试化学试卷2015-2016学年广东省湛江市高二上学期期末质检化学试卷2015-2016学年四川省绵阳南山中学高二4月月考化学试卷2016-2017学年黑龙江省鸡西市第十九中学高二上学期期末考试化学试卷宁夏石嘴山市第三中学2016-2017学年高二下学期第二次(5月)月考化学试题河南省洛阳名校2017-2018学年高二上学期第二次联考化学试题黑龙江省大庆十中2018-2019学年高二上学期期末考试化学试题【全国百强校】贵州省铜仁市思南中学2018-2019学年高二上学期期末考试化学试题吉林省辽源市田家炳高级中学2019-2020学年高二12月月考化学试题黑龙江省大庆市第十中学2019-2020学年高二上学期期末考试化学试题甘肃省永昌四中2019-2020学年高二上学期期末考试化学试题黑龙江省牡丹江市穆棱市第一中学2019-2020学年高二上学期期末考试化学试题北京市第四中学2019-2020学年高二上学期期末考试化学试题福建省福清市龙西中学2018-2019学年高二下学期期中考试化学试题甘肃省张掖市第二中学2020-2021学年高二上学期期中考试化学试题四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题吉林省长春市第二实验中学2020-2021学年高二上学期期中考试化学试题江苏省苏州工业园区星海实验中学2019-2020学年高二下学期期中考试化学试卷福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题北京市平谷区2021-2022学年高二上学期期末化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期11月测试化学试题新疆乌苏市第一中学2021-2022学年高二12月月考化学试题四川省遂宁市第二中学校2021-2022学年高二下学期半期考试化学试题广东省深圳市龙华高级中学2022-2023学年高二上学期第二次段考化学试题2020届高三化学选修4二轮专题练——盐类水解章节强化【精编25题】
11-12高二上·广西桂林·期中
名校
3 . 在CH3COOH溶液中存在如下平衡:CH3COOH H++CH3COO-,加入少量下列固体物质能使平衡向左移动的是
H++CH3COO-,加入少量下列固体物质能使平衡向左移动的是
 H++CH3COO-,加入少量下列固体物质能使平衡向左移动的是
H++CH3COO-,加入少量下列固体物质能使平衡向左移动的是| A.NaCl | B.Na2CO3 | C.CH3COONa | D.NaOH |
您最近一年使用:0次
2021-01-19更新
|
211次组卷
|
11卷引用:陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)
陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)(已下线)2011-2012学年广西桂林十八中高二上学期期中考试化学(理)试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷2014-2015湖南省怀化市中小学课改高二上学期期末化学试卷安徽省滁州市定远县育才学校2019-2020学年高二上学期期中考试(普通班)化学试题宁夏回族自治区银川市长庆高级中学2019-2020学年高二上学期第二次月考化学试题西藏自治区日喀则市第三高级中学2019-2020学年高二上学期期末考试化学(理)试题甘肃省陇南市徽县第三中学2020-2021学年高二上学期期末考试化学试题甘肃省陇南市徽县第二中学2020-2021学年高二上学期期末考试化学试题山西省太原市行知宏实验中学校2020-2021学年高二上学期期末考试化学试题苏教2020版选择性必修1专题3第一单元 弱电解质的电离平衡课后习题
11-12高二下·浙江台州·期中
4 . 下列因素中,对发生在溶液中且无气体参加的反应的速率不产生显著影响的是
| A.浓度 | B.压强 | C.温度 | D.反应物的性质 |
您最近一年使用:0次
2019-06-23更新
|
99次组卷
|
9卷引用:陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)
陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)(已下线)2011-2012学年浙江临海市白云高级中学高二下学期期中考试化学卷(已下线)2012-2013学年福建福清东张中学高二上学期期中考试理科化学试卷2014-2015浙江省嘉兴一中高二上学期期中化学(文)试卷陕西省吴起高级中学2018-2019学年高一下学期期中考试基础题化学试题福建省福州市长乐高级中学2019-2020学年高二上学期第一次月考化学(学考)试题福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题福建省莆田第十五中学2018-2019学年高二上学期期末考试化学试题苏教2020版选择性必修1专题2第一单元 化学反应速率课后习题
5 . 如图所示,通电5min后,电极5的质量增加2.16g。假设电解过程中溶液的体积不变。
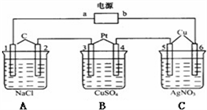
请回答下列问题:
(1)电源中a是_______ 极。A池中阳极的电极反应式为___________ ,C池中阴极的电极反应式为___________________________ 。
(2)通电5min后,如果B槽中共收集到224mL气体(标准状况),且溶液体积为200mL,则通电前溶液中Cu2+的物质的量浓度为___________________ 。
(3)如果A池溶液是200mL食盐水(假设电解液足量),则通电5min后,溶液的pH为__________ 。

请回答下列问题:
(1)电源中a是
(2)通电5min后,如果B槽中共收集到224mL气体(标准状况),且溶液体积为200mL,则通电前溶液中Cu2+的物质的量浓度为
(3)如果A池溶液是200mL食盐水(假设电解液足量),则通电5min后,溶液的pH为
您最近一年使用:0次
解题方法
6 . 常温下,将某一元酸HA溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表所示:
请回答下列问题:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?______________________
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol·L-1?________ (选填“是”或“否”)。
(3)从丙组实验结果分析,HA是________ (选填“强”或“弱”)酸。该混合溶液中离子浓度由大到小的顺序是______________________
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________ mol·L-1。
| 实验编号 | HA物质的量浓度 (mol·L-1) | NaOH物质的量浓度 (mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | c1 | 0.2 | 7 |
| 丙 | 0.2 | 0.1 | 7 |
| 丁 | 0.1 | 0.1 | 9 |
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol·L-1?
(3)从丙组实验结果分析,HA是
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
解题方法
7 . (1)常温下pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合溶液的pH=11,求强碱与强酸的体积比(溶液的体积变化忽略不计)是________________ 。
(2)取浓度相同的NaOH和HCl溶液,以3 :2体积比相混合,所得溶液的pH等于12,则该原溶液的浓度(溶液的体积变化忽略不计)为__________________ 。
(3)常温下,PH=11的NH3·H2O与PH=3的盐酸等体积混合,混合溶液中,离子浓度关系为_________________________________________ 。
(4)已知:Ksp(FeS)=6.5×10-18,Ksp(CuS)=1.3×10-36。向浓度均为0.1 mol·L-1的FeSO4和CuSO4的混合溶液中滴加Na2S溶液,当加入Na2S溶液至出现两种沉淀,则溶液中c(Fe2+) : c(Cu2+) =___________ 。
(2)取浓度相同的NaOH和HCl溶液,以3 :2体积比相混合,所得溶液的pH等于12,则该原溶液的浓度(溶液的体积变化忽略不计)为
(3)常温下,PH=11的NH3·H2O与PH=3的盐酸等体积混合,混合溶液中,离子浓度关系为
(4)已知:Ksp(FeS)=6.5×10-18,Ksp(CuS)=1.3×10-36。向浓度均为0.1 mol·L-1的FeSO4和CuSO4的混合溶液中滴加Na2S溶液,当加入Na2S溶液至出现两种沉淀,则溶液中c(Fe2+) : c(Cu2+) =
您最近一年使用:0次
11-12高二下·陕西宝鸡·期中
解题方法
8 . 煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
试回答下列问题:
(1)该反应的化学平衡常数表达式为K=______________________ 。
(2)上述正向反应是_________________ (填“放热”或“吸热”)反应。
(3)某温度下,上述反应达到平衡时,恒容、升高温度,原化学平衡向_________ (填“正”或“逆”)反应方向移动,正反应速率___________ (填“增大”“减小”或“不变”),容器内混合气体的压强_____________ (填“增大”“减小”或“不变”)。
(4)有830oC时发生上述反应,按下表中的物质的量投入恒容反应器,其中在向正反应方向进行的有____________ (选填A、B、C、D)。
已知:CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:| 温度/oC | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(1)该反应的化学平衡常数表达式为K=
(2)上述正向反应是
(3)某温度下,上述反应达到平衡时,恒容、升高温度,原化学平衡向
(4)有830oC时发生上述反应,按下表中的物质的量投入恒容反应器,其中在向正反应方向进行的有
| A | B | C | D | |
| n(CO2)/mol | 3 | 1 | 0 | 1 |
| n(H2)/mol | 2 | 1 | 0 | 1 |
| n(CO)/mol | 1 | 2 | 3 | 0.5 |
| n(H2O)/mol | 5 | 2 | 3 | 2 |
您最近一年使用:0次
9 . (1)根据氧化还原反应2H2+O2===2H2O,设计成燃料电池,负极通的气体应是___________ 。
(2)如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是_____ 。
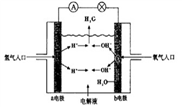
A.a电极是负极
B.b电极的电极反应为4OH--4e-====2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(3)根据氢氧燃料电池电解质溶液的不同,填写下表:
(4)若把H2改为CH4,KOH溶液作电解质溶液,则负极反应为_________________________________________ 。
(2)如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是

A.a电极是负极
B.b电极的电极反应为4OH--4e-====2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(3)根据氢氧燃料电池电解质溶液的不同,填写下表:
| 电解质溶液 | H2SO4溶液 | KOH溶液 |
| 负极反应 | ||
| 正极反应 | ||
| 溶液的pH变化 |
您最近一年使用:0次
10 . 水的电离过程为H2O H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
 H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是| A.在35℃时,纯水中c(H+)>c(OH-) | B.c(H+)随着温度的升高而降低 |
| C.水的电离过程是吸热过程 | D.水的电离度α(25℃)>α(35℃) |
您最近一年使用:0次
2018-03-28更新
|
256次组卷
|
2卷引用:陕西岐山县2017—2018学年度第一学期期末质量检测高二化学(理科)



