25. I.影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的H
2O溶液分别进行H
2O
2的分解实验,实验报告如下表所示(现象和结论略)。
| 序号 | 温度/℃ | 催化剂 | 现象 | 结论 |
| 1 | 40 | FeCl3溶液 | | |
| 2 | 20 | FeCl3溶液 | | |
| 3 | 20 | MnO2 | | |
| 4 | 20 | 无 | | |
①实验1、2研究的是
________________对H
2O
2分解速率的影响。
②实验2、3的目的是
________________。
(2)查文献可知:Cu
2+对H
2O
2分解也有催化作用,为比较Fe
3+、Cu
2+对H
2O
2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
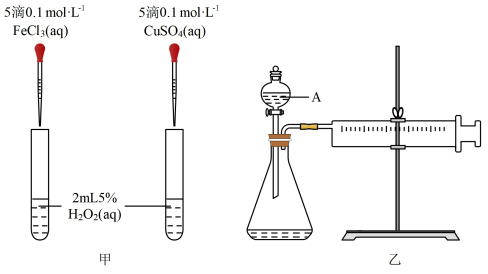
①定性性分析:如图甲可通过观察
__________,先定性比较得出结论。有同学提出将CuSO
4溶液改为CuCl
2溶液更合理,其理由是
__________。
②定量分析:如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是
____________ 。
II.化学兴趣小组的同学0.100 mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用分析天平准确称取烧碱样品2. 500 g,全部溶于水配制成500 mL溶液。配制溶液需用的玻璃仪器除了烧杯、胶头滴管外,还需要
__________(2)滴定:
①用碱式滴定管量取20.00 mL所配溶液放在锥形瓶中,滴加几滴指示剂,待测。滴定管在装入反应液之前应进行的操作有
___________ 。
②用浓度为0. 1000 mol/L 的盐酸标准溶液进行滴定。开始滴定前的一步操作是
____________。③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时每滴一滴测一次pH。滴定过程中,测得锥形瓶中溶液的pH变化如下表:
| V(HCI) /mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 |
| V(HCI) /mL | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 | |
| pH | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 | |
(3)数据处理:
所测样品中NaOH的质量百分含量为
____________。