名校
1 . 设 为阿伏加德罗常数的值,下列叙述中正确的是
为阿伏加德罗常数的值,下列叙述中正确的是
 为阿伏加德罗常数的值,下列叙述中正确的是
为阿伏加德罗常数的值,下列叙述中正确的是A.标况下,22.4L 、 、 、 、 均含有 均含有 个分子 个分子 |
B.1  所含的质子数和电子数都为10 所含的质子数和电子数都为10 |
C.1  和 和 的混合物中含有的阴、阳离子总数是3 的混合物中含有的阴、阳离子总数是3 |
D.含2  的浓 的浓 与足量铜在加热条件下反应,有1 与足量铜在加热条件下反应,有1  生成 生成 |
您最近一年使用:0次
解题方法
2 . “绿水青山就是金山银山。”下列相关做法错误的是
| A.垃圾分类回收 | B.化石燃料脱硫 | C.推广使用氢能源 | D.先污染后治理 |
您最近一年使用:0次
名校
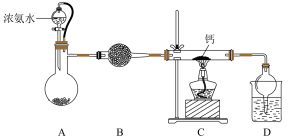
3 . Ca3N2是一种极易水解的试剂。某小组利用氨气与钙反应制备氮化钙。___________ ;分液漏斗和烧瓶间连接的橡皮管的作用___________ 。
(2)装置B中盛放的试剂是___________ ,D中球形干燥管的作用是___________ 。
(3)实验开始前,先通一段时间氨气的原因是___________ 。
(4)C中硬质玻璃管中反应的化学方程式为___________ ,若将Ca3N2溶于足量稀硝酸,反应的离子方程式为___________ 。
(5)本实验装置有一处明显的不足,具体的改进措施是___________ 。
(2)装置B中盛放的试剂是
(3)实验开始前,先通一段时间氨气的原因是
(4)C中硬质玻璃管中反应的化学方程式为
(5)本实验装置有一处明显的不足,具体的改进措施是
您最近一年使用:0次
名校
4 . 下列关于 的说法不正确的是
的说法不正确的是
 的说法不正确的是
的说法不正确的是A.工业制备硫酸后含 的尾气可用NaOH溶液吸收 的尾气可用NaOH溶液吸收 |
| B.SO2使酸性KMnO4褪色,体现了SO2的还原性 |
C. 通入氯水,溶液褪色,体现了 通入氯水,溶液褪色,体现了 的漂白性 的漂白性 |
D. 通入滴有酚酞的 通入滴有酚酞的 溶液中,红色褪去,向褪色后的溶液中滴加 溶液中,红色褪去,向褪色后的溶液中滴加 溶液,红色复现,体现了 溶液,红色复现,体现了 酸性氧化物的通性 酸性氧化物的通性 |
您最近一年使用:0次
名校
5 . 下列离子方程式书写不正确的是
A.稀 溶液中通入过量 溶液中通入过量 : : |
B.氯化铵溶液中加入氢氧化钠溶液加热: +OH- +OH- NH3·H2O NH3·H2O |
C. 和浓盐酸制取 和浓盐酸制取 :MnO2+4H++2Cl- :MnO2+4H++2Cl-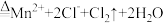 |
D.铜粉加入稀硝酸溶液中: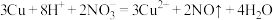 |
您最近一年使用:0次
名校
解题方法
6 . 下列对浓硫酸的叙述错误的是
| A.常温下,浓硫酸能使镁、铝发生钝化 |
| B.浓硫酸与碳反应,浓硫酸表现出强氧化性 |
| C.浓硫酸使胆矾变成白色,浓硫酸表现出吸水性 |
| D.较浓硫酸和Na2SO3反应制取SO2时,较浓硫酸表现出酸性 |
您最近一年使用:0次
名校
7 . 下列各组离子能大量共存的是
A.在透明溶液中: 、 、 、 、 、 、 |
B.能与Al反应放出H2的溶液: 、 、 、 、 、 、 |
C. 溶液中: 溶液中: 、 、 、 、 、 、 |
D.使石蕊变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
8 . 下列说法中正确的是
| A.CuSO4+5H2O=CuSO4·5H2O属于物理变化 |
| B.N与S元素在自然界中仅有化合态 |
C.“雷雨发庄稼”所包含的化学变化有N2 NO NO NO2 NO2 HNO3 HNO3 硝酸盐 硝酸盐 |
| D.植物直接吸收利用空气中的NO和NO2作为肥料,实现氮的固定 |
您最近一年使用:0次
名校
解题方法
9 . 化学与我们的生活息息相关,下列有关物质的性质与应用均正确的是
A. 难溶于水,医疗上可用作X射线透视肠胃的内服药“钡餐” 难溶于水,医疗上可用作X射线透视肠胃的内服药“钡餐” |
B.氨气是一种碱性气体,可用硅胶或无水 干燥 干燥 |
| C.SO2不可作为食品添加剂 |
| D.氨气易液化,液氨气化时吸收大量的热,是一种制冷剂 |
您最近一年使用:0次
名校
解题方法
10 . 为改变生橡胶受热发粘遇冷变硬的不良性能,工业上常将橡胶硫化来改善橡胶的性能, 和
和 均为改善橡胶性能的重要化工产品。
均为改善橡胶性能的重要化工产品。
Ⅰ.已知反应: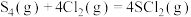 。下列为部分化学键的键能及
。下列为部分化学键的键能及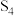 的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):
的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):
(1)则该反应是一个__________ (填“吸热”或“放热”)反应。
Ⅱ. 通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、
通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、 和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产
和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产 ,已知装置B的加热温度控制在140 ℃,回答下列问题:
,已知装置B的加热温度控制在140 ℃,回答下列问题:__________ ,A中发生的化学反应方程式为______________________________ 。
(3)装置接口从左到右的顺序为:a→__________ (填小写字母)。
(4)证明实验中有 生成的现象是
生成的现象是____________________ 。装置C中所装碱石灰的作用是____________________ 。
(5)实验结束时,装置B中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,该反应的离子方程式为____________________ (产物为 和
和 )。
)。
(6)同学们联想到铁与硫单质也能反应。在空气中加热硫粉和铁粉的混合物,可观察到下列现象:
①有淡蓝色火焰,且生成刺激性气味的气体;
②混合物变红,放出热量,最后变成黑色固体;
③不时有火星从混合物中射出。
请写出产生现象②发生反应的化学方程式:________________________________ 。
 和
和 均为改善橡胶性能的重要化工产品。
均为改善橡胶性能的重要化工产品。Ⅰ.已知反应:
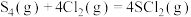 。下列为部分化学键的键能及
。下列为部分化学键的键能及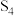 的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):
的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):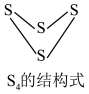
化学键 | S-S | S-Cl | Cl-Cl |
键能/(kJ/mol) | 266 | 255 | 243 |
(1)则该反应是一个
Ⅱ.
 通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、
通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、 和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产
和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产 ,已知装置B的加热温度控制在140 ℃,回答下列问题:
,已知装置B的加热温度控制在140 ℃,回答下列问题: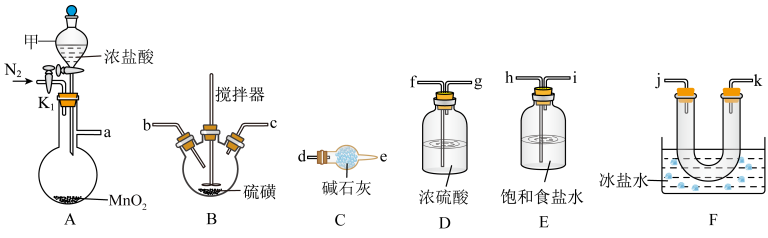
(3)装置接口从左到右的顺序为:a→
(4)证明实验中有
 生成的现象是
生成的现象是(5)实验结束时,装置B中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,该反应的离子方程式为
 和
和 )。
)。(6)同学们联想到铁与硫单质也能反应。在空气中加热硫粉和铁粉的混合物,可观察到下列现象:
①有淡蓝色火焰,且生成刺激性气味的气体;
②混合物变红,放出热量,最后变成黑色固体;
③不时有火星从混合物中射出。
请写出产生现象②发生反应的化学方程式:
您最近一年使用:0次



