名校
解题方法
1 . 2023年,农业绿色发展步伐加快,农业生态环境持续改善。下列说法正确的是
| A.铵盐、硝酸因含有N元素,在农业上常作化肥使用 |
| B.“雷雨发庄稼”,N2与O2在放电的条件下一步转化为NO2,NO2再经过一系列转化生成硝酸盐 |
| C.胆矾和石灰乳混合可制成农药波尔多液,胆矾的化学式为CuSO4·5H2O |
| D.农村常用木柴作燃料做饭,木柴属于化石燃料 |
您最近一年使用:0次
2 . 某化学兴趣小组利用如图所示装置进行SO2的制备与性质探究的一体化实验,下列说法错误的是

| A.分液漏斗中的溶液为70%的稀硫酸,其效果优于30%的硫酸和98.3%的硫酸 |
| B.打开分液漏斗活塞一段时间后,三种试纸均褪色 |
| C.试剂a可选择Na2CO3以吸收多余的SO2,防止污染环境 |
| D.反应结束后,拆卸装置前需打开止水夹K并挤压气囊 |
您最近一年使用:0次
解题方法
3 . 下列制取、收集SO2并验证其还原性及进行尾气处理的装置不能达到实验目的的是
|
|
| A.制取SO2 | B.收集SO2 |
|
|
| C.验证SO2的还原性 | D.吸收多余的SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . X、Y、Z、W、R是五种短周期主族元素,Y2的化学性质十分稳定, Z的最高价氧化物的水化物是一种强碱,W的单质既能和酸,也能和碱溶液反应,且产生相同的气体,R的一种氧化物用于海水提溴吸收塔中的吸收剂,五种元素的原子序数和原子半径的关系如图所示(只标出X)。下列说法错误的是
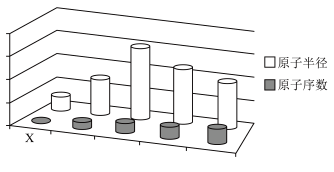
| A.X和Y元素形成的单质之间所发生的反应是可逆反应 |
| B.Z、W的单质一般均采用电解法冶炼 |
| C.常温下 ,W元素形成的单质与Y元素的最高价氧化物的浓溶液不反应 |
| D.R元素的一种氧化物能与其氢化物反应 |
您最近一年使用:0次
5 . 某化学兴趣小组用如图1装置探究氨气喷泉实验中三颈烧瓶内压强变化。图1中的三颈烧瓶收集满氨气后关闭K1,用在冰水中浸泡后的湿毛巾敷在三颈烧瓶上,50s时拿走毛巾并打开K2,整个过程中测得三颈烧瓶内压强变化曲线如图2。下列说法正确的是


| A.固体X可选择NH4Cl,试剂a可选择NaOH溶液 |
| B.20s~50s时,因氨气易溶于水导致三颈烧瓶内压强减小 |
| C.70s时,三颈烧瓶内溶液最多 |
| D.c可以为水,不能是CCl4 |
您最近一年使用:0次
解题方法
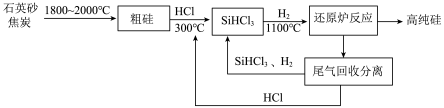
6 . 高纯硅广泛应用于信息技术和新能源技术等领域。改良西门子法生产高纯硅的流程如图所示,回答下列问题:___________ (填化学式),其与氢氟酸溶液反应的化学方程式为___________ 。
(2)制取粗硅时生成的气体为___________ (填化学式),粗硅与HCl反应的化学方程式为___________ 。
(3)还原炉中反应生成的氧化产物的电子式为___________ ,“还原炉反应”通入H2后加热前必须___________ ,以防造成严重后果。
(4)下列说法错误的是___________ (填标号)。
A.改良西门子法中H2、HCl的循环利用,体现了绿色化学思想
B.自然界中硅的存在的主要形式为石英砂
C.石英砂熔点高、硬度大是因为含有硅氧四面体结构
(2)制取粗硅时生成的气体为
(3)还原炉中反应生成的氧化产物的电子式为
(4)下列说法错误的是
A.改良西门子法中H2、HCl的循环利用,体现了绿色化学思想
B.自然界中硅的存在的主要形式为石英砂
C.石英砂熔点高、硬度大是因为含有硅氧四面体结构
您最近一年使用:0次
解题方法
7 . 柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,某研究团队用硫铁矿(主要成分为FeS2、SiO2、Al2O3)为原料,制备柠檬酸亚铁,其流程如图:___________ (填“正”“酸式”或“碱式”)盐,“焙烧”过程中发生反应的化学方程式为___________ ;滤渣1的成分为___________ (填化学式)。
(2)已知:FeS2与H2SO4不反应。则“还原”时FeS2发生反应的离子方程式为___________ 。
(3)“沉铁”时反应需控制温度在35℃以下,其可能的原因是___________ 。
(4)柠檬酸亚铁(FeC6H6O7)在空气中煅烧得到Fe2O3和FeO的混合物。检验Fe2O3存在的方法是___________ 。

(2)已知:FeS2与H2SO4不反应。则“还原”时FeS2发生反应的离子方程式为
(3)“沉铁”时反应需控制温度在35℃以下,其可能的原因是
(4)柠檬酸亚铁(FeC6H6O7)在空气中煅烧得到Fe2O3和FeO的混合物。检验Fe2O3存在的方法是
您最近一年使用:0次
解题方法
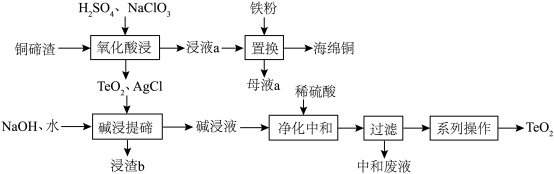
8 . 二氧化碲(TeO2)是一种性能优良的声光晶体材料,一种以铜碲渣(主要成分为Cu2Te,还含有少量Cu,Ag)为原料制备TeO2并获得海绵铜的工艺流程如图所示。
(1)Te位于元素周期表的___________ 族。
(2)“氧化酸浸”时:
①Cu2Te中被氧化的元素为___________ ,为了加快反应速率,不可以采取的措施为___________ (写字母)
A.搅拌反应物 B.升高反应体系的温度 C. 将铜碲渣粉碎 D.使用浓H2SO4
②除Cu2Te反应外,Ag、Cu溶解,配平其中Ag发生反应的离子方程式:______ 。
□Ag+□H++□ =□___________+□H2O+AgCl。
=□___________+□H2O+AgCl。
③若使用稀硝酸代替NaClO3,不足之处可能是___________ 。
(3)“碱浸提碲”时,TeO2反应的化学方程式为___________ ,浸渣b的主要成分为___________ 。
(4)“净化中和”时,稀硫酸参加的主要反应的离子方程式为___________ 。
(1)Te位于元素周期表的
(2)“氧化酸浸”时:
①Cu2Te中被氧化的元素为
A.搅拌反应物 B.升高反应体系的温度 C. 将铜碲渣粉碎 D.使用浓H2SO4
②除Cu2Te反应外,Ag、Cu溶解,配平其中Ag发生反应的离子方程式:
□Ag+□H++□
 =□___________+□H2O+AgCl。
=□___________+□H2O+AgCl。③若使用稀硝酸代替NaClO3,不足之处可能是
(3)“碱浸提碲”时,TeO2反应的化学方程式为
(4)“净化中和”时,稀硫酸参加的主要反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 某溶液X中只可能含有 、Fe2+、Al3+、
、Fe2+、Al3+、 、
、 、Cl-、
、Cl-、 中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
实验Ⅰ.取2000mL溶液X,加入足量的浓NaOH溶液并加热,共收集到5.6L(已换算成标准状况)气体A,反应过程中有沉淀产生,最终无沉淀产生;往反应后的溶液中通入足量CO2,充分反应后生成19.5g沉淀B。
实验Ⅱ.另取200mL溶液X,加入足量2mol·L-1BaCl2溶液,充分反应后生成58.25g白色沉淀C;将沉淀C加入盐酸中,无明显现象。
实验Ⅲ.另取200mL溶液X,加入盐酸酸化的FeCl2溶液,无明显现象。
请回答下列问题:
(1)实验过程中需要用BaCl2固体配制250mL2mol·L-1BaCl2溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、___________ 、250mL容量瓶,容量瓶使用前需要___________ 。
(2)写出生成沉淀B的离子方程式___________ ,实验Ⅰ说明溶液中一定含有的离子有___________ 。
(3)实验Ⅱ中生成白色沉淀C后进行的操作为___________ 、___________ 、干燥、称量;由实验Ⅱ可知溶液X中含有___________ (填离子符号)。
(4)通过三组实验检验,溶液X中一定不含有的离子为___________ 。
 、Fe2+、Al3+、
、Fe2+、Al3+、 、
、 、Cl-、
、Cl-、 中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:实验Ⅰ.取2000mL溶液X,加入足量的浓NaOH溶液并加热,共收集到5.6L(已换算成标准状况)气体A,反应过程中有沉淀产生,最终无沉淀产生;往反应后的溶液中通入足量CO2,充分反应后生成19.5g沉淀B。
实验Ⅱ.另取200mL溶液X,加入足量2mol·L-1BaCl2溶液,充分反应后生成58.25g白色沉淀C;将沉淀C加入盐酸中,无明显现象。
实验Ⅲ.另取200mL溶液X,加入盐酸酸化的FeCl2溶液,无明显现象。
请回答下列问题:
(1)实验过程中需要用BaCl2固体配制250mL2mol·L-1BaCl2溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
(2)写出生成沉淀B的离子方程式
(3)实验Ⅱ中生成白色沉淀C后进行的操作为
(4)通过三组实验检验,溶液X中一定不含有的离子为
您最近一年使用:0次
解题方法
10 . 下列实验操作和现象能得出相应结论的是
| 选项 | 操作、现象 | 结论 |
| A | 往大理石中滴加稀硝酸,产生气泡 | 非金属性:N>C |
| B | 往某溶液中滴加少量BaCl2溶液,产生白色沉淀 | 该溶液中含有SO |
| C | 浓硫酸滴到pH试纸上,试纸变黑 | 浓硫酸具有吸水性 |
| D | 往浓硝酸中加入炽热的炭,有红棕色气体产生 | 浓硝酸具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次







