解题方法
1 . I.现有A、B、C、D四种可溶性物质,它们溶于水后电离产生的所有离子如下表所示:(各物质中所含离子均不相同)
已知:①A物质是中学里用来检验Cl-的盐;
②向B物质的溶液中滴入无色酚酞溶液,呈红色;
③C物质分别与其它三种物质在溶液中反应均能产生白色沉淀,且B和C反应产生的白色沉淀会迅速变为灰绿色,最后变为红褐色。
回答下列问题:
(1)写出下列物质的化学式:A___________ ,D___________ 。
(2)写出③中沉淀颜色变化过程中涉及的化学反应方程式___________ 。
(3)检验溶液中Fe2+是否变质的操作是___________ 。
(4)D物质和C物质在溶液中反应的离子方程式为___________ 。
II.研究钠及其化合物的性质有重要的意义。
(5)某同学向 和
和 的混合液中逐滴加入一定浓度的盐酸,生成
的混合液中逐滴加入一定浓度的盐酸,生成 的体积(标准状况)与加入盐酸的体积的关系如图所示:
的体积(标准状况)与加入盐酸的体积的关系如图所示:
___________ 。
②盐酸的物质的量浓度为___________ 。
| 阳离子 |
|
| 阴离子 |
|
②向B物质的溶液中滴入无色酚酞溶液,呈红色;
③C物质分别与其它三种物质在溶液中反应均能产生白色沉淀,且B和C反应产生的白色沉淀会迅速变为灰绿色,最后变为红褐色。
回答下列问题:
(1)写出下列物质的化学式:A
(2)写出③中沉淀颜色变化过程中涉及的化学反应方程式
(3)检验溶液中Fe2+是否变质的操作是
(4)D物质和C物质在溶液中反应的离子方程式为
II.研究钠及其化合物的性质有重要的意义。
(5)某同学向
 和
和 的混合液中逐滴加入一定浓度的盐酸,生成
的混合液中逐滴加入一定浓度的盐酸,生成 的体积(标准状况)与加入盐酸的体积的关系如图所示:
的体积(标准状况)与加入盐酸的体积的关系如图所示:
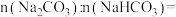
②盐酸的物质的量浓度为
您最近一年使用:0次
解题方法
2 . 以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
(1)黄铁矿中硫元素的化合价为___________ 。
(2)“氧化”时,反应的化学方程式为___________ 。
(3)工业上,吸收 时宜选用的试剂X为
时宜选用的试剂X为___________ (填“水”或“浓硫酸”)。
(4) 高温灼烧时,火焰呈
高温灼烧时,火焰呈___________ 色。
(5) 在保存过程中发生
在保存过程中发生___________ (填“氧化”或“还原”)反应,导致商品 中不可避免地存在
中不可避免地存在 ,欲检验其中的
,欲检验其中的 ,可取少量样品溶于水中,
,可取少量样品溶于水中,___________ ,说明含有 。
。
(6)一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用已知浓度的K2Cr2O7溶液测定其中的Fe2+。反应原理为___________Cr2O +___________Fe2++___________H+=___________Cr3++___________Fe3++___________H2O。
+___________Fe2++___________H+=___________Cr3++___________Fe3++___________H2O。
①配平上述离子反应方程式___________ 。
②某次实验称取0.2800g样品,测定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为___________ %(保留至小数点后第一位)。
 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。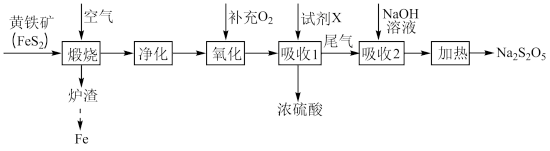
(1)黄铁矿中硫元素的化合价为
(2)“氧化”时,反应的化学方程式为
(3)工业上,吸收
 时宜选用的试剂X为
时宜选用的试剂X为(4)
 高温灼烧时,火焰呈
高温灼烧时,火焰呈(5)
 在保存过程中发生
在保存过程中发生 中不可避免地存在
中不可避免地存在 ,欲检验其中的
,欲检验其中的 ,可取少量样品溶于水中,
,可取少量样品溶于水中, 。
。(6)一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用已知浓度的K2Cr2O7溶液测定其中的Fe2+。反应原理为___________Cr2O
 +___________Fe2++___________H+=___________Cr3++___________Fe3++___________H2O。
+___________Fe2++___________H+=___________Cr3++___________Fe3++___________H2O。①配平上述离子反应方程式
②某次实验称取0.2800g样品,测定时消耗浓度为0.03000mol·L-1的K2Cr2O7溶液25.10mL,则样品中铁含量为
您最近一年使用:0次
3 . 根据下列实验操作和现象所得出的结论或解释一定正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,变浑浊 | 该溶液中可能含有 |
| B | 检验SO2气体中是否混有SO3(g):将气体通入Ba(NO3)2溶液,有白色沉淀生成 | 该气体中一定混有SO3(g) |
| C | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有 |
| D | 用玻璃棒蘸取少量某溶液进行焰色试验,有黄色火焰,透过蓝色钴玻璃显紫色 | 该溶液中一定含有Na+和K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列各组物质的分类正确的是
①含有氧元素的物质叫做氧化物
②CO2、P2O5、N2O3、SiO2均为酸性氧化物
③有单质参加或有单质生成的化学反应不一定是氧化还原反应
④纯碱、一水合氨都是碱
⑤氧化钠溶于水能导电,所以氧化钠是电解质
①含有氧元素的物质叫做氧化物
②CO2、P2O5、N2O3、SiO2均为酸性氧化物
③有单质参加或有单质生成的化学反应不一定是氧化还原反应
④纯碱、一水合氨都是碱
⑤氧化钠溶于水能导电,所以氧化钠是电解质
| A.①② | B.②③ | C.②④ | D.④⑤ |
您最近一年使用:0次
解题方法
5 . 下列离子方程式正确的是
A.向NaOH溶液中通入少量SO2:SO2+OH-=HS |
B.向氯水中通入少量SO2:Cl2+SO2+2H2O=4H++2Cl-+S |
| C.将SO2通入BaCl2溶液中:SO2+H2O+Ba2+=BaSO3↓+2H+ |
D.NO2气体溶于水中:2NO2+H2O=H++ +NO +NO |
您最近一年使用:0次
6 . 下列物质中,不能由单质直接化合生成的是
①CuS ②FeCl2 ③SO3 ④Na2O2 ⑤HCl
①CuS ②FeCl2 ③SO3 ④Na2O2 ⑤HCl
| A.①②③ | B.①②④ | C.②④ | D.②③④ |
您最近一年使用:0次
解题方法
7 . 下列关于N2的叙述正确的是
| A.在雷雨天,空气中的N2与O2可反应生成NO2 |
| B.将氨气转化为NO属于氮的固定 |
| C.氮气是一种无色无味的有毒气体 |
| D.在化学反应中,氮气既可作还原剂也可作氧化剂 |
您最近一年使用:0次
8 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.22.4LN2中含有氮原子的数目为2NA |
| B.18gH2O在标况下的体积为22.4L |
| C.23gNa和78gNa2O2分别与足量水反应产生的气体体积相同 |
| D.1molCu与足量硫粉反应转移的电子数为NA |
您最近一年使用:0次
解题方法
9 . 下列离子方程式中,正确的是
| A.将稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B.将氧化镁与稀盐酸混合:MgO+2H+=Mg2++H2O |
| C.将铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D.将稀盐酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
您最近一年使用:0次
名校
10 . 金表面发生分解反应: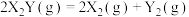 ,其速率方程为
,其速率方程为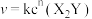 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
下列叙述不正确的是
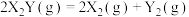 ,其速率方程为
,其速率方程为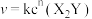 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:t/min c/(mol·L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| X2Y | 0.100 | 0.040 | 0.020 | 0 | ||
| X2 | 0 | 0.020 | ||||
| Y2 | 0 | 0.020 |
| A.提高反应物浓度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为 起始浓度为 ,则反应物浓度减半所需时间为 ,则反应物浓度减半所需时间为 |
D.当升高温度,反应 时 时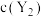 可能小于 可能小于 |
您最近一年使用:0次

 Na+、Fe2+、Ag+、Ba2+
Na+、Fe2+、Ag+、Ba2+

