解题方法
1 . 从核心元素价态分析,亚硝酸盐(如 )、亚铁盐(如
)、亚铁盐(如 )既具有氧化性,又具有还原性,请回答下面问题:
)既具有氧化性,又具有还原性,请回答下面问题:
(1)26号元素铁在周期表中的位置是_____ 。
(2)请用“单线桥”表示 与
与 反应时的电子转移情况
反应时的电子转移情况_____ 。

(3) 像食盐一样有咸味,可以做防腐剂,误食会导致血红蛋白中的
像食盐一样有咸味,可以做防腐剂,误食会导致血红蛋白中的 转化为
转化为 ,可服用维生素C解毒。关于该过程的叙述,不正确的是_____(填字母)。
,可服用维生素C解毒。关于该过程的叙述,不正确的是_____(填字母)。
(4)某同学把酸性 溶液滴加到
溶液滴加到 溶液中,观察到溶液褆色裉色,证明
溶液中,观察到溶液褆色裉色,证明 具有还原性,请写出反应的离子方程式:
具有还原性,请写出反应的离子方程式:_____ 。
(5) 可用于制备一种新型、高效、多功能绿色水处理剂—高铁酸钾
可用于制备一种新型、高效、多功能绿色水处理剂—高铁酸钾 。
。 制备原理为。
制备原理为。
①
②
③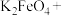 _____
_____ _____
_____ (胶体)
(胶体) _____
_____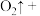 _____
_____
已知 的氧化性很强,还原产物一般为
的氧化性很强,还原产物一般为 ,反应①中还原剂为
,反应①中还原剂为_____ (填化学式);配平并写出反应③的化学方程式:_____ ;简要说明 作为水处理剂时所起的作用:
作为水处理剂时所起的作用:_____ (写出两点)。
 )、亚铁盐(如
)、亚铁盐(如 )既具有氧化性,又具有还原性,请回答下面问题:
)既具有氧化性,又具有还原性,请回答下面问题:(1)26号元素铁在周期表中的位置是
(2)请用“单线桥”表示
 与
与 反应时的电子转移情况
反应时的电子转移情况
(3)
 像食盐一样有咸味,可以做防腐剂,误食会导致血红蛋白中的
像食盐一样有咸味,可以做防腐剂,误食会导致血红蛋白中的 转化为
转化为 ,可服用维生素C解毒。关于该过程的叙述,不正确的是_____(填字母)。
,可服用维生素C解毒。关于该过程的叙述,不正确的是_____(填字母)。A.亚硝酸钠氧化性强于 | B.所有盐类都具有咸味 |
C.维生素 的还原性强于 的还原性强于 | D.亚硝酸钠可能将 氧化生成 氧化生成 |
 溶液滴加到
溶液滴加到 溶液中,观察到溶液褆色裉色,证明
溶液中,观察到溶液褆色裉色,证明 具有还原性,请写出反应的离子方程式:
具有还原性,请写出反应的离子方程式:(5)
 可用于制备一种新型、高效、多功能绿色水处理剂—高铁酸钾
可用于制备一种新型、高效、多功能绿色水处理剂—高铁酸钾 。
。 制备原理为。
制备原理为。①

②

③
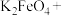 _____
_____ _____
_____ (胶体)
(胶体) _____
_____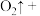 _____
_____
已知
 的氧化性很强,还原产物一般为
的氧化性很强,还原产物一般为 ,反应①中还原剂为
,反应①中还原剂为 作为水处理剂时所起的作用:
作为水处理剂时所起的作用:
您最近一年使用:0次
解题方法
2 . 碳酸镧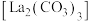 可用于治疗高磷酸盐血症,某化学小组拟以侯氏制碱的原理设计如图装置制备碳酸镧,反应为
可用于治疗高磷酸盐血症,某化学小组拟以侯氏制碱的原理设计如图装置制备碳酸镧,反应为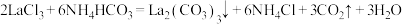 ,下列说法正确的是
,下列说法正确的是
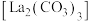 可用于治疗高磷酸盐血症,某化学小组拟以侯氏制碱的原理设计如图装置制备碳酸镧,反应为
可用于治疗高磷酸盐血症,某化学小组拟以侯氏制碱的原理设计如图装置制备碳酸镧,反应为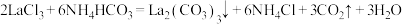 ,下列说法正确的是
,下列说法正确的是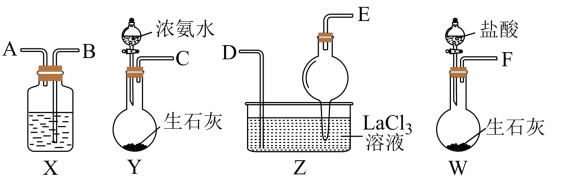
A.装置 中用干燥管的主要目的是增大接触面积,加快气体溶解 中用干燥管的主要目的是增大接触面积,加快气体溶解 |
B.从左向右接口的连接顺序: |
C.实验开始时应先打开 中分液漏斗的旋转活塞 中分液漏斗的旋转活塞 |
D.装置 中盛放的试剂为饱和 中盛放的试剂为饱和 溶液 溶液 |
您最近一年使用:0次
名校
3 . Ⅰ.现有10种物质:①空气;②金刚石;③生石灰;④无水酒精;⑤稀硫酸;⑥干冰;⑦铜;⑧高锰酸钾;⑨水;⑩碳酸钠。用物质的序号填空:
(1)属于混合物的有___________ ,属于单质的有___________ 。
(2)属于碱性氧化物的有___________ ,属于盐类的有___________ 。
(3)属于非电解质的有___________ ,能导电的有___________ ,属于弱电解质的有___________ 。
Ⅱ.请对以下过程形成的物质进行分类:
①冰块加入水中后充分搅拌;
②向蒸馏水中加入过量碳酸钙;
③饱和氯化铁溶液中加入氢氧化钠溶液;
④碘和酒精的混合物;
⑤用烧杯盛放蒸馏水,用半透膜盛放氢氧化铁胶体并放入烧杯中,分离后烧杯中的液体;
⑥将纳米材料分散在塑料中制备复合材料。
(4)属于胶体的是___________ 。
(1)属于混合物的有
(2)属于碱性氧化物的有
(3)属于非电解质的有
Ⅱ.请对以下过程形成的物质进行分类:
①冰块加入水中后充分搅拌;
②向蒸馏水中加入过量碳酸钙;
③饱和氯化铁溶液中加入氢氧化钠溶液;
④碘和酒精的混合物;
⑤用烧杯盛放蒸馏水,用半透膜盛放氢氧化铁胶体并放入烧杯中,分离后烧杯中的液体;
⑥将纳米材料分散在塑料中制备复合材料。
(4)属于胶体的是
您最近一年使用:0次
名校
4 . 下列电离方程式的书写正确的是
A.熔融状态下: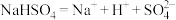 | B. |
C. | D.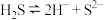 |
您最近一年使用:0次
名校
5 .  在固体、熔融状态、溶于水三种状态下导电实验如图所示,下列说法正确的是
在固体、熔融状态、溶于水三种状态下导电实验如图所示,下列说法正确的是
 在固体、熔融状态、溶于水三种状态下导电实验如图所示,下列说法正确的是
在固体、熔融状态、溶于水三种状态下导电实验如图所示,下列说法正确的是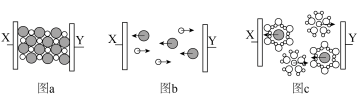
A.固体 中不存在离子,不能导电 中不存在离子,不能导电 |
B. 熔融状态下不能导电 熔融状态下不能导电 |
C. 表示水合氯离子 表示水合氯离子 |
D. 溶液能导电,是电解质 溶液能导电,是电解质 |
您最近一年使用:0次
6 . 下列古诗词中涉及物质的性质说法错误的是
| A.“庐山山南刷铜绿”中的“铜绿”借指的是Cu2(OH)2CO3的颜色 |
| B.“雾凇沆砀,天与云与山与水,上下一白”,雾是一种气溶胶,有丁达尔效应 |
| C.“日照香炉生紫烟,遥看瀑布挂前川”,该过程中涉及化学反应 |
| D.“冲天香阵透长安,满城尽带黄金甲”,金的性质稳定,不易被腐蚀 |
您最近一年使用:0次
名校
解题方法
7 . 某化学兴趣小组的同学设计实验方案来制备氢氧化铁胶体,请思考并回答下列问题。
(1)按照下列实验操作来制备氢氧化铁胶体,不能达到预期目的的是_______。
(2)在制备Fe(OH)3胶体实验中,需要标识的图标是_______ (填序号)。_______ 。
(4)鉴别烧杯中制得的是胶体还是溶液,最常用的方法是_______ 。
(5)某同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是_______ 。
(6)某同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4 溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是_______ 。
②随后沉淀溶解,此反应的离子方程式是_______ 。
(7)在外加电场的情况下,发现Fe(OH)3胶粒向阴极移动,下列说法正确的是_______。
(1)按照下列实验操作来制备氢氧化铁胶体,不能达到预期目的的是_______。
| A.取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加稀的FeCl3溶液。继续煮沸 |
| B.取少量自来水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液。继续煮沸 |
| C.取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液。继续煮沸至液体呈透明的红褐色 |
| D.取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和FeCl3溶液。持续煮沸至液体变浑浊 |
(2)在制备Fe(OH)3胶体实验中,需要标识的图标是
a.  b.
b.  c.
c.  d.
d. 
(4)鉴别烧杯中制得的是胶体还是溶液,最常用的方法是
(5)某同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是
(6)某同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4 溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
(7)在外加电场的情况下,发现Fe(OH)3胶粒向阴极移动,下列说法正确的是_______。
| A.Fe(OH)3胶体粒子能吸附阳离子,从而使Fe(OH)3胶体带正电荷 |
| B.能用过滤的方法除去Fe(OH)3胶体中的硝酸钾溶液 |
| C.Fe(OH)3溶胶中,胶体粒子的直径为1~100 nm |
| D.Fe(OH)3固体与水混合形成的分散系会产生丁达尔效应 |
您最近一年使用:0次
名校
解题方法
8 . I.按要求回答下列问题。
(1)已知H3PO3是二元酸,写出其与足量NaOH反应的化学方程式_______ 。
(2)下列各项与胶体性质有关的有_______ 。(填序号)
a.卤水点豆腐
b.明矾净水
c.油水分离
d.血液透析
e.酸碱中和
f.三角洲形成
g.制备氢氧化铁沉淀
h.臭氧消毒
(3)写出下列反应的离子方程式。
①NH4Fe(SO4)2与足量NaOH溶液反应:_______ 。
②澄清石灰水与少量NaHCO3溶液反应:_______ 。
Ⅱ.已知赤铁矿石的主要成分为氧化铁。某课外兴趣小组的同学将18g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,并不断加入稀盐酸,烧杯中固体的质量随加入稀盐酸的质量变化情况如图所示。_______ g。
(5)计算加入稀盐酸至恰好完全反应时所得溶液的溶质质量分数_______ 。
(1)已知H3PO3是二元酸,写出其与足量NaOH反应的化学方程式
(2)下列各项与胶体性质有关的有
a.卤水点豆腐
b.明矾净水
c.油水分离
d.血液透析
e.酸碱中和
f.三角洲形成
g.制备氢氧化铁沉淀
h.臭氧消毒
(3)写出下列反应的离子方程式。
①NH4Fe(SO4)2与足量NaOH溶液反应:
②澄清石灰水与少量NaHCO3溶液反应:
Ⅱ.已知赤铁矿石的主要成分为氧化铁。某课外兴趣小组的同学将18g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,并不断加入稀盐酸,烧杯中固体的质量随加入稀盐酸的质量变化情况如图所示。
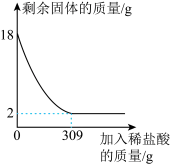
(5)计算加入稀盐酸至恰好完全反应时所得溶液的溶质质量分数
您最近一年使用:0次
名校
解题方法
9 . 离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、S 、OH-、C
、OH-、C 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
Ⅰ.取少量溶液滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ.另取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ,肯定存在的离子是_______ 。
②写出实验Ⅲ中可能发生反应的离子方程式:_______ 。
③如溶液中各种离子的个数相等,确定溶液中____ (填“有”或“无”)K+,判断依据是_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、S
 、OH-、C
、OH-、C 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:Ⅰ.取少量溶液滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ.另取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是
②写出实验Ⅲ中可能发生反应的离子方程式:
③如溶液中各种离子的个数相等,确定溶液中
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.下列物质中:A.NaCl晶体;B.CH3CH2OH (酒精);C.H2SO4溶液;D.单质铜;E.HNO3溶液;F.熔融氯化钾;G.SO2气体;H.液态氯化氢。
(1)能够直接导电的是_______ 。
(2)虽溶于水能导电,但不是电解质的是_______ 。
(3)能导电,但不是电解质的是_______ 。
(4)虽不能直接导电,但也是电解质的是_______ 。
Ⅱ.酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用。下图表示硫酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作。提示:一般条件下,溶液的酸性越强,pH值越小;碱性越强,pH值越大。请从中获取信息,回答下列问题:_______ 溶液(填化学式)。
(6)小明做了硫酸和氢氧化钠溶液混合反应的实验,该中和反应的实质是H+和OH-反应生成水。然后,对反应过程中废液的溶质进行了如下探究,请填写下列表格及填空:
【提出问题】氢氧化钠溶液和稀硫酸混合后,溶质是什么?
【查阅资料】硫酸钠溶液呈中性。
【猜想假设】
猜想i:硫酸钠和氢氧化钠;
猜想ii:硫酸钠和硫酸;
猜想iii:_______ (填名称)。
【设计实验】
【反思与评价】小芳认为实验操作②得出的结论不成立,理由是______________ 。可以改为向废液中加入少量_______ ,溶液变为红色,证明猜想ii成立。
(1)能够直接导电的是
(2)虽溶于水能导电,但不是电解质的是
(3)能导电,但不是电解质的是
(4)虽不能直接导电,但也是电解质的是
Ⅱ.酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用。下图表示硫酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作。提示:一般条件下,溶液的酸性越强,pH值越小;碱性越强,pH值越大。请从中获取信息,回答下列问题:
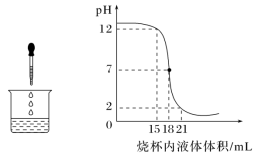
(6)小明做了硫酸和氢氧化钠溶液混合反应的实验,该中和反应的实质是H+和OH-反应生成水。然后,对反应过程中废液的溶质进行了如下探究,请填写下列表格及填空:
【提出问题】氢氧化钠溶液和稀硫酸混合后,溶质是什么?
【查阅资料】硫酸钠溶液呈中性。
【猜想假设】
猜想i:硫酸钠和氢氧化钠;
猜想ii:硫酸钠和硫酸;
猜想iii:
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量废液于试管中,滴入几滴酚酞溶液 | 溶液无明 显变化 | 猜想 |
| ②另取少量废液于试管中,滴入几滴氯化钡溶液 | 有白色沉淀 | 猜想ii成立 |
您最近一年使用:0次



