名校
1 . 按要求填空
(1)相同物质的量的 和
和 ,其分子数目之比为
,其分子数目之比为_______ ,原子数目之比为_______ ,氧原子数目之比为_______ ;质量相同的 和
和 ,其物质的量之比为
,其物质的量之比为_______ 。
(2)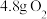 和
和 ,它们的物质的量之比是
,它们的物质的量之比是_______ ,质量之比是_______ ,在同温同压下的体积之比是_______ 。
(3)_______ 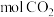 中含有的氧原子数与
中含有的氧原子数与 个
个 分子所含的氧原子数相同。
分子所含的氧原子数相同。
(1)相同物质的量的
 和
和 ,其分子数目之比为
,其分子数目之比为 和
和 ,其物质的量之比为
,其物质的量之比为(2)
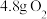 和
和 ,它们的物质的量之比是
,它们的物质的量之比是(3)
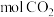 中含有的氧原子数与
中含有的氧原子数与 个
个 分子所含的氧原子数相同。
分子所含的氧原子数相同。
您最近一年使用:0次
2 . 生产生活中的化学反应都伴随能量的变化,请回答下列问题。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途,制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)天然气中含有的微量 会腐蚀管道和设备,在
会腐蚀管道和设备,在 下进行脱硫处理,
下进行脱硫处理, 会被氧气氧化为
会被氧气氧化为 ,并产生水蒸气。
,并产生水蒸气。
写出该反应的热化学方程式:___________ 。
(3)汽车尾气中排放的 和
和 会污染环境,在汽车尾气系统中装置催化转化器,可有效降低
会污染环境,在汽车尾气系统中装置催化转化器,可有效降低 和
和 的排放。已知:
的排放。已知:
Ⅰ.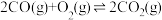
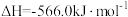
Ⅱ.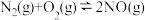
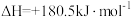
Ⅲ.
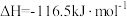
① 的燃烧热为
的燃烧热为___________  。
。
② 将
将 还原为单质的热化学方程式为
还原为单质的热化学方程式为___________ 。
③下图是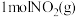 和
和 反应生成
反应生成 和
和 过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是___________ (填“增大”、“减小”或“不变”,下同), 的变化是
的变化是___________ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途,制作冷敷袋可以利用
(2)天然气中含有的微量
 会腐蚀管道和设备,在
会腐蚀管道和设备,在 下进行脱硫处理,
下进行脱硫处理, 会被氧气氧化为
会被氧气氧化为 ,并产生水蒸气。
,并产生水蒸气。| 化学键 | 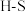 |  |  |  中共价键 中共价键 |
键能/(  ) ) | 339 | 498 | 464 | 1083 |
(3)汽车尾气中排放的
 和
和 会污染环境,在汽车尾气系统中装置催化转化器,可有效降低
会污染环境,在汽车尾气系统中装置催化转化器,可有效降低 和
和 的排放。已知:
的排放。已知:Ⅰ.
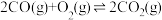
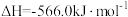
Ⅱ.
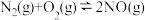
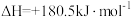
Ⅲ.

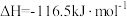
①
 的燃烧热为
的燃烧热为 。
。②
 将
将 还原为单质的热化学方程式为
还原为单质的热化学方程式为③下图是
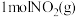 和
和 反应生成
反应生成 和
和 过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是 的变化是
的变化是
您最近一年使用:0次
解题方法
3 . 回答下列问题
(1)有以下六种物质:①乙醇;②0.1mol/LNa2CO3溶液;③NaOH固体;④液态氯化氢;⑤AgC1;⑥石墨。
上述状态下的物质中,能导电的有_____ (填序号,下同),属于电解质的有_____ 。
(2)请写出下列物质在水溶液中的电离方程式:
①H2SO3_____ 。
②KHSO4_____ 。
③NH4HCO3_____ 。
(1)有以下六种物质:①乙醇;②0.1mol/LNa2CO3溶液;③NaOH固体;④液态氯化氢;⑤AgC1;⑥石墨。
上述状态下的物质中,能导电的有
(2)请写出下列物质在水溶液中的电离方程式:
①H2SO3
②KHSO4
③NH4HCO3
您最近一年使用:0次
4 . 碳酸锂( )是制备新能源汽车电池的重要原料。如图是一种利用
)是制备新能源汽车电池的重要原料。如图是一种利用 样品(含少量
样品(含少量 、
、 )模拟提纯碳酸锂的工艺流程。
)模拟提纯碳酸锂的工艺流程。
【查阅资料】 为无色晶体,微溶于水,在冷水中的溶解度比热水中大,其化学性质与
为无色晶体,微溶于水,在冷水中的溶解度比热水中大,其化学性质与 类似,
类似, 难溶于水,不与稀硫酸、稀盐酸反应。
难溶于水,不与稀硫酸、稀盐酸反应。
(1)写出“步骤Ⅰ”中主要反应的化学方程式为___________ 。
(2)“滤渣1”是___________ (填化学式),“滤液1”中大量存在的金属阳离子有___________ (填离子符号)。
(3)“滤渣2”的颜色为___________ ,“步骤Ⅲ”中反应的化学方程式为___________ 。
(4)为了提高成品的产量,在“步骤Ⅲ”中,下列温度最适宜的是___________ (填序号)。
A.0℃ B.20℃ C.80℃
(5)“滤液3”中大量存在的酸根阴离子有___________ (填离子符号);将“滤液3”经一系列操作可得到其他化工产品,其中过滤操作所用到的主要玻璃仪器有___________ 。
 )是制备新能源汽车电池的重要原料。如图是一种利用
)是制备新能源汽车电池的重要原料。如图是一种利用 样品(含少量
样品(含少量 、
、 )模拟提纯碳酸锂的工艺流程。
)模拟提纯碳酸锂的工艺流程。【查阅资料】
 为无色晶体,微溶于水,在冷水中的溶解度比热水中大,其化学性质与
为无色晶体,微溶于水,在冷水中的溶解度比热水中大,其化学性质与 类似,
类似, 难溶于水,不与稀硫酸、稀盐酸反应。
难溶于水,不与稀硫酸、稀盐酸反应。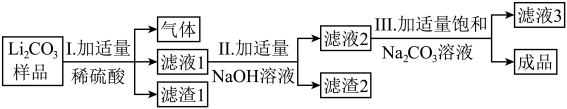
(1)写出“步骤Ⅰ”中主要反应的化学方程式为
(2)“滤渣1”是
(3)“滤渣2”的颜色为
(4)为了提高成品的产量,在“步骤Ⅲ”中,下列温度最适宜的是
A.0℃ B.20℃ C.80℃
(5)“滤液3”中大量存在的酸根阴离子有
您最近一年使用:0次
解题方法
5 . 金属钴(Co)的金属活动性与铁相近,钴的化合物相关性质如下,下列判断合理的是
| 物质 |  |  |  |  |
| 在水中的溶解性等 | 难溶,灰绿色固体 | 难溶,粉红色固体 | 易溶,溶液呈粉红色 | 难溶,粉红色固体 |
A.Co能从 溶液中置换出Mg 溶液中置换出Mg | B. 能与盐酸反应得到粉红色溶液 能与盐酸反应得到粉红色溶液 |
C. 能与盐酸反应生成 能与盐酸反应生成 | D. 可由Co与 可由Co与 溶液反应制得 溶液反应制得 |
您最近一年使用:0次
6 . 向盛有一定质量 、
、 和
和 混合溶液的烧杯中,逐渐加入锌粉至过量使其充分反应。烧杯里“溶液中溶质的质量”和“金属固体的质量”随锌粉质量变化情况如图所示,下列说法正确的是
混合溶液的烧杯中,逐渐加入锌粉至过量使其充分反应。烧杯里“溶液中溶质的质量”和“金属固体的质量”随锌粉质量变化情况如图所示,下列说法正确的是
 、
、 和
和 混合溶液的烧杯中,逐渐加入锌粉至过量使其充分反应。烧杯里“溶液中溶质的质量”和“金属固体的质量”随锌粉质量变化情况如图所示,下列说法正确的是
混合溶液的烧杯中,逐渐加入锌粉至过量使其充分反应。烧杯里“溶液中溶质的质量”和“金属固体的质量”随锌粉质量变化情况如图所示,下列说法正确的是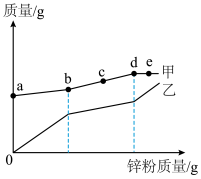
A.甲曲线ab段发生反应: |
| B.乙曲线表示“溶液中溶质的质量”随锌粉质量变化情况 |
| C.反应过程中溶液质量减小 |
D.e点时,溶液中大量存在的金属阳离子是 和 和 |
您最近一年使用:0次
解题方法
7 . 元素化合价和物质类别是认识物质的两个重要维度,构建元素化合价和物质类别的“价类二维图”是学习元素及其化合物的一种重要方法。如图是氮元素的“价类二维图”,下列说法正确的是
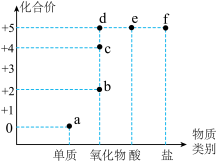
| A.a点对应的物质约占空气质量的78% |
B.b点对应物质的化学式为 |
| C.e点对应的物质能使紫色石蕊试液变蓝 |
| D.f点对应的物质可由e对应的物质与碱反应生成 |
您最近一年使用:0次
8 . 实验小组用图1装置探究稀 溶液与稀盐酸的反应,用注射器吸取稀盐酸,逐滴滴加到盛有
溶液与稀盐酸的反应,用注射器吸取稀盐酸,逐滴滴加到盛有 溶液的烧杯中,测得溶液温度随时间变化的曲线如图2所示。下列说法
溶液的烧杯中,测得溶液温度随时间变化的曲线如图2所示。下列说法不正确 的是
 溶液与稀盐酸的反应,用注射器吸取稀盐酸,逐滴滴加到盛有
溶液与稀盐酸的反应,用注射器吸取稀盐酸,逐滴滴加到盛有 溶液的烧杯中,测得溶液温度随时间变化的曲线如图2所示。下列说法
溶液的烧杯中,测得溶液温度随时间变化的曲线如图2所示。下列说法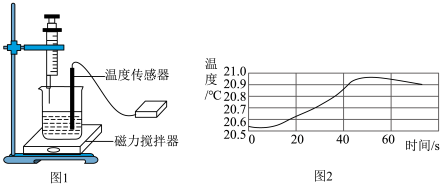
| A.图2说明该反应是放热反应 |
B.滴加过程中烧杯里溶液的 浓度逐渐增大 浓度逐渐增大 |
C.40s时溶液中的溶质是 和 和 |
D.实验说明 溶液与稀盐酸发生了反应 溶液与稀盐酸发生了反应 |
您最近一年使用:0次
9 . 将 和
和 的混合物27.4g充分加热至质量不再改变,冷却至室温,再向其中加入200g溶质质量分数为7.3%的盐酸,恰好完全反应。下列分析正确的是
的混合物27.4g充分加热至质量不再改变,冷却至室温,再向其中加入200g溶质质量分数为7.3%的盐酸,恰好完全反应。下列分析正确的是
已知: 受热不易分解,
受热不易分解, 受热易分解:
受热易分解: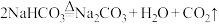 。
。
 和
和 的混合物27.4g充分加热至质量不再改变,冷却至室温,再向其中加入200g溶质质量分数为7.3%的盐酸,恰好完全反应。下列分析正确的是
的混合物27.4g充分加热至质量不再改变,冷却至室温,再向其中加入200g溶质质量分数为7.3%的盐酸,恰好完全反应。下列分析正确的是已知:
 受热不易分解,
受热不易分解, 受热易分解:
受热易分解: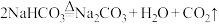 。
。| A.原混合物中钠元素质量为9.2g | B.整个实验过程中产生 的质量为8.8g 的质量为8.8g |
C.原混合物中 质量为10.6g 质量为10.6g | D.反应后所得溶液的溶质质量分数为15% |
您最近一年使用:0次
解题方法
10 . 元素周期表体现了化学元素之间的相互联系和变化规律。已知X、Y、Z、W为前20号元素,原子序数依次增大,X是非金属元素,Y元素原子最外层电子数是次外层电子数的3倍。X元素与Y元素可形成 和
和 型化合物,
型化合物, 可形成硫酸型酸雨。Z和W在同一横行,四种元素原子的最外层电子数之和为14,下列说法正确的是
可形成硫酸型酸雨。Z和W在同一横行,四种元素原子的最外层电子数之和为14,下列说法正确的是
 和
和 型化合物,
型化合物, 可形成硫酸型酸雨。Z和W在同一横行,四种元素原子的最外层电子数之和为14,下列说法正确的是
可形成硫酸型酸雨。Z和W在同一横行,四种元素原子的最外层电子数之和为14,下列说法正确的是| A.X元素组成的单质具有可燃性 |
B.化合物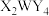 的水溶液不能与Z单质反应生成X的单质 的水溶液不能与Z单质反应生成X的单质 |
C.Y和Z元素可形成化合物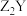 |
| D.Z元素的原子在化学反应中易得到电子 |
您最近一年使用:0次



