名校
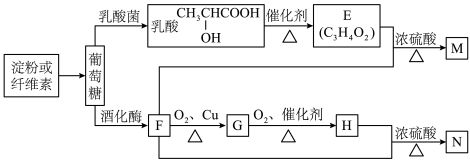
1 . 以富含淀粉或纤维素的农林产品为原料,制备生活中的某些有机物。
(1)葡萄糖的分子式为_______ ,乳酸分子中的官能团的名称为_______ 。
(2)下列说法正确的是_______。
(3)G在一定条件下可转化为F,则该反应的反应类型是_______ 。
(4)久置的M自身会发生聚合反应得到弹性较好的聚合物,请写出该聚合物的结构简式:_______ 。
(5)写出“F→G”、“E+F→M”两个反应的化学方程式(有机物用结构简式表示)
“F→G”:_______
“E+F→M”:_______
(1)葡萄糖的分子式为
(2)下列说法正确的是_______。
| A.淀粉和纤维素互为同分异构体 |
| B.E和H属于同系物、M和N也属于同系物 |
| C.E、F和G均能使酸性高锰酸钾溶液褪色 |
| D.乳酸、F和H均能与钠、氢氧化钠溶液发生反应 |
(3)G在一定条件下可转化为F,则该反应的反应类型是
(4)久置的M自身会发生聚合反应得到弹性较好的聚合物,请写出该聚合物的结构简式:
(5)写出“F→G”、“E+F→M”两个反应的化学方程式(有机物用结构简式表示)
“F→G”:
“E+F→M”:
您最近一年使用:0次
名校
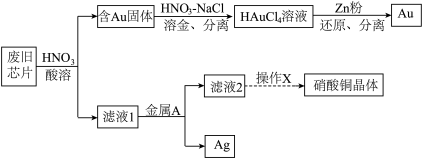
2 . 废旧芯片中常含有大量的单质Si和少量的Au、Ag、Cu等金属。某化学兴趣小组设计了如下图所示方法回收废旧芯片中的Au、Ag并制取硝酸铜晶体[Cu(NO3)2·6H2O]。 。
。
请回答下列问题:
(1)为加快酸溶速率,可采取的两种措施为:_______ 、_______ 。
(2)浓、稀HNO3均可作酸溶试剂,溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量多的反应的化学方程式_______ 。
(3)写出过量的锌粉还原HAuCl4溶液生成金的离子方程式_______ 。
(4)金属A的名称是_______ 。
(5)操作X包括了_______ 过滤、洗涤、晾干。
(6)上述过程产生的NO和NO2等氮氧化物会污染空气,可用如下方法处理:
①氨气催化吸收法:已知1mol氨气恰好能将含NO和NO2共0.9mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比_______ 。
②酸化的Ca(ClO)2溶液吸收法:NO能被氧化成NO 。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是_______ 。
 。
。请回答下列问题:
(1)为加快酸溶速率,可采取的两种措施为:
(2)浓、稀HNO3均可作酸溶试剂,溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量多的反应的化学方程式
(3)写出过量的锌粉还原HAuCl4溶液生成金的离子方程式
(4)金属A的名称是
(5)操作X包括了
(6)上述过程产生的NO和NO2等氮氧化物会污染空气,可用如下方法处理:
①氨气催化吸收法:已知1mol氨气恰好能将含NO和NO2共0.9mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比
②酸化的Ca(ClO)2溶液吸收法:NO能被氧化成NO
 。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是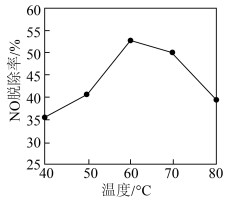
您最近一年使用:0次
名校
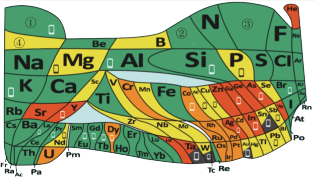
3 . 化学教材后的元素周期表为通用元素周期表,2019年是门捷列夫提出元素周期表诞生150周年,联合国宣布2019年为“国际化学元素周期表年”。同年,欧洲化学学会(EuChemS)发布了1张“扭曲”的元素周期表,指出:由于过度使用,部分元素可能在未来的100年内从地球上消失。每种元素在周期表上所占面积的大小,呈现出元素的稀缺程度。___________ ;④是手机电池的主要构成元素,④的单质在③的常见单质中点燃的方程式为___________ 。
(2)用电子式表示①与③形成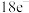 化合物的过程:
化合物的过程:___________ 。
(3)①和②能形成多种化合物,下图模型表示的分子中,不可能由①②形成的有___________ (填序号)。___________ 。
(5)一种新型除草剂的结构如下图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M与Z同主族,W是最不稀缺的元素。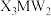 与NaOH溶液反应只生成一种盐,则
与NaOH溶液反应只生成一种盐,则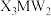 与足量NaOH溶液反应的离子方程式为
与足量NaOH溶液反应的离子方程式为___________ 。
② 可做火箭推进剂的燃料,优点之一是其与
可做火箭推进剂的燃料,优点之一是其与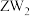 反应的产物绿色无污染,请写出相应的化学方程式
反应的产物绿色无污染,请写出相应的化学方程式___________ 。
(2)用电子式表示①与③形成
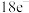 化合物的过程:
化合物的过程:(3)①和②能形成多种化合物,下图模型表示的分子中,不可能由①②形成的有
a. 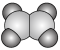 b.
b.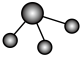 c.
c. 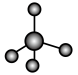 d.
d.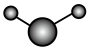
(5)一种新型除草剂的结构如下图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M与Z同主族,W是最不稀缺的元素。
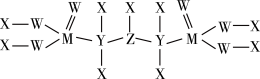
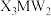 与NaOH溶液反应只生成一种盐,则
与NaOH溶液反应只生成一种盐,则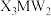 与足量NaOH溶液反应的离子方程式为
与足量NaOH溶液反应的离子方程式为②
 可做火箭推进剂的燃料,优点之一是其与
可做火箭推进剂的燃料,优点之一是其与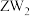 反应的产物绿色无污染,请写出相应的化学方程式
反应的产物绿色无污染,请写出相应的化学方程式
您最近一年使用:0次
名校
4 . 请回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是___________ 。(填字母)
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有___________ 。(填字母)
a. b.盐酸和镁条
b.盐酸和镁条
c.盐酸和碳酸氢钠 d. 和氯化铵
和氯化铵
e. 分解
分解
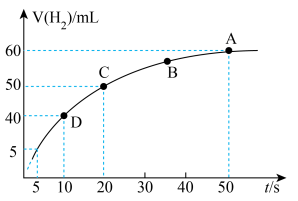
③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为___________ ;在20s内用H+浓度表示的平均反应速率
___________ (20s时溶液体积为50mL,气体摩尔体积为25L/mol)。 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。
t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:
①4-6min内 的平均反应速率
的平均反应速率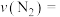
___________ 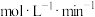
②下列情况能说明反应达到平衡状态的是___________ (填标号)。
A.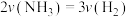 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化
C. 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变
③如表列出了在不同温度和压强下,反应达到平衡时 的百分含量
的百分含量 。
。
从表中数据得出,合成氨最优的条件是___________ 。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。
①制作冷敷袋常利用吸热的化学变化来实现,以下组合最能满足的是
A.冰 B.硝酸铵+水 C.硝酸铵+水合碳酸钠
②下列过程中的热量变化与冰袋一致的有
a.
 b.盐酸和镁条
b.盐酸和镁条c.盐酸和碳酸氢钠 d.
 和氯化铵
和氯化铵e.
 分解
分解③某课外实验小组利用压强传感器、温度传感器、数据采集器和计算机等数字化实验设备,探究镁与一定量盐酸的反应速率,测得产生
 的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
的体积与反应时间的关系曲线如图所示,结合所学知识分析速率变化的原因为
 ,是一个常见的放热反应。回答下列问题。
,是一个常见的放热反应。回答下列问题。t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的
 和
和 合成氨,实验中测得
合成氨,实验中测得 随时间的变化如表所示:
随时间的变化如表所示:①4-6min内
 的平均反应速率
的平均反应速率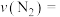
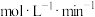
| 时间/min | 2 | 4 | 6 | 8 | 10 | 12 |
 / / | 0.04 | 0.10 | 0.14 | 0.16 | 0.16 | 0.16 |
A.
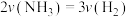 B.混合气体的平均相对分子质量不再变化
B.混合气体的平均相对分子质量不再变化C.
 体积分数不再变化 D.混合气体的密度保持不变
体积分数不再变化 D.混合气体的密度保持不变③如表列出了在不同温度和压强下,反应达到平衡时
 的百分含量
的百分含量 。
。压强/MPa % %温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
您最近一年使用:0次
名校
5 . 钛被称为“二十一世纪的金属”,绿矾是重要的化工原料,用钛铁矿[主要成分是钛酸亚铁( ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下:___________ 。
(2)矿渣的主要成分是___________ ;试剂A为___________ (填化学式)。
(3)“操作Ⅱ”为___________ 、___________ 、过滤、洗涤、干燥。
(4)对所得到的绿矾晶体常用75%的乙醇溶液洗涤,用乙醇溶液洗涤绿矾的优点为___________ 。
(5)沸腾氯化中,氯气与矿料逆流而行,目的是___________ ,充分反应后,混合气体中CO与 的分压之比为1∶2,该温度下,
的分压之比为1∶2,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为___________ 。
(6)俄罗斯科学家于20世纪60年代提出了用金属氢化物还原法生产钛粉这一技术构想,并进行了试验研究。俄罗斯图拉化工冶金厂以 为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式
为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式___________ 。
 ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下: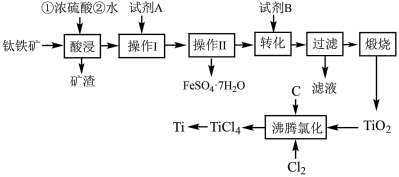
(2)矿渣的主要成分是
(3)“操作Ⅱ”为
(4)对所得到的绿矾晶体常用75%的乙醇溶液洗涤,用乙醇溶液洗涤绿矾的优点为
(5)沸腾氯化中,氯气与矿料逆流而行,目的是
 的分压之比为1∶2,该温度下,
的分压之比为1∶2,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为(6)俄罗斯科学家于20世纪60年代提出了用金属氢化物还原法生产钛粉这一技术构想,并进行了试验研究。俄罗斯图拉化工冶金厂以
 为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式
为原料,采用在1100℃-1200℃条件下氢化钙还原生产钛粉的方法并产生一种气体,请写出相关反应方程式
您最近一年使用:0次
名校
解题方法
6 . A~F六种元素中,除F外其他均为短周期元素,它们的原子结构或性质如下表所示。
请回答下列问题:(用对应的化学用语回答)
(1)B在元素周期表中的位置是___________ ;A和C形成供氧剂的电子式___________ 。
(2) A、C、D、E离子半径由小到大的顺序为___________ 。(用离子符号表示)
(3)F的某种氯化物的饱和溶液滴加到沸水中可以形成胶体,写出此反应的化学反应方程式:___________ 。
(4)A和C形成的供氧剂与C的氢化物反应的化学方程式是:___________ 。
(5)E的单质与A的最高价氧化物的水化物反应的离子方程式为___________ 。
(6)红热的B单质与D的最高价氧化物对应水化物的浓溶液反应的化学方程式:___________ 。
| 元素 | 原子结构或性质 |
| A | 原子的最外层电子数是电子层数的 ,其含氧化合物可作为供氧剂 ,其含氧化合物可作为供氧剂 |
| B | 其形成的一种同位素原子在考古中可推测化石的年代 |
| C | 地壳中含量最多的元素 |
| D | 其单质位于火山口附近 |
| E | 与D同周期,且最外层电子数等于电子层数 |
| F | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
(1)B在元素周期表中的位置是
(2) A、C、D、E离子半径由小到大的顺序为
(3)F的某种氯化物的饱和溶液滴加到沸水中可以形成胶体,写出此反应的化学反应方程式:
(4)A和C形成的供氧剂与C的氢化物反应的化学方程式是:
(5)E的单质与A的最高价氧化物的水化物反应的离子方程式为
(6)红热的B单质与D的最高价氧化物对应水化物的浓溶液反应的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 材料是经济增长与社会发展的重要物质基础,请回答下列问题。
(1)硅是重要的半导体材料,广泛应用于电子产品领域,工业上以硅石 为原料制备冶金级高纯硅的工艺流程如图所示:
为原料制备冶金级高纯硅的工艺流程如图所示: 室温下为易挥发、易水解的无色液体。
室温下为易挥发、易水解的无色液体。
①写出上述过程中氧化过程的化学方程式:___________ ;
② 极易水解且生成某种可燃性气体,写出化学反应方程式:
极易水解且生成某种可燃性气体,写出化学反应方程式:___________ ;
③上述工艺生产中需要在无水、无氧的条件下进行的操作有:___________ 。
(2)某MOFs多孔材料能高选择性吸附 ,其孔径大小和形状恰好将
,其孔径大小和形状恰好将 “固定”。废气中的
“固定”。废气中的 被吸附后,经处理能全部转化为
被吸附后,经处理能全部转化为 。原理示意图如下。
。原理示意图如下。
①写出反应中转化为 的化学反应方程式
的化学反应方程式___________ ;
②每生成 时,氧化剂与还原剂的物质的量之比为
时,氧化剂与还原剂的物质的量之比为___________ 。
(3)甲醇是重要的化工原料之一,其制备和用途研究一直是化学工业热门研究方向。
工业上利用 和
和 合成甲醇,反应方程式为
合成甲醇,反应方程式为 ,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入
,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入 和
和 进行上述反应,测得
进行上述反应,测得 和
和 浓度随时间变化如图所示。
浓度随时间变化如图所示。 和
和 充分反应后,放出的能量
充分反应后,放出的能量___________ (填“>”“<”或“=”)89kJ;
②从0到10min,
___________ ;
③达到平衡时 的体积分数
的体积分数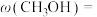
___________ 。
(1)硅是重要的半导体材料,广泛应用于电子产品领域,工业上以硅石
 为原料制备冶金级高纯硅的工艺流程如图所示:
为原料制备冶金级高纯硅的工艺流程如图所示: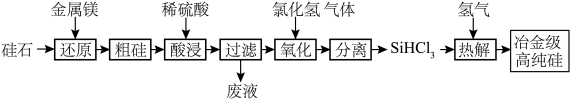
 室温下为易挥发、易水解的无色液体。
室温下为易挥发、易水解的无色液体。①写出上述过程中氧化过程的化学方程式:
②
 极易水解且生成某种可燃性气体,写出化学反应方程式:
极易水解且生成某种可燃性气体,写出化学反应方程式:③上述工艺生产中需要在无水、无氧的条件下进行的操作有:
(2)某MOFs多孔材料能高选择性吸附
 ,其孔径大小和形状恰好将
,其孔径大小和形状恰好将 “固定”。废气中的
“固定”。废气中的 被吸附后,经处理能全部转化为
被吸附后,经处理能全部转化为 。原理示意图如下。
。原理示意图如下。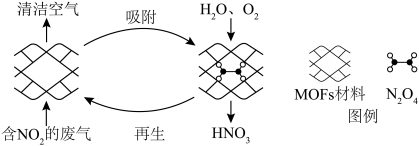

①写出反应中转化为
 的化学反应方程式
的化学反应方程式②每生成
 时,氧化剂与还原剂的物质的量之比为
时,氧化剂与还原剂的物质的量之比为(3)甲醇是重要的化工原料之一,其制备和用途研究一直是化学工业热门研究方向。
工业上利用
 和
和 合成甲醇,反应方程式为
合成甲醇,反应方程式为 ,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入
,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入 和
和 进行上述反应,测得
进行上述反应,测得 和
和 浓度随时间变化如图所示。
浓度随时间变化如图所示。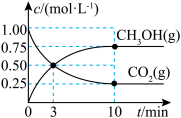
 和
和 充分反应后,放出的能量
充分反应后,放出的能量②从0到10min,

③达到平衡时
 的体积分数
的体积分数
您最近一年使用:0次
解题方法
8 . 硫和氮是人们熟悉的元素,含硫、含氮的物质与人们的生活密切相关。自然界中硫、氮的循环是维持生态平衡的重要物质基础。
Ⅰ.某化学兴趣小组制备并验证SO2的相关性质,实验装置如下图(abc均为浸有相应试液的棉花,夹持与加热装置略)。_____________ ,该反应体现了浓硫酸的性质是_____________ 。
(2)b处观察到紫色褪去,SO2体现的化学性质为_____________ 。
(3)c处的棉花团蘸有浓NaOH溶液,所起的作用是_____________ 。
Ⅱ.已知氮元素及其化合物的转化关系如图所示,回答下列问题。____________ 。
(5)生物固氮过程中铵盐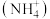 可通过硝化细菌转化为硝酸盐
可通过硝化细菌转化为硝酸盐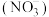 ,若该过程中转移了2mol电子,则生成
,若该过程中转移了2mol电子,则生成 的物质的量为
的物质的量为____________ 。
(6)氮肥能促进植物光合作用,常见的氮肥有铵态氮肥、硝态氮肥等。检验某固体氮肥中含有 的实验操作是
的实验操作是____________ 。
Ⅰ.某化学兴趣小组制备并验证SO2的相关性质,实验装置如下图(abc均为浸有相应试液的棉花,夹持与加热装置略)。
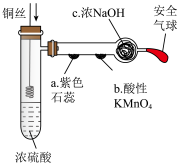
(2)b处观察到紫色褪去,SO2体现的化学性质为
(3)c处的棉花团蘸有浓NaOH溶液,所起的作用是
Ⅱ.已知氮元素及其化合物的转化关系如图所示,回答下列问题。
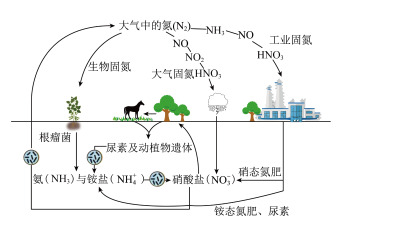
(5)生物固氮过程中铵盐
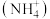 可通过硝化细菌转化为硝酸盐
可通过硝化细菌转化为硝酸盐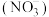 ,若该过程中转移了2mol电子,则生成
,若该过程中转移了2mol电子,则生成 的物质的量为
的物质的量为(6)氮肥能促进植物光合作用,常见的氮肥有铵态氮肥、硝态氮肥等。检验某固体氮肥中含有
 的实验操作是
的实验操作是
您最近一年使用:0次
解题方法
9 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图所示的实验。请据此回答下列问题。___________ 。
(2)浓硫酸和木炭粉发生的反应化学方程式___________ 。
(3)装置A中出现___________ 现象,证明气体产物中有 。
。
(4)为验证产物中是否含有 ,该同学思考如下:
,该同学思考如下:
①装置可证明产物中有 生成,现象是
生成,现象是___________ 。
②该同学认为,如果去掉装置B也能实现产物 的验证,该同学依据的实验现象是
的验证,该同学依据的实验现象是___________ 。
③在不影响实验检验结果的情况下,理论上以下试剂中可以用来代替装置B中的品红溶液的有___________ (填序号)。
a. 溶液 b.饱和
溶液 b.饱和 溶液 c.氯水 d.
溶液 c.氯水 d. 溶液
溶液
(5)D装置的作用是___________ 。

(2)浓硫酸和木炭粉发生的反应化学方程式
(3)装置A中出现
 。
。(4)为验证产物中是否含有
 ,该同学思考如下:
,该同学思考如下:①装置可证明产物中有
 生成,现象是
生成,现象是②该同学认为,如果去掉装置B也能实现产物
 的验证,该同学依据的实验现象是
的验证,该同学依据的实验现象是③在不影响实验检验结果的情况下,理论上以下试剂中可以用来代替装置B中的品红溶液的有
a.
 溶液 b.饱和
溶液 b.饱和 溶液 c.氯水 d.
溶液 c.氯水 d. 溶液
溶液(5)D装置的作用是
您最近一年使用:0次
10 . 元素周期表反映了元素之间的内在联系,是研究物质性质的重要工具。下表是元素周期表的一部分,请回答:_________ 。
(2)②③④简单氢化物的稳定性由强到弱的顺序为_________ (填化学式);④⑤⑥形成的简单离子半径由大到小的顺序为_________ (填离子符号)。
(3)用电子式表示④的简单氢化物的形成过程_______________ 。
(4)①~⑦号元素中,金属性最强的是_________ (写元素符号),其最高价氧化物对应的水化物与元素⑥
的单质反应的化学方程式为。
(5)⑧在元素周期表中的位置是____________ 。
(6)下列性质的比较,不能用元素周期律解释的是__________。

(2)②③④简单氢化物的稳定性由强到弱的顺序为
(3)用电子式表示④的简单氢化物的形成过程
(4)①~⑦号元素中,金属性最强的是
的单质反应的化学方程式为。
(5)⑧在元素周期表中的位置是
(6)下列性质的比较,不能用元素周期律解释的是__________。
A.酸性: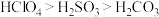 | B.碱性: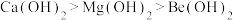 |
C.稳定性: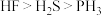 | D.沸点高低: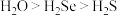 |
您最近一年使用:0次



