名校
1 . I.亚硫酸氢铵(NH4HSO3)可用作防腐剂、还原剂,也用于制造二氧化硫、保险粉等,某化学兴趣小组设计如图装置(加热和夹持装置已省略)制备亚硫酸氢铵,请回答下列问题:
(1)盛装浓硫酸的仪器名称为___________ ;实验开始时,先关闭K1,打开K2,先通氨气使溶液呈碱性的目的:___________ ;戊装置的试管内反应的化学方程式为___________ ;乙中仪器a的作用是___________ 。
(2)一段时间后,关闭K2,打开K1,甲装置圆底烧瓶内发生反应的化学方程式为___________ ;丙装置的作用是___________ ;丁装置用于吸收多余的SO2,则丁装置中的试剂为___________ 。
(3)设计实验检验亚硫酸氢铵中阳离子,写出操作、现象及相应的结论:___________ 。
II.另一化学兴趣小组同学利用下图装置探究氨的催化氧化,并测定氯化铵的纯度。取10.0g氯化铵样品(杂质不参加反应)与足量消石灰反应,将产生的气体全部通入下图装置,待完全反应后,E中质量增加了1.02g,通过测量的数据进行计算得出C中反应生成的水为0.18 mol。___________ 。
(5)计算氯化铵样品的纯度___________ %(保留小数点后一位)。
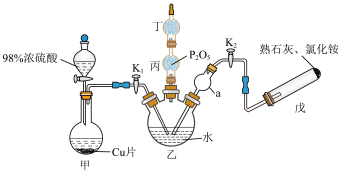
(1)盛装浓硫酸的仪器名称为
(2)一段时间后,关闭K2,打开K1,甲装置圆底烧瓶内发生反应的化学方程式为
(3)设计实验检验亚硫酸氢铵中阳离子,写出操作、现象及相应的结论:
II.另一化学兴趣小组同学利用下图装置探究氨的催化氧化,并测定氯化铵的纯度。取10.0g氯化铵样品(杂质不参加反应)与足量消石灰反应,将产生的气体全部通入下图装置,待完全反应后,E中质量增加了1.02g,通过测量的数据进行计算得出C中反应生成的水为0.18 mol。
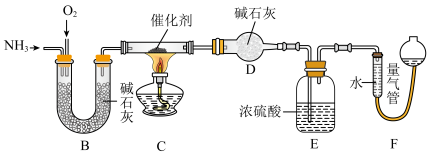
(5)计算氯化铵样品的纯度
您最近一年使用:0次
名校
解题方法
2 . I.汽车尾气中含有CO、NOx等有害气体。
(1)NOx能形成酸雨,氮有多种价态的氧化物,氮元素从+1~+5价都有对应的氧化物,常见的有N2O、NO、N2O3、NO2(或N2O4)、N2O5,其中属于酸性氧化物的是___________ 。
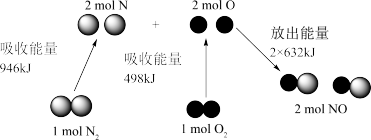
(2)汽车尾气中NO生成过程的能量变化示意图如下:___________ (填“吸热”或“放热”)___________ kJ的能量。
Ⅱ.目前工业上烟气脱硫脱硝的工艺流程如下: > 9)。
> 9)。
(3)“氧化”的目的是___________ 。图中产品中含硫成分为___________ (填化学式)。
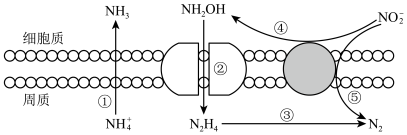
Ⅲ.海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。___________ 种价态。反应③和⑤中,若生成等物质的量的N2,则转移的电子数之比为___________ 。
Ⅳ.利用NaOH溶液吸收NO2,避免硝酸生产尾气中的氮氧化物对环境的破坏作用。
(5)已知用NaOH溶液吸收时会生成NaNO2和另一种盐,则吸收NO2的离子方程式为___________ 。
(1)NOx能形成酸雨,氮有多种价态的氧化物,氮元素从+1~+5价都有对应的氧化物,常见的有N2O、NO、N2O3、NO2(或N2O4)、N2O5,其中属于酸性氧化物的是
(2)汽车尾气中NO生成过程的能量变化示意图如下:
Ⅱ.目前工业上烟气脱硫脱硝的工艺流程如下:
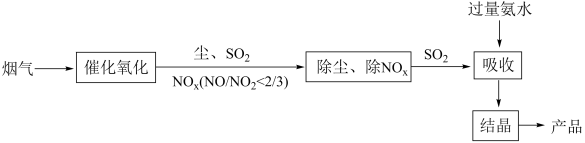
 > 9)。
> 9)。(3)“氧化”的目的是
Ⅲ.海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。
Ⅳ.利用NaOH溶液吸收NO2,避免硝酸生产尾气中的氮氧化物对环境的破坏作用。
(5)已知用NaOH溶液吸收时会生成NaNO2和另一种盐,则吸收NO2的离子方程式为
您最近一年使用:0次
名校
3 . 下表是元素周期表的一部分,请按要求回答下列问题:___________ 。
(2)写出⑥最高价氧化物的电子式___________ 。
(3)在②~⑤元素中,原子半径最大的是___________ (填元素符号)。
(4)比较④、⑤、⑥、⑦离子的半径大小___________ (用离子符号表示且用“>”连接)。
(5)以上这些元素中,最不活泼的金属元素是___________ (填元素符号),这些元素的最高价氧化物对应的水化物中,碱性最强的是___________ (填化学式)。
(6)砷(As)是人体必需的微量元素,与③同一主族,As原子比③原子多两个电子层,则砷在周期表中的位置为___________ ,该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是___________ (用化学式表示且用“>”连接)。

(2)写出⑥最高价氧化物的电子式
(3)在②~⑤元素中,原子半径最大的是
(4)比较④、⑤、⑥、⑦离子的半径大小
(5)以上这些元素中,最不活泼的金属元素是
(6)砷(As)是人体必需的微量元素,与③同一主族,As原子比③原子多两个电子层,则砷在周期表中的位置为
您最近一年使用:0次
名校
解题方法
4 . 可用如图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:___________ 。
(2)反应的化学方程式:___________ 。
(3)球形干燥管c的作用是___________ 。
(4)饱和Na2CO3溶液,其作用是___________ ,若反应前向饱和Na2CO3溶液中加入几滴石蕊,溶液呈蓝色,反应结束后b中的现象是___________ 。
(5)浓硫酸在该反应中的作用主要有___________ 作用,该作用能使乙酸乙酯的产量增加,从反应速率和平衡的角度解释其原因是___________ 。
(6)已知:CaCl2分别与H2O、NH3、C2H5OH反应生成CaCl2·6H2O、CaCl2·8NH3、CaCl2·6C2H5OH。乙酸乙酯粗产品精制提纯的流程如下。___________ (填序号,下同),试剂X为___________ ,操作2的名称是___________ 。
A.萃取 B.分液 C.过滤 D.蒸馏 E.浓硫酸 F.饱和氯化钙溶液 G.无水硫酸镁 H.无水氯化钙
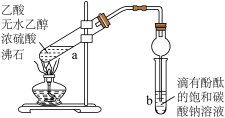
(2)反应的化学方程式:
(3)球形干燥管c的作用是
(4)饱和Na2CO3溶液,其作用是
(5)浓硫酸在该反应中的作用主要有
(6)已知:CaCl2分别与H2O、NH3、C2H5OH反应生成CaCl2·6H2O、CaCl2·8NH3、CaCl2·6C2H5OH。乙酸乙酯粗产品精制提纯的流程如下。
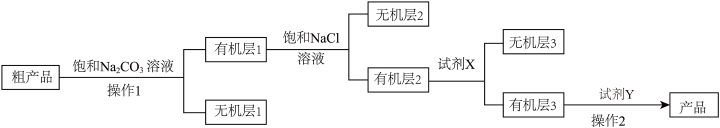
A.萃取 B.分液 C.过滤 D.蒸馏 E.浓硫酸 F.饱和氯化钙溶液 G.无水硫酸镁 H.无水氯化钙
您最近一年使用:0次
名校
5 . 某化学课外小组用如图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。___________ 。
(2)反应结束后,打开A下端的活塞,让反应液流入B中,充分振荡,目的是___________ 。
(3)C中盛放CCl4的作用是___________ 。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,请按要求填写下表。
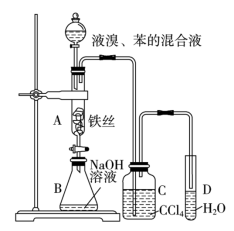
(2)反应结束后,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(3)C中盛放CCl4的作用是
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,请按要求填写下表。
| 向试管D中加入的试剂 | |
| 方法一 | |
| 方法二 |
您最近一年使用:0次
名校
解题方法
6 . 根据要求回答问题
(1)已知:键线式要点
a.分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略
b.环形结构用相应边数的多边形来表示
c.杂原子(非碳、氢原子)不得省略,并且其上连有的氢也不省略
①一氯甲烷生成二氯甲烷___________ 。
②乙烯通入溴水中___________ 。
③苯的硝化___________ 。
④苯和氢气___________ 。
(3)已知有机物有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C10H14O4,试回答下列有关问题。 R-OH+NaX (R-表示烃基,X表示卤原子)。
R-OH+NaX (R-表示烃基,X表示卤原子)。
①A的分子式为___________ 。
②G的结构简式为___________ 。
③反应E→F的反应类型:___________ ,B+F→G的反应类型:___________ 。
④C生成D的化学方程式:___________ ;D生成E的化学方程式:___________ ;A生成B的化学方程式:___________ 。
(1)已知:键线式要点
a.分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略
b.环形结构用相应边数的多边形来表示
c.杂原子(非碳、氢原子)不得省略,并且其上连有的氢也不省略
①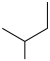 的系统命名为
的系统命名为 的名称为
的名称为
②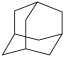 (四个等同的六元环组成)的分子式为
(四个等同的六元环组成)的分子式为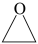 的分子式为
的分子式为
①一氯甲烷生成二氯甲烷
②乙烯通入溴水中
③苯的硝化
④苯和氢气
(3)已知有机物有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C10H14O4,试回答下列有关问题。
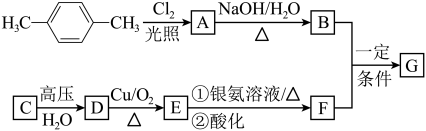
 R-OH+NaX (R-表示烃基,X表示卤原子)。
R-OH+NaX (R-表示烃基,X表示卤原子)。①A的分子式为
②G的结构简式为
③反应E→F的反应类型:
④C生成D的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有___________ 。
(2)要加快上述实验中气体产生的速率,还可采取的措施有___________ (写两种)。
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间。
①请完成此实验设计,其中:V1=___________ ,V6=___________ ,V9=___________ 。
②反应一段时间后,实验A中的金属呈___________ 色,实验E中的金属呈___________ 色。
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率变化的主要原因:___________ 。
(1)上述实验中发生反应的离子方程式有
(2)要加快上述实验中气体产生的速率,还可采取的措施有
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间。
| 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4溶液/mL | 40 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②反应一段时间后,实验A中的金属呈
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率变化的主要原因:
您最近一年使用:0次
8 . 某化学研究性学习小组利用以下装置制取并探究氨气的性质,回答下列问题:___________ 。
(2)B装置中的干燥剂成分是___________ 。气流通过C、D装置时候分别观察到的现象:C. ___________ 、D.___________ 。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到E装置中的现象是产生___________ 。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是___________ (填“F”或“G”)。

(2)B装置中的干燥剂成分是
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到E装置中的现象是产生
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是
您最近一年使用:0次
名校
9 . 如下图所示,A是酒的主要成分,D为具有果香的无色油状液体。由A到D的转化如图,请回答下列问题:___________ ,该反应类型为___________ 反应。
(2)请写出由A生成B的化学反应方程式___________ ,B中所含官能团的名称是___________ 该反应类型为___________ 反应。
(3)C的结构简式为___________ ,C与 互为
互为___________ 。
(4)写出A与C反应生成D的化学反应方程式___________ 。
(5)油脂和物质D具有相同官能团,下列物质中不属于油脂的是___________ 。

(2)请写出由A生成B的化学反应方程式
(3)C的结构简式为
 互为
互为(4)写出A与C反应生成D的化学反应方程式
(5)油脂和物质D具有相同官能团,下列物质中不属于油脂的是
| A.花生油 | B.石蜡油 | C.棉籽油 | D.牛油 |
您最近一年使用:0次
名校
10 . 某化学兴趣小组为检验木炭和浓硫酸反应生成的产物,设计如图装置,请回答:___________ ;盛装碳粉的仪器的名称是___________ 。
(2)上述装置接口的连接顺序为a→___________ 。
(3)写出木炭和浓硫酸发生反应的化学方程式___________ 。
(4)U形管中现象是___________ ,证明产物中有___________ (填化学式)。
(5)酸性KMnO4溶液的作用是___________ 。
(6)澄清石灰水的作用是___________ 。
(7)写出SO2与酸性KMnO4反应的离子方程式___________ 。
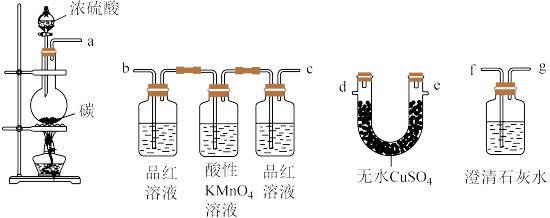
(2)上述装置接口的连接顺序为a→
(3)写出木炭和浓硫酸发生反应的化学方程式
(4)U形管中现象是
(5)酸性KMnO4溶液的作用是
(6)澄清石灰水的作用是
(7)写出SO2与酸性KMnO4反应的离子方程式
您最近一年使用:0次



