名校
1 . 下列离子方程式正确的是
A.向次氯酸钙溶液中通入 : : |
B.向硅酸钠溶液中加入醋酸: |
C.同浓度同体积 溶液与NaOH溶液混合: 溶液与NaOH溶液混合: |
D.过量铁粉加入稀硝酸中: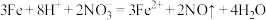 |
您最近一年使用:0次
名校
解题方法
2 . 下列图示与对应的叙述相符的是
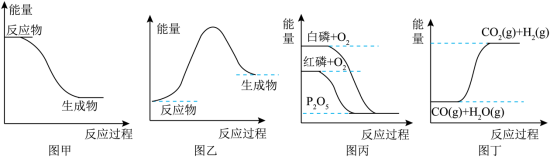
| A.图甲代表浓H2SO4稀释过程中体系的能量变化 |
| B.图乙表示反应物断键吸收的能量小于生成物成键放出的能量 |
| C.图丙表示白磷比红磷稳定 |
| D.图丁表示CO与H2O的反应是吸热反应 |
您最近一年使用:0次
名校
解题方法
3 . 用 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:
①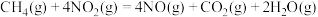

②

下列说法错误的是
 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:①
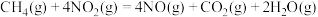

②


下列说法错误的是
| A.反应①②中,相同物质的量的甲烷发生反应,转移的电子数相同。 |
B.若用标准状况下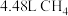 还原 还原 生成 生成 、 、 和 和 ,则放出的热量为 ,则放出的热量为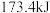 。 。 |
C.由反应①可知:  。 。 |
D.已知 的燃烧热为 的燃烧热为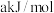 ,由 ,由 组成的混合物 组成的混合物 ,完全燃烧并恢复到常温时放出的热量为 ,完全燃烧并恢复到常温时放出的热量为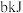 ,则 ,则 的燃烧热为 的燃烧热为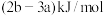 。 。 |
您最近一年使用:0次
2024-05-21更新
|
125次组卷
|
4卷引用: 重庆市第一中学校2022-2023学年高一下学期期中考试化学试题
解题方法
4 . 回答下列问题
(1)有下列物质① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ,其中含非极性键的离子化合物有
,其中含非极性键的离子化合物有________ (用物质前的序号填空,下同),只含共价键的物质有______ ,熔化时只破坏范德华力的是____________ 。
(2)硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图,图2是硫元素的“价类二维图”,回答下列问题: 均为图1中的物质,写出X与Y反应的化学方程式
均为图1中的物质,写出X与Y反应的化学方程式__________ 。
②芒硝的化学式为_________ 。
③工业制硫酸时, 参与的化学方程式为
参与的化学方程式为______________ 。
(3)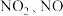 是大气污染物的主要成分,可以用
是大气污染物的主要成分,可以用 溶液吸收,当
溶液吸收,当 与
与 的体积比为
的体积比为 时,所得
时,所得 与
与 的物质的量之比为
的物质的量之比为_________ .用 也能处理
也能处理 和
和 ,反应原理如图所示,当
,反应原理如图所示,当 与
与 的物质的量之比为
的物质的量之比为 ,写出相应的化学方程式
,写出相应的化学方程式______ 。
(1)有下列物质①
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ,其中含非极性键的离子化合物有
,其中含非极性键的离子化合物有(2)硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图,图2是硫元素的“价类二维图”,回答下列问题:

 均为图1中的物质,写出X与Y反应的化学方程式
均为图1中的物质,写出X与Y反应的化学方程式②芒硝的化学式为
③工业制硫酸时,
 参与的化学方程式为
参与的化学方程式为(3)
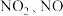 是大气污染物的主要成分,可以用
是大气污染物的主要成分,可以用 溶液吸收,当
溶液吸收,当 与
与 的体积比为
的体积比为 时,所得
时,所得 与
与 的物质的量之比为
的物质的量之比为 也能处理
也能处理 和
和 ,反应原理如图所示,当
,反应原理如图所示,当 与
与 的物质的量之比为
的物质的量之比为 ,写出相应的化学方程式
,写出相应的化学方程式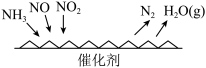
您最近一年使用:0次
5 . 回答下列问题
(1)浓硫酸是重要的化工原料,有其特殊的性质,某实验小组用如图所示的装置探究铜与浓硫酸的反应.___________ ,该反应中浓硫酸表现_________ 性;
②用可抽动铜丝替代铜片的优点是__________ ;
③若用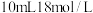 的浓硫酸与足量的铜反应,得到
的浓硫酸与足量的铜反应,得到 的质量范围为
的质量范围为_________ 。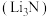 是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知:
是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知: 与
与 在加热条件下反应生成氮气)
在加热条件下反应生成氮气)
①写出 与水反应的化学方程式
与水反应的化学方程式___________ ;
②开始实验时,应该先点燃_____ (填“A”或“C”)处酒精灯;
③实验结束后,发现产品中混有少量 ,产生该杂质的原因可能为
,产生该杂质的原因可能为________ ;
④测 的纯度:取
的纯度:取 粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重
粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重 ,则产品中
,则产品中 的百分含量为
的百分含量为________ (保留三位有效数字)。
(1)浓硫酸是重要的化工原料,有其特殊的性质,某实验小组用如图所示的装置探究铜与浓硫酸的反应.
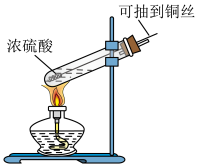
②用可抽动铜丝替代铜片的优点是
③若用
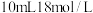 的浓硫酸与足量的铜反应,得到
的浓硫酸与足量的铜反应,得到 的质量范围为
的质量范围为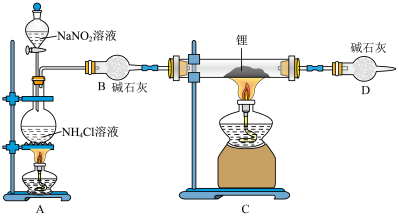
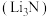 是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知:
是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知: 与
与 在加热条件下反应生成氮气)
在加热条件下反应生成氮气)①写出
 与水反应的化学方程式
与水反应的化学方程式②开始实验时,应该先点燃
③实验结束后,发现产品中混有少量
 ,产生该杂质的原因可能为
,产生该杂质的原因可能为④测
 的纯度:取
的纯度:取 粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重
粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重 ,则产品中
,则产品中 的百分含量为
的百分含量为
您最近一年使用:0次
解题方法
6 . 用锰废料(含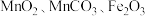 和少量
和少量 )制备
)制备 的工艺流程如下:
的工艺流程如下:
(1)流程中将锰废料粉碎的原因是_________ 。
(2)通入 时,
时, 发生还原反应,此时发生反应的化学方程式为
发生还原反应,此时发生反应的化学方程式为__________ ,能证明“吸收”后上层清液中没有 的试剂为
的试剂为_________ 。
(3)加入 的目的是将
的目的是将 氧化成
氧化成 ,写出“氧化”时的离子方程式
,写出“氧化”时的离子方程式________ ,所得“滤渣”的主要成分为_________ 。
(4)“化浆”操作中,________ (填“能”或“不能”)将稀硫酸换成稀盐酸;
(5)“转化”过程中,只有锰元素变价,则氧化剂与还原剂的物质的量之比为____ 。
(6)“系列操作”是过滤、洗涤、干燥,证明 洗涤干净的操作为
洗涤干净的操作为______ 。
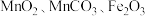 和少量
和少量 )制备
)制备 的工艺流程如下:
的工艺流程如下: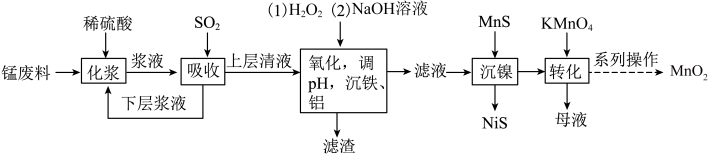
(1)流程中将锰废料粉碎的原因是
(2)通入
 时,
时, 发生还原反应,此时发生反应的化学方程式为
发生还原反应,此时发生反应的化学方程式为 的试剂为
的试剂为(3)加入
 的目的是将
的目的是将 氧化成
氧化成 ,写出“氧化”时的离子方程式
,写出“氧化”时的离子方程式(4)“化浆”操作中,
(5)“转化”过程中,只有锰元素变价,则氧化剂与还原剂的物质的量之比为
(6)“系列操作”是过滤、洗涤、干燥,证明
 洗涤干净的操作为
洗涤干净的操作为
您最近一年使用:0次
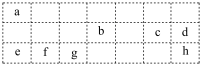
7 . 下表是元素周期表中主族的一部分,其中c是地壳中含量最多的元素,回答下列问题:__________ , 的结构式为
的结构式为___________ 。
(2)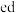 为
为__________ (填“离子”或“共价”)化合物,能证明该结论的实验依据为___________ .
(3)用电子式表示物质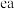 的形成过程
的形成过程__________________ ,该物质能与 反应生成
反应生成 ,反应中
,反应中 作
作________ 剂。
(4) 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为_________ (用化学式表示)。
(5)若 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: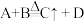 ,写出该反应的离子方程式
,写出该反应的离子方程式____________________ 。
(6)下列有关说法正确的是__________ 。
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用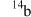 测定一些文物的年代
测定一些文物的年代
C.科学家常在 等元素区域寻找新型农药
等元素区域寻找新型农药
D.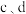 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
 的结构式为
的结构式为(2)
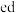 为
为(3)用电子式表示物质
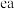 的形成过程
的形成过程 反应生成
反应生成 ,反应中
,反应中 作
作(4)
 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为(5)若
 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: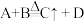 ,写出该反应的离子方程式
,写出该反应的离子方程式(6)下列有关说法正确的是
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用
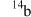 测定一些文物的年代
测定一些文物的年代C.科学家常在
 等元素区域寻找新型农药
等元素区域寻找新型农药D.
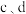 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
您最近一年使用:0次
8 .  是6种短周期元素组成的物质,各物质之间有如下转化关系.其中
是6种短周期元素组成的物质,各物质之间有如下转化关系.其中 是气体单质,E是一种理想的清洁能源,F是日常生活中常用金属,J是能使澄清石灰水变浑浊的无色无味气体,化合物
是气体单质,E是一种理想的清洁能源,F是日常生活中常用金属,J是能使澄清石灰水变浑浊的无色无味气体,化合物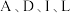 的焰色试验均显黄色,白色沉淀K既溶于H溶液,又能溶于D溶液.则下列说法正确的是
的焰色试验均显黄色,白色沉淀K既溶于H溶液,又能溶于D溶液.则下列说法正确的是
 是6种短周期元素组成的物质,各物质之间有如下转化关系.其中
是6种短周期元素组成的物质,各物质之间有如下转化关系.其中 是气体单质,E是一种理想的清洁能源,F是日常生活中常用金属,J是能使澄清石灰水变浑浊的无色无味气体,化合物
是气体单质,E是一种理想的清洁能源,F是日常生活中常用金属,J是能使澄清石灰水变浑浊的无色无味气体,化合物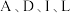 的焰色试验均显黄色,白色沉淀K既溶于H溶液,又能溶于D溶液.则下列说法正确的是
的焰色试验均显黄色,白色沉淀K既溶于H溶液,又能溶于D溶液.则下列说法正确的是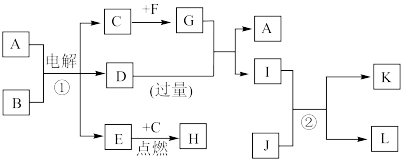
| A.常温条件下,F的单质不与浓硫酸反应,所以可用F制成的容器贮存浓硫酸 |
| B.反应①为氧化还原反应,反应②为非氧化还原反应 |
| C.E在C中燃烧时发出淡蓝色火焰 |
D.若A中含有杂质 ,可先后加入过量 ,可先后加入过量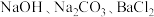 溶液,过滤除掉固体后,向滤液中加盐酸至 溶液,过滤除掉固体后,向滤液中加盐酸至 的方式除去 的方式除去 |
您最近一年使用:0次
9 . 已知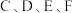 均含同种短周期元素,则下列说法不正确的是
均含同种短周期元素,则下列说法不正确的是

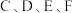 均含同种短周期元素,则下列说法不正确的是
均含同种短周期元素,则下列说法不正确的是
| A.若C是空气中含量最多的气体,则C到D的条件为点燃 | B.若F是一种强碱,则E有强氧化性 |
| C.若C为甲烷,则F溶液显弱酸性 | D.若F的浓溶液能使纸条变黑,则C可为黄色固体 |
您最近一年使用:0次
解题方法
10 . 为控制污染,工业上可以用 酸化的
酸化的 溶液吸收废气中的
溶液吸收废气中的 ,下列说法中不正确的是
,下列说法中不正确的是
 酸化的
酸化的 溶液吸收废气中的
溶液吸收废气中的 ,下列说法中不正确的是
,下列说法中不正确的是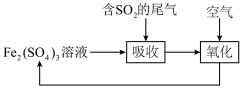
A.“吸收”过程中的离子反应方程式为: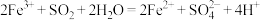 |
B.“氧化”过程中,可将空气换成 |
C. 可以循环使用 可以循环使用 |
D.吸收 含量为 含量为 (体积分数)的 (体积分数)的 的废气,至少需要通入相同条件下 的废气,至少需要通入相同条件下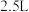 的空气(假设空气中 的空气(假设空气中 的体积分数为 的体积分数为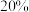 ) ) |
您最近一年使用:0次



