名校
1 . 下列化学事实不遵循 “量变引起质变”哲学思想的是
| A.铜丝分别与等体积的浓硝酸和稀硝酸反应,实验现象不同 |
| B.向蓝色石蕊试纸上滴加氯水,试纸先变为红色,后迅速褪色 |
| C.向氢氧化铁胶体中逐滴加入稀盐酸,先生成红褐色沉淀,后沉淀溶解 |
| D.浓盐酸与浓硝酸混合可得到溶解金和铂的“王水”,稀盐酸与稀硝酸混合不可溶解金和铂 |
您最近一年使用:0次
名校
2 . 根据实验操作及现象,下列结论中正确 的是
| 选项 | 实验操作及现象 | 结论 |
| A | 加热碳酸盐X使其分解,将产生的气体通入 溶液中,无明显现象 溶液中,无明显现象 | X可能为 |
| B | 向某无色溶液中通入过量的 气体,产生白色沉淀 气体,产生白色沉淀 | 该溶液中可能含有 |
| C | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入过量新制氯水后,溶液最终不显红色 | 该溶液中一定无 |
| D | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 某同学进行下列实验,下列说法正确的是
| 装置 | 操作 | 现象 |
| 将盛有浓盐酸的烧杯A放入盛有水玻璃的烧杯C中,然后将石灰石放入烧杯A后,立即用烧杯B罩住 | 烧杯A中固体溶解,有无色气泡产生,C中有白色胶状沉淀生成 |
A.C中发生反应的离子方程式一定是: |
| B.C中出现沉淀,表明碳元素的非金属性大于硅元素 |
| C.若将石灰石换成石墨粉,C中也会产生沉淀 |
| D.水玻璃的主要成分和硅酸都是离子化合物 |
您最近一年使用:0次
4 . 下列关于无机非金属材料说法正确的是
| A.高纯二氧化硅可用于制造太阳能电池 |
| B.硅酸盐中Si和O构成了硅氧四面体结构 |
| C.陶瓷、水晶、水泥、玻璃都属于硅酸盐 |
| D.水玻璃是纯净物,可用于生产黏合剂和防火剂 |
您最近一年使用:0次
名校
解题方法
5 . 已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温下,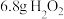 中的共价键数目为 中的共价键数目为 |
B.在标准状况下,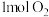 与1mol HF的体积相同 与1mol HF的体积相同 |
C.100g 46%的乙醇 溶液中含有氧原子数为 溶液中含有氧原子数为 |
D.44g二氧化碳中含共用电子对对数为 |
您最近一年使用:0次
名校
解题方法
6 . 化学与生活密切相关,下列说法正确的是
A.古陶瓷修复所用的熟石膏,其成分为 |
B. 可用于丝织品漂白是由于其能氧化丝织品中有色成分 可用于丝织品漂白是由于其能氧化丝织品中有色成分 |
| C.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化 |
| D.用激光笔照射牛奶可观察到丁达尔效应是由于胶体粒子对光线的散射 |
您最近一年使用:0次
名校
解题方法
7 . A~F六种元素中,除F外其他均为短周期元素,它们的原子结构或性质如下表所示。
请回答下列问题:(用对应的化学用语回答)
(1)B在元素周期表中的位置是___________ ;A和C形成供氧剂的电子式___________ 。
(2) A、C、D、E离子半径由小到大的顺序为___________ 。(用离子符号表示)
(3)F的某种氯化物的饱和溶液滴加到沸水中可以形成胶体,写出此反应的化学反应方程式:___________ 。
(4)A和C形成的供氧剂与C的氢化物反应的化学方程式是:___________ 。
(5)E的单质与A的最高价氧化物的水化物反应的离子方程式为___________ 。
(6)红热的B单质与D的最高价氧化物对应水化物的浓溶液反应的化学方程式:___________ 。
| 元素 | 原子结构或性质 |
| A | 原子的最外层电子数是电子层数的 ,其含氧化合物可作为供氧剂 ,其含氧化合物可作为供氧剂 |
| B | 其形成的一种同位素原子在考古中可推测化石的年代 |
| C | 地壳中含量最多的元素 |
| D | 其单质位于火山口附近 |
| E | 与D同周期,且最外层电子数等于电子层数 |
| F | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
(1)B在元素周期表中的位置是
(2) A、C、D、E离子半径由小到大的顺序为
(3)F的某种氯化物的饱和溶液滴加到沸水中可以形成胶体,写出此反应的化学反应方程式:
(4)A和C形成的供氧剂与C的氢化物反应的化学方程式是:
(5)E的单质与A的最高价氧化物的水化物反应的离子方程式为
(6)红热的B单质与D的最高价氧化物对应水化物的浓溶液反应的化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 某无色溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子,为确定其成分,现进行如下实验:
等离子,为确定其成分,现进行如下实验:
①取10mL该溶液于试管中,滴加足量稀硝酸酸化的 溶液后过滤得到0.03mol白色沉淀,向滤液中加入
溶液后过滤得到0.03mol白色沉淀,向滤液中加入 溶液无沉淀产生;
溶液无沉淀产生;
②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示。(不考虑沉淀、气体的溶解和损失)
 、
、 、
、 、
、 、
、 、
、 、
、 等离子,为确定其成分,现进行如下实验:
等离子,为确定其成分,现进行如下实验:①取10mL该溶液于试管中,滴加足量稀硝酸酸化的
 溶液后过滤得到0.03mol白色沉淀,向滤液中加入
溶液后过滤得到0.03mol白色沉淀,向滤液中加入 溶液无沉淀产生;
溶液无沉淀产生;②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示。(不考虑沉淀、气体的溶解和损失)

A.实验中使用的NaOH溶液的浓度为 |
| B.该溶液中存在的离子有3种 |
| C.可推测该溶液是硫酸铝铵的水溶液 |
D.另取一定量该溶液滴加0.03mol的 溶液可能使溶液中 溶液可能使溶液中 和 和 同时沉淀完全 同时沉淀完全 |
您最近一年使用:0次
名校
解题方法
9 . 可逆反应 在不同条件下的反应速率最大的是
在不同条件下的反应速率最大的是
 在不同条件下的反应速率最大的是
在不同条件下的反应速率最大的是A.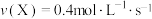 | B. |
C.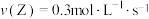 | D. |
您最近一年使用:0次
名校
解题方法
10 . 材料是经济增长与社会发展的重要物质基础,请回答下列问题。
(1)硅是重要的半导体材料,广泛应用于电子产品领域,工业上以硅石 为原料制备冶金级高纯硅的工艺流程如图所示:
为原料制备冶金级高纯硅的工艺流程如图所示: 室温下为易挥发、易水解的无色液体。
室温下为易挥发、易水解的无色液体。
①写出上述过程中氧化过程的化学方程式:___________ ;
② 极易水解且生成某种可燃性气体,写出化学反应方程式:
极易水解且生成某种可燃性气体,写出化学反应方程式:___________ ;
③上述工艺生产中需要在无水、无氧的条件下进行的操作有:___________ 。
(2)某MOFs多孔材料能高选择性吸附 ,其孔径大小和形状恰好将
,其孔径大小和形状恰好将 “固定”。废气中的
“固定”。废气中的 被吸附后,经处理能全部转化为
被吸附后,经处理能全部转化为 。原理示意图如下。
。原理示意图如下。
①写出反应中转化为 的化学反应方程式
的化学反应方程式___________ ;
②每生成 时,氧化剂与还原剂的物质的量之比为
时,氧化剂与还原剂的物质的量之比为___________ 。
(3)甲醇是重要的化工原料之一,其制备和用途研究一直是化学工业热门研究方向。
工业上利用 和
和 合成甲醇,反应方程式为
合成甲醇,反应方程式为 ,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入
,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入 和
和 进行上述反应,测得
进行上述反应,测得 和
和 浓度随时间变化如图所示。
浓度随时间变化如图所示。 和
和 充分反应后,放出的能量
充分反应后,放出的能量___________ (填“>”“<”或“=”)89kJ;
②从0到10min,
___________ ;
③达到平衡时 的体积分数
的体积分数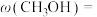
___________ 。
(1)硅是重要的半导体材料,广泛应用于电子产品领域,工业上以硅石
 为原料制备冶金级高纯硅的工艺流程如图所示:
为原料制备冶金级高纯硅的工艺流程如图所示: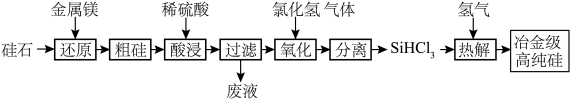
 室温下为易挥发、易水解的无色液体。
室温下为易挥发、易水解的无色液体。①写出上述过程中氧化过程的化学方程式:
②
 极易水解且生成某种可燃性气体,写出化学反应方程式:
极易水解且生成某种可燃性气体,写出化学反应方程式:③上述工艺生产中需要在无水、无氧的条件下进行的操作有:
(2)某MOFs多孔材料能高选择性吸附
 ,其孔径大小和形状恰好将
,其孔径大小和形状恰好将 “固定”。废气中的
“固定”。废气中的 被吸附后,经处理能全部转化为
被吸附后,经处理能全部转化为 。原理示意图如下。
。原理示意图如下。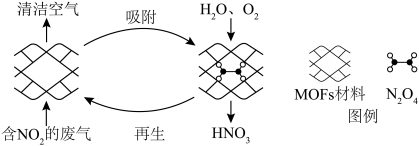

①写出反应中转化为
 的化学反应方程式
的化学反应方程式②每生成
 时,氧化剂与还原剂的物质的量之比为
时,氧化剂与还原剂的物质的量之比为(3)甲醇是重要的化工原料之一,其制备和用途研究一直是化学工业热门研究方向。
工业上利用
 和
和 合成甲醇,反应方程式为
合成甲醇,反应方程式为 ,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入
,每生成1mol甲醇反应放出89kJ的能量,在一恒温恒容密闭容器中充入 和
和 进行上述反应,测得
进行上述反应,测得 和
和 浓度随时间变化如图所示。
浓度随时间变化如图所示。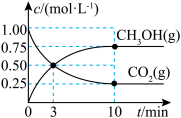
 和
和 充分反应后,放出的能量
充分反应后,放出的能量②从0到10min,

③达到平衡时
 的体积分数
的体积分数
您最近一年使用:0次




