1 . 我国科学家开发出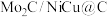 催化剂,设计了新型
催化剂,设计了新型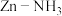 电池,实现高效、连续的
电池,实现高效、连续的 到
到 的转化,装置如图所示。下列叙述错误的是
的转化,装置如图所示。下列叙述错误的是
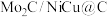 催化剂,设计了新型
催化剂,设计了新型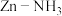 电池,实现高效、连续的
电池,实现高效、连续的 到
到 的转化,装置如图所示。下列叙述错误的是
的转化,装置如图所示。下列叙述错误的是
A.放电时,电极电势: |
B.充电时,a极反应式为 |
C.放电时,生成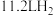 (标准状况)时,有 (标准状况)时,有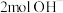 向a极迁移 向a极迁移 |
D.充电时,b极净增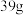 时,电路中转移 时,电路中转移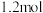 电子 电子 |
您最近一年使用:0次
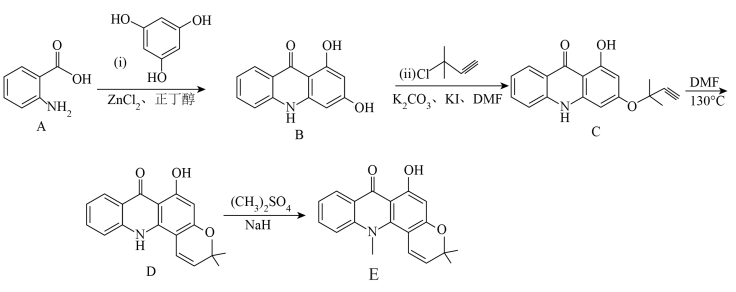
2 . 有机物E是一种广谱抗癌药,一种合成路线如下:
(1)A中所含官能团的名称是_____ 。
(2)B→C中 的作用是
的作用是_____ 。D→E的反应类型是_____ 。
(3)1moli与足量溴水反应,最多消耗_____ 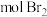 。
。
(4)写出A→B的化学方程式:_____ 。
(5)在A的芳香族同分异构体中,苯环上直接连—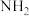 且能发生银镜反应的物质有
且能发生银镜反应的物质有_____ 种(不考虑立体异构),其中核磁共振氢谱上有四组峰且峰面积比为1:2:2:2的结构简式为_____ 。
(6)设计以苯酚和1,3-丁二烯为原料合成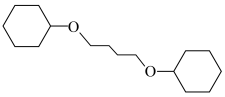 的路线
的路线_____ (其他试剂任选)。
(1)A中所含官能团的名称是
(2)B→C中
 的作用是
的作用是(3)1moli与足量溴水反应,最多消耗
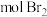 。
。(4)写出A→B的化学方程式:
(5)在A的芳香族同分异构体中,苯环上直接连—
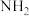 且能发生银镜反应的物质有
且能发生银镜反应的物质有(6)设计以苯酚和1,3-丁二烯为原料合成
 的路线
的路线
您最近一年使用:0次
解题方法
3 . 下列离子方程式正确的是
A.向稀硫酸中加入熟石灰: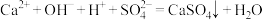 |
B.向含 的废水中加入 的废水中加入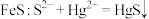 |
C.向 溶液中滴加少量 溶液中滴加少量 溶液: 溶液: |
D. 溶于稀硝酸: 溶于稀硝酸: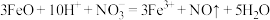 |
您最近一年使用:0次
解题方法
4 . 近日,我国科学家根据Co3O4在HZSM-5载体上的单层分散行为设计催化剂用于NH3选择性还原NOx。
已知:①
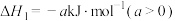
②
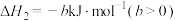
回答下列问题:
(1)反应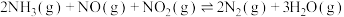 的
的
_____  。
。
(2)一定温度下,在恒容密闭容器中充入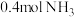 和
和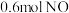 ,发生反应①。下列叙述正确的是_____(填字母)。
,发生反应①。下列叙述正确的是_____(填字母)。
(3)在恒容密闭容器中充入1molNO、2molNO2和4molNH3,在不同组成的催化剂作用下发生上述反应,相同时间内氮氧化物的转化率与温度关系如图所示。_____ 。
② 段变化的原因是
段变化的原因是_____ 。
③M点_____ (填“达到”或“未达到”)平衡状态,判断依据是_____ 。 段变化的原因可能是
段变化的原因可能是_____ 。
(4)一定温度下,在 恒容密闭容器中充入
恒容密闭容器中充入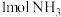 和
和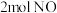 ,在催化剂作用下发生反应:①
,在催化剂作用下发生反应:① ;②
;②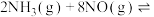
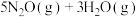 。达到平衡时,
。达到平衡时, 的转化率为
的转化率为 ,
, 的选择性为50%[
的选择性为50%[ 的选择性
的选择性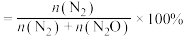 ]。则平衡时,
]。则平衡时, 的浓度为
的浓度为_____  ,该温度下,反应①的平衡常数
,该温度下,反应①的平衡常数
_____ (只列计算式即可):
已知:①

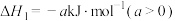
②

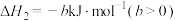
回答下列问题:
(1)反应
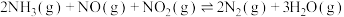 的
的
 。
。(2)一定温度下,在恒容密闭容器中充入
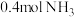 和
和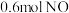 ,发生反应①。下列叙述正确的是_____(填字母)。
,发生反应①。下列叙述正确的是_____(填字母)。| A.混合气体的压强不随时间变化时达到平衡状态 |
B.达到平衡后,充入 ,平衡逆向移动,平衡常数减小 ,平衡逆向移动,平衡常数减小 |
C.达到平衡时,反应放出的热量为 |
| D.加入高效催化剂,达到平衡前,单位时间内NO的转化率增大 |
(3)在恒容密闭容器中充入1molNO、2molNO2和4molNH3,在不同组成的催化剂作用下发生上述反应,相同时间内氮氧化物的转化率与温度关系如图所示。

②
 段变化的原因是
段变化的原因是③M点
 段变化的原因可能是
段变化的原因可能是(4)一定温度下,在
 恒容密闭容器中充入
恒容密闭容器中充入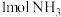 和
和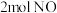 ,在催化剂作用下发生反应:①
,在催化剂作用下发生反应:① ;②
;②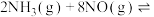
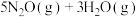 。达到平衡时,
。达到平衡时, 的转化率为
的转化率为 ,
, 的选择性为50%[
的选择性为50%[ 的选择性
的选择性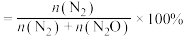 ]。则平衡时,
]。则平衡时, 的浓度为
的浓度为 ,该温度下,反应①的平衡常数
,该温度下,反应①的平衡常数
您最近一年使用:0次
解题方法
5 . 广泛用于火箭、原子能、电子工业等领域。以矿石(主要成分是Be2SiO4,含少量MnO等)为原料制备Be的工艺流程如图所示。
(1)“烧结”之前,将铍矿石粉碎成粉末,其目的是_____ 。
(2)“除锰”时发生反应的离子方程式为_____ 。“除锰”时温度不宜过高,原因是_____ 。
(3)制备无水 过程如下:将
过程如下:将 溶于盐酸,蒸发浓缩、冷却结晶得到
溶于盐酸,蒸发浓缩、冷却结晶得到 ;加热
;加热 和
和 的混合物得到无水
的混合物得到无水 ,该化学方程式为
,该化学方程式为_____ 。也可以用 固体替代
固体替代 ,
, 的作用是
的作用是_____ 。
(4)1828年德国化学家维勒用金属钾还原熔融的氯化铍而得到 。若将这个反应设计成原电池,则在电池的
。若将这个反应设计成原电池,则在电池的_____ (填“正”或“负”)极得到Be。
(5)铍和铝的化学性质相似,下列叙述错误的是_____ (填字母)。
A.铍是一种轻金属,能与冷水反应
B.常温下,BeCl2溶液的pH<7
C.氧化铍的熔点高、耐酸碱腐蚀

(1)“烧结”之前,将铍矿石粉碎成粉末,其目的是
(2)“除锰”时发生反应的离子方程式为
(3)制备无水
 过程如下:将
过程如下:将 溶于盐酸,蒸发浓缩、冷却结晶得到
溶于盐酸,蒸发浓缩、冷却结晶得到 ;加热
;加热 和
和 的混合物得到无水
的混合物得到无水 ,该化学方程式为
,该化学方程式为 固体替代
固体替代 ,
, 的作用是
的作用是(4)1828年德国化学家维勒用金属钾还原熔融的氯化铍而得到
 。若将这个反应设计成原电池,则在电池的
。若将这个反应设计成原电池,则在电池的(5)铍和铝的化学性质相似,下列叙述错误的是
A.铍是一种轻金属,能与冷水反应
B.常温下,BeCl2溶液的pH<7
C.氧化铍的熔点高、耐酸碱腐蚀
您最近一年使用:0次
6 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X、Q为同主族元素且这两种元素能组成离子化合物,Y元素的气态氢化物溶于水呈碱性。下列说法正确的是
| A.简单氢化物的稳定性:W>Z | B.简单离子半径:Q>Z>W |
| C.元素最高正价:W>Y>Q | D.X、Y、Z只能组成共价化合物 |
您最近一年使用:0次
解题方法
7 . 烯烃的加氢甲酰化反应是醛合成中重要的均相催化工业反应之一。我国科学家利用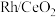 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: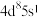 ,位于周期表第五周期第
,位于周期表第五周期第_____ 族,位于_____ 区。
(2)基态O原子核外电子有_____ 种不同的空间运动状态。
(3)乙中C原子的杂化类型是_____ 。
(4)丙分子中所含元素电负性由大到小顺序为_____ 。丙分子有_____ 个手性碳原子。
(5)已知: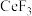 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是_____ 。
(6) 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。_____ 。该晶体密度为_____  。
。
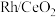 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: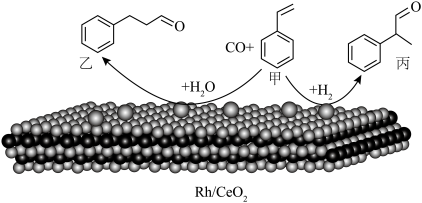
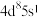 ,位于周期表第五周期第
,位于周期表第五周期第(2)基态O原子核外电子有
(3)乙中C原子的杂化类型是
(4)丙分子中所含元素电负性由大到小顺序为
(5)已知:
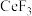 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是(6)
 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。
 。
。
您最近一年使用:0次
解题方法
8 . 化学与人类的生活密切相关。下列叙述错误的是
| A.食醋中含有的乙酸属于弱电解质 |
| B.钡盐对人体无害,硫酸钡可用于肠胃检查 |
| C.包装食品的塑料盒属于合成高分子材料 |
| D.煤炭燃烧时发生放热反应 |
您最近一年使用:0次
解题方法
9 . 市售食用油中常添加叔丁基对苯二酚(TBHQ)作抗氧化剂。实验室制备 的原理为
的原理为 。
。
Ⅰ.在图1装置的三颈烧瓶中依次加入3.3g对苯二酚、5mL85%磷酸和15mL甲苯。
Ⅱ.用热水浴加热使三颈烧瓶中混合物升温至90℃,从仪器B中分批滴加4mL叔丁醇(密度为
 ),控制温度在90~95℃。滴加完毕(需15min),加热并搅拌20min,直至混合物中的固体全部溶解为止。
),控制温度在90~95℃。滴加完毕(需15min),加热并搅拌20min,直至混合物中的固体全部溶解为止。Ⅲ.趁热将反应物转入分液漏斗分出磷酸层,有机相转入烧瓶中,加入10mL水,进行水蒸气蒸馏(如图2)。蒸馏完毕,将烧瓶中剩余物趁热过滤(如图3),弃去不溶物。滤液转入烧杯中,若剩余液体体积不足10mL,应补加热水,使产物被热水提取。
Ⅳ.将滤液在冰水浴中冷却,析出白色晶体,抽滤,并用少量冷水洗涤两次,干燥。称量为3.0g。

| 物质 | 甲苯 | 对苯二酚 | 叔丁基对苯二酚 | 磷酸 | 甲苯与水的共沸物 |
| 熔点/℃ | -94 | 175.5 | 128 | 42.35 | |
| 沸点/℃ | 110.63 | 286 | 295 | 213 | 84.1 |
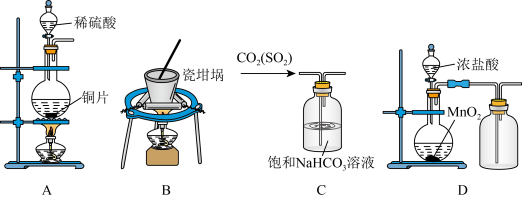
(1)图1中仪器B的名称是
A.
 B.
B.  C.
C.  D.
D. 
(2)实验中甲苯的作用是
(3)图2中水蒸气蒸馏的目的是
(4)步骤Ⅲ中趁热过滤的目的是
(5)若图3中锥形瓶内壁有白色晶体析出,可采取的措施是
(6)该实验的产率为
 (保留三位有效数字)。
(保留三位有效数字)。
您最近一年使用:0次


 中的
中的


