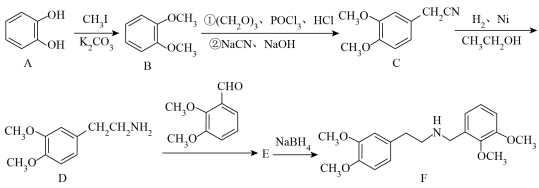
1 . 延胡索乙素具有镇痛及催眠作用,其中间体F的合成路线如图。回答下列问题: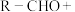 H2NR′
H2NR′ NR′(R为烃基,R′为烃基或H)
NR′(R为烃基,R′为烃基或H)_______ ,A→B的反应类型为_______ 。
(2)已知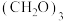 为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为
为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为_______ 。
(3)D中官能团的名称为_______ ,D中碳原子的杂化方式为_______ 。
(4)反应C→D的化学方程式为_______ 。
(5)已知化合物M是 的芳香族同分异构体,则符合下列条件的M的结构有
的芳香族同分异构体,则符合下列条件的M的结构有_____ 种。
①苯环上只有2个取代基;
②能与 溶液发生显色反应;
溶液发生显色反应;
③能发生水解反应。
(6)参照上述合成路线,以苯和乙醇为原料,设计合成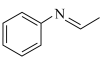 的路线:
的路线:_______ 。(无机试剂任选)
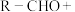 H2NR′
H2NR′ NR′(R为烃基,R′为烃基或H)
NR′(R为烃基,R′为烃基或H)②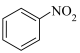


(2)已知
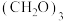 为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为
为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为(3)D中官能团的名称为
(4)反应C→D的化学方程式为
(5)已知化合物M是
 的芳香族同分异构体,则符合下列条件的M的结构有
的芳香族同分异构体,则符合下列条件的M的结构有①苯环上只有2个取代基;
②能与
 溶液发生显色反应;
溶液发生显色反应;③能发生水解反应。
(6)参照上述合成路线,以苯和乙醇为原料,设计合成
 的路线:
的路线:
您最近一年使用:0次
昨日更新
|
307次组卷
|
3卷引用:2024届云南省德宏师范高等专科学校附属天成中学高三下学期全真第三次模拟测理综试卷-高中化学
2024届云南省德宏师范高等专科学校附属天成中学高三下学期全真第三次模拟测理综试卷-高中化学广西南宁市2024届高三下学期二模考试化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题
名校
解题方法
2 . 一种含Pt催化剂催化甲烷中的碳氢键活化的反应机理如图所示。下列有关说法正确的是
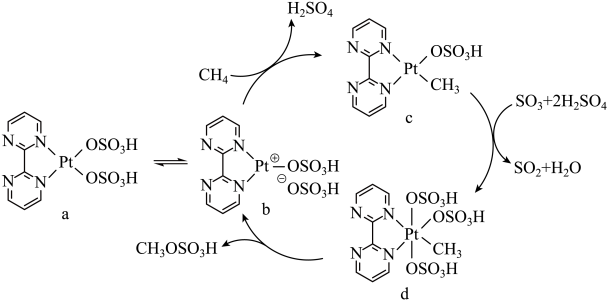
| A.SO2和SO3都是极性分子 | B.SO3是中间产物 |
| C.c→d的反应是氧化还原反应 | D.催化循环中Pt的配位数不改变 |
您最近一年使用:0次
昨日更新
|
129次组卷
|
3卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三下学期适应性月考(九)理综试卷-高中化学
名校
解题方法
3 . LiDFOB是一种新型的电解质锂盐,被广泛用于目前的锂电池中。LiDFOB的结构如图所示,其中元素M、X、Y、Z位于同一短周期且原子序数依次增大,X原子核外的s轨道与p轨道上的电子数之比为2:1,下列叙述正确的是
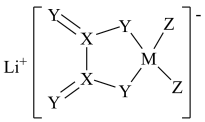
| A.基态Z原子核外有5种能量不同的电子 |
| B.该化合物中有极性键、非极性键、配位键和离子键 |
| C.第一电离能:Z>X>Y>M |
| D.M、X、Y、Z中,Z的最高价氧化物对应的水化物酸性最强 |
您最近一年使用:0次
昨日更新
|
142次组卷
|
3卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三下学期适应性月考(九)理综试卷-高中化学
解题方法
4 . 化学与生活联系紧密,下列说法正确的是
A.熟石膏可用于制作医用石膏绷带,其主要成分为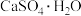 |
| B.用于制作塑料包扎绳的聚丙烯,可使酸性高锰酸钾溶液褪色 |
| C.酒精能使蛋白质变性,生活中常用95%酒精消毒 |
| D.烷基磺酸根离子等表面活性剂同时具有亲水基团和疏水基团,可用于除去油污 |
您最近一年使用:0次
昨日更新
|
117次组卷
|
2卷引用:2024届云南省德宏师范高等专科学校附属天成中学高三下学期全真第三次模拟测理综试卷-高中化学
名校
解题方法
5 . 碳酸锶(SrCO3)主要用于电子工业的磁性材料。以天青石(主要成分为:SrSO4,含有BaO、CaO、MgO、FeO、Fe2O3、Al2O3、SiO2等杂质)为原料制备SrCO3的一种工艺流程如下: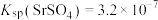 ,
,
② 、
、 在100g水中的溶解度如下表:
在100g水中的溶解度如下表:
回答下列问题:
(1)“转化”中主要是SrSO4(s)转化为SrCO3(s),该反应的离子方程式为______ ,其平衡常数K=______ 。
(2)“酸溶”后,滤渣1的主要成分为______ 和BaSO4;“除钡”时,若所用硫酸浓度较大,其后果是______ 。
(3)Fe2+被NaClO3氧化为Fe3+的离子方程式为______ ;与H2O2比较,用NaClO3为氧化剂的优点是铁、铝沉淀时颗粒较大,不易形成胶体,原因是______ 。
(4)“除钙镁”时,为提高钙去除率且避免锶沉淀损失,适宜的温度为______ 。
(5)Sr的原子序数为38,位于元素周期表第______ 周期第______ 族;已知:SrCO3晶体的密度为3.76g/cm3,晶胞参数: ,
, ,
, ,
, 。SrCO3晶胞中含有Sr2+数目的计算式为
。SrCO3晶胞中含有Sr2+数目的计算式为______ 。

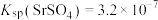 ,
,
②
 、
、 在100g水中的溶解度如下表:
在100g水中的溶解度如下表:温度/℃ | 20 | 60 | 80 | 90 |
| 0.69 | 3.13 | 7.03 | 13.60 |
| 0.165 | 0.116 | 0.094 | 0.085 |
(1)“转化”中主要是SrSO4(s)转化为SrCO3(s),该反应的离子方程式为
(2)“酸溶”后,滤渣1的主要成分为
(3)Fe2+被NaClO3氧化为Fe3+的离子方程式为
(4)“除钙镁”时,为提高钙去除率且避免锶沉淀损失,适宜的温度为
(5)Sr的原子序数为38,位于元素周期表第
 ,
, ,
, ,
, 。SrCO3晶胞中含有Sr2+数目的计算式为
。SrCO3晶胞中含有Sr2+数目的计算式为
您最近一年使用:0次
2024·云南昆明·三模
6 . 充分利用钴资源具有重要意义。以某湿法炼锌厂产出的高钴渣(含Co、Zn、Pb、Cu、Fe、Cd、Mn等金属元素)为原料回收钴和锰的一种工艺流程如下:
①除Cd后的滤液中含有 和
和 ;
;
②pH<3.7时, 还原性小于
还原性小于 ,pH>3.7时,
,pH>3.7时, 还原性大于
还原性大于 ;
;
③部分金属离子形成氢氧化物完全沉淀的pH如下表:
④不同pH下, 被
被 氧化的产物如下表:
氧化的产物如下表:
回答下列问题:
(1)滤渣1的主要成分为___________ (填化学式)。
(2)“沉铁”步骤中加入产品1的作用是___________ ,该步骤中调节pH的范围可以为___________ (填标号)。
a.pH<2.8 b.4.0<pH<4.5 c.8.2<pH<10.1
(3)Cd与Zn同族,“置换”步骤中发生反应的离子方程式为___________ 。
(4)“步骤3”中发生主要反应的离子方程式为___________ ,滤液中存在的主要金属离子除 外还有
外还有___________ (填离子符号)。
(5)沉淀前后 的浓度分别为
的浓度分别为 和
和 ,若溶液体积不变,则锰的沉淀率为
,若溶液体积不变,则锰的沉淀率为___________ %(保留小数点后两位)。

①除Cd后的滤液中含有
 和
和 ;
;②pH<3.7时,
 还原性小于
还原性小于 ,pH>3.7时,
,pH>3.7时, 还原性大于
还原性大于 ;
;③部分金属离子形成氢氧化物完全沉淀的pH如下表:
| 金属离子 |  |  |  |  |  |
| 完全沉淀的pH | 8.3 | 3.2 | 8.7 | 8.2 | 10.1 |
 被
被 氧化的产物如下表:
氧化的产物如下表:| pH | pH<3 | 3<pH<6 | 6<pH<6.2 |
 的氧化产物 的氧化产物 | 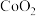 |  |  |
(1)滤渣1的主要成分为
(2)“沉铁”步骤中加入产品1的作用是
a.pH<2.8 b.4.0<pH<4.5 c.8.2<pH<10.1
(3)Cd与Zn同族,“置换”步骤中发生反应的离子方程式为
(4)“步骤3”中发生主要反应的离子方程式为
 外还有
外还有(5)沉淀前后
 的浓度分别为
的浓度分别为 和
和 ,若溶液体积不变,则锰的沉淀率为
,若溶液体积不变,则锰的沉淀率为
您最近一年使用:0次
7 . 氮化镓(GaN)是一种重要的半导体材料,用于制造高功率、高频率的电子器件。一种综合利用炼锌矿渣[主要含铁酸镓 、铁酸锌
、铁酸锌 、
、 ]制备GaN的工艺流程如图所示:
]制备GaN的工艺流程如图所示:
②常温下,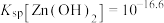 ,
,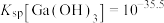 ,
, 。
。
③ 、
、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系如下表。
在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系如下表。
回答下列问题:
(1)基态Ga原子的价层电子排布式为___________ 。
(2)“酸浸”时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。“酸溶”所得滤渣的主要成分是___________ (填化学式)。
(3)“酸浸”所得浸出液中 、
、 浓度分别为0.21 g⋅L
浓度分别为0.21 g⋅L 、6.5 g⋅L
、6.5 g⋅L 。常温下,为尽可能多地提取
。常温下,为尽可能多地提取 并确保不混入
并确保不混入 ,用CaO“调pH”时须不大于
,用CaO“调pH”时须不大于___________ (假设调pH时溶液体积不变)。
(4)“反萃取”时,所用盐酸的浓度
___________ mol/L(选填上表中盐酸的浓度)。
(5)“沉镓”时,若加入NaOH的量过多,会导致 的沉淀率降低,原因是
的沉淀率降低,原因是___________ (用离子方程式表示)。
(6)利用CVD(化学气相沉积)技术,将热分解得到的 与
与 在高温下反应可制得GaN,同时生成另一种产物,该产物的电子式为:
在高温下反应可制得GaN,同时生成另一种产物,该产物的电子式为:___________ 。
(7)GaN晶体的一种立方晶胞如图所示,该晶胞中镓原子的配位数为___________ 。若该晶胞边长为a pm,则该晶胞密度为___________ g/cm (列出计算式,NA为阿伏加德罗常数的值)。
(列出计算式,NA为阿伏加德罗常数的值)。
 、铁酸锌
、铁酸锌 、
、 ]制备GaN的工艺流程如图所示:
]制备GaN的工艺流程如图所示:
②常温下,
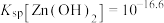 ,
,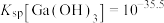 ,
, 。
。③
 、
、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系如下表。
在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系如下表。| 盐酸浓度/mol/L | 反萃取率/% | |
 |  | |
| 2.3 | 86.9 | 9.4 |
| 4.1 | 69.1 | 52.1 |
| 6.2 | 17.5 | 71.3 |
(1)基态Ga原子的价层电子排布式为
(2)“酸浸”时
 发生反应的离子方程式为
发生反应的离子方程式为(3)“酸浸”所得浸出液中
 、
、 浓度分别为0.21 g⋅L
浓度分别为0.21 g⋅L 、6.5 g⋅L
、6.5 g⋅L 。常温下,为尽可能多地提取
。常温下,为尽可能多地提取 并确保不混入
并确保不混入 ,用CaO“调pH”时须不大于
,用CaO“调pH”时须不大于(4)“反萃取”时,所用盐酸的浓度

(5)“沉镓”时,若加入NaOH的量过多,会导致
 的沉淀率降低,原因是
的沉淀率降低,原因是(6)利用CVD(化学气相沉积)技术,将热分解得到的
 与
与 在高温下反应可制得GaN,同时生成另一种产物,该产物的电子式为:
在高温下反应可制得GaN,同时生成另一种产物,该产物的电子式为:(7)GaN晶体的一种立方晶胞如图所示,该晶胞中镓原子的配位数为
 (列出计算式,NA为阿伏加德罗常数的值)。
(列出计算式,NA为阿伏加德罗常数的值)。
您最近一年使用:0次
8 . 化学实验源于生活。下列实验方案设计、现象与结论均正确的是
| 选项 | 实验目的 | 实验方案 | 现象和结论 |
| A | 检验葡萄糖中是否含有醛基 | 向葡萄糖溶液中滴加少量酸性高锰酸钾溶液,观察高锰酸钾溶液是否褪色 | 若溶液褪色,说明葡萄糖中含有醛基 |
| B | 比较常温下 和 和 溶度积的大小 溶度积的大小 | 向5 mL 0.2 mol/L NaOH溶液中滴加4滴0.2 mol/L  溶液,充分振荡,再滴加8滴0.2 mol/L 溶液,充分振荡,再滴加8滴0.2 mol/L  溶液 溶液 | 若溶液中出现白色沉淀,之后又出现蓝色沉淀,说明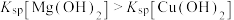 |
| C | 比较N和Cl的非金属性的强弱 | 分别取等浓度的 溶液和HClO溶液,用玻璃棒蘸取后点于pH试纸中部,与标准比色卡比较 溶液和HClO溶液,用玻璃棒蘸取后点于pH试纸中部,与标准比色卡比较 | 证明N的非金属性比Cl的弱 |
| D | 验证乙酸乙酯在碱性条件下可以水解 | 向盛有1mL乙酸乙酯的a、b两支试管中分别加入2 mL 、2 mL NaOH溶液,70~80℃热水浴 、2 mL NaOH溶液,70~80℃热水浴 | 若试管a液体分层,酯层无明显变化;试管b酯层消失,说明乙酸乙酯在碱性条件下可以水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 云南省博物馆中璀璨的历史文物,展示了云南各族人民在红土高原创造的厚重历史和辉煌文明,下列关于历史文物的说法不正确的是
| A.战国青铜器牛虎铜案是云南省博物馆的镇馆之宝,其硬度比纯铜大 |
| B.彝族五彩拼花绣花裙独具民族特色,其纺织材料棉和麻均为天然有机高分子 |
| C.宋大理国银鎏金镶珠金翅鸟充满勃勃生机,其采用的鎏金工艺利用了电解的原理 |
| D.建水紫陶刻填诗文梅花纹瓶工艺精湛,建水紫陶是一种传统无机硅酸盐材料 |
您最近一年使用:0次
2024·云南昆明·三模
10 . 2024年中国科学家首次提出了一种通过双中心催化(Pb和Cu作为电极材料)电解草酸( )和羟胺(
)和羟胺( )的混合溶液合成甘氨酸(
)的混合溶液合成甘氨酸( )的方法。其中,X电极区的反应原理示意图如下。下列说法正确的是
)的方法。其中,X电极区的反应原理示意图如下。下列说法正确的是

| A.X电极为阳极 |
| B.X电极区反应中存在极性键和非极性键的断裂与形成 |
C.当生成1mol 时,外电路中转移 时,外电路中转移 个电子 个电子 |
D.X电极区总反应: |
您最近一年使用:0次



