名校
解题方法
1 . 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。
Ⅰ.甲醇-水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓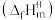 数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
则

_______  ,该反应在
,该反应在_______ (填“高温”“低温”或“任意温度”)下能自发进行。
Ⅱ.乙醇-水催化重整亦可获得,主要反应如下:
反应①: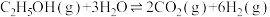
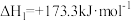
反应②:
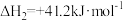
(2)向恒容密闭容器中充入1mol 和3mol
和3mol  发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时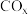 的分布分数
的分布分数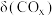 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。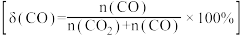
_______ (写出2条)。
②200℃以后,解释曲线a随温度变化趋势的原因:_______ 。
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内
___  ,该温度下,反应②的
,该温度下,反应②的
_______ (保留小数点后两位)。
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:_______ ,当转移1.2mol电子时,正极消耗的氧气的体积为_______ L(标准状况下)。
Ⅰ.甲醇-水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓
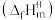 数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。| 物质 |  |  |  |  |
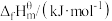 | 0 | -393.5 | -241.8 | -200.7 |


 ,该反应在
,该反应在Ⅱ.乙醇-水催化重整亦可获得,主要反应如下:
反应①:
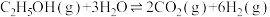
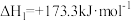
反应②:

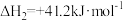
(2)向恒容密闭容器中充入1mol
 和3mol
和3mol  发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时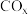 的分布分数
的分布分数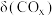 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。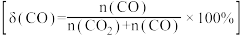

②200℃以后,解释曲线a随温度变化趋势的原因:
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内

 ,该温度下,反应②的
,该温度下,反应②的
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:

您最近一年使用:0次
昨日更新
|
95次组卷
|
2卷引用:辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷
名校
解题方法
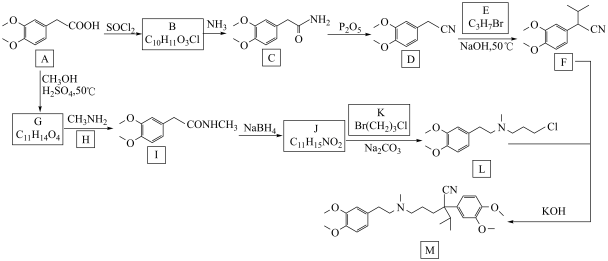
2 . 维拉帕米(化合物M)可以抗心律失常和抗心绞痛,广泛用于治疗原发性高血压。我国科学家设计了一条该化合物的新的合成路线,如下所示:___________ ,化合物B的结构简式为___________ 。
(2)上述合成路线中不涉及到的反应类型有___________ 。
A.取代反应 B.加成反应 C.消去反应 D.氧化反应 E.还原反应
(3)写出由G生成I的化学反应方程式___________ 。
(4)化合物C中官能团的名称为___________ 。
(5)化合物K参加反应时断裂碳溴键而不是碳氯键的理由是___________ 。
(6)化合物 中氮原子的杂化方式为
中氮原子的杂化方式为___________ ,其碱性___________  。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)
(7)满足下列条件的A的同分异构体有多种,任意写出其中一种结构简式___________ 。
①与FeCl3溶液反应显紫色,与过量Na2CO3反应的物质的量之比为1:2
②除苯环外无其它环,有两个手性碳且相邻
③核磁共振氢谱显示八组峰,且峰面积之比为
(2)上述合成路线中不涉及到的反应类型有
A.取代反应 B.加成反应 C.消去反应 D.氧化反应 E.还原反应
(3)写出由G生成I的化学反应方程式
(4)化合物C中官能团的名称为
(5)化合物K参加反应时断裂碳溴键而不是碳氯键的理由是
(6)化合物
 中氮原子的杂化方式为
中氮原子的杂化方式为 。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)(7)满足下列条件的A的同分异构体有多种,任意写出其中一种结构简式
①与FeCl3溶液反应显紫色,与过量Na2CO3反应的物质的量之比为1:2
②除苯环外无其它环,有两个手性碳且相邻
③核磁共振氢谱显示八组峰,且峰面积之比为

您最近一年使用:0次
3 . Wolff-Kishner-黄鸣龙还原反应机理如下(R、 均代表烃基),下列有关说法错误的是
均代表烃基),下列有关说法错误的是
 均代表烃基),下列有关说法错误的是
均代表烃基),下列有关说法错误的是
| A.肼的沸点高于氨气,原因是分子间氢键数目更多,且相对分子质量更大 |
| B.过程①发生加成反应,过程②、③均发生消去反应 |
C.过程④的反应历程可表示为 |
D.应用该机理, 可以在碱性条件下转变为 可以在碱性条件下转变为 |
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语表示正确的是
A.用电子式表示 的形成过程: 的形成过程: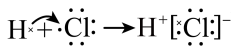 |
B.邻羟基苯甲醛分子内氢键示意图: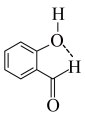 |
C. 的VSEPR构型为 的VSEPR构型为 |
D. 分子中 分子中 键的形成: 键的形成: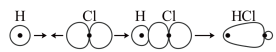 |
您最近一年使用:0次
5 . 化合物Z是一种药物合成中间体,其合成路线如下:
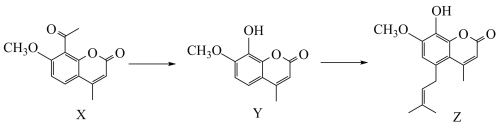
| A.X分子中只含有酮羰基、醚键两种含氧官能团 |
B. 与足量 与足量 溶液反应,消耗 溶液反应,消耗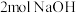 |
C.X与足量 反应后的产物有6个手性碳原子 反应后的产物有6个手性碳原子 |
D.Z可以与 在一定条件下发生缩聚反应 在一定条件下发生缩聚反应 |
您最近一年使用:0次
6 . 甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
反应I:

反应II:

已知:①平衡状态下,甲醛选择性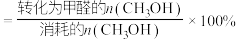 ;甲醛的收率
;甲醛的收率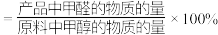 。
。
②几种物质的燃烧热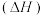 如下表:
如下表:
回答下列问题:
(1)
_______ ,HCHO的空间结构为_______ 形。
(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii: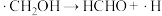
历程iii:
历程iv: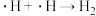
写出历程i的反应方程式:_______ 。
(3)将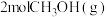 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示:_______ (填“I”或“II”),判断的依据是_______ 。
② ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为_______ ,
_______ ,反应I的平衡常数
_______  。
。
反应I:


反应II:


已知:①平衡状态下,甲醛选择性
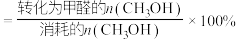 ;甲醛的收率
;甲醛的收率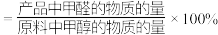 。
。②几种物质的燃烧热
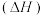 如下表:
如下表:| 物质 |  |  |  |  |
燃烧热 | -725.8 | -563.6 | -283.0 | -285.8 |
(1)

(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii:
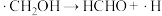
历程iii:

历程iv:
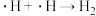
写出历程i的反应方程式:
(3)将
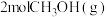 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示: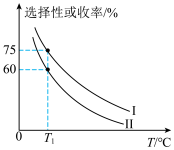
②
 ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为

 。
。
您最近一年使用:0次
昨日更新
|
143次组卷
|
3卷引用:2024届辽宁省沈阳市第二中学高三下学期三模化学试题
名校
解题方法
7 . 某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M为原子序数依次增大的短周期元素,W、X、Y、Z原子半径依次减小,且M的原子序数是Y的2倍。下列说法正确的是
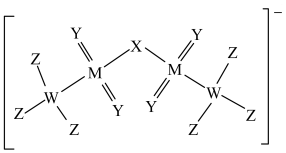
| A.同周期第一电离能大于Y的元素有1种 |
B.在配合物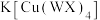 中,X提供孤电子对 中,X提供孤电子对 |
C.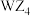 、 、 、 、 中心原子孤电子对数依次增多 中心原子孤电子对数依次增多 |
| D.氢化物的熔沸点大小顺序一定为W<X<Y |
您最近一年使用:0次
名校
解题方法
8 . 绿氢由于生产过程中100%绿色的特点备受青睐,发展前景最为广阔,光催化制氢机理研究取得新进展。如图是通过光催化循环在较低温度下由水分解制备氢气的反应原理。下列有关说法错误的是
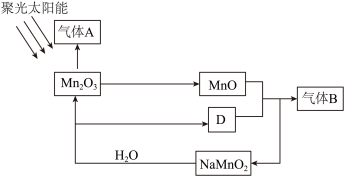
| A.该制氢过程中,消耗了水和太阳能,含锰化合物均为中间产物 |
| B.该制氢过程解决了气体A、B难分离的问题 |
| C.制氢过程中涉及Mn元素转化的反应不都是氧化还原反应 |
D.生成气体B的反应方程式为 |
您最近一年使用:0次
名校
解题方法
9 . 某新型能源材料由阳离子 、
、 和阴离子A-组成,该材料的晶胞如图所示,下列说法错误的是
和阴离子A-组成,该材料的晶胞如图所示,下列说法错误的是
 、
、 和阴离子A-组成,该材料的晶胞如图所示,下列说法错误的是
和阴离子A-组成,该材料的晶胞如图所示,下列说法错误的是
| A.该物质的化学式为X2YA4 |
| B.a=1,b=2 |
| C.A-离子周围最近且等距的A-离子有12个 |
| D.该晶体中,正四面体形空隙的填充率为36.5% |
您最近一年使用:0次
名校
解题方法
10 . 为实现碳中和,将 在一定条件下转化为化工原料,其中
在一定条件下转化为化工原料,其中 和
和 可发生如下两个平行反应:
可发生如下两个平行反应:
①

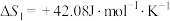
②
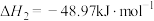
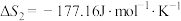
(1)根据所给信息,若要反应②自发进行,需要控制温度范围为___________ ℃(保留一位小数)。
(2)将 和
和 按物质的量之比
按物质的量之比 通入刚性密闭容器中,在催化剂作用下发生反应①和反应②,在相同的时间内
通入刚性密闭容器中,在催化剂作用下发生反应①和反应②,在相同的时间内 的选择性和产率随温度的变化如下表所示。
的选择性和产率随温度的变化如下表所示。
已知:X代表 的选择性=
的选择性=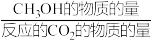 ×100%,Y代表甲醇的产率%
×100%,Y代表甲醇的产率%
①在上述条件下合成甲醇的工业条件是___________ 。
A.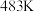 B.
B.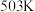
C.催化剂B(CZT) D.催化剂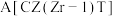
②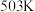 以上,升高温度导致
以上,升高温度导致 的转化率增大,甲醇的产率降低。可能的原因是
的转化率增大,甲醇的产率降低。可能的原因是___________ 。
(3)在容器体积不变的条件下,下列说法中,能判断反应②达到平衡状态的有___________ (填标号)。
A.混合气体总压强不再变化 B.断裂 键的同时断裂
键的同时断裂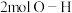 键
键
C. 和
和 的物质的量之比不再变化 D.混合气体的平均相对分子质量不再变化
的物质的量之比不再变化 D.混合气体的平均相对分子质量不再变化
E.混合气体的密度不再变化 F.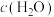 保持不变
保持不变
(4)若体积不变的密闭容器中只发生上述反应①,在进气比 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度
平衡转化率如图所示。则B和D两点的温度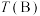
___________ 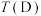 (选填“<”,“>”或“=”)。
(选填“<”,“>”或“=”)。 )、乙(容积为
)、乙(容积为 )两刚性容器中分别充入
)两刚性容器中分别充入 和
和 在适宜的催化剂作用下发生反应②,容器内总压强随时间变化如图所示:
在适宜的催化剂作用下发生反应②,容器内总压强随时间变化如图所示:___________ 容器中压强的变化情况(填“甲”或“乙”);
②利用图中数据计算250℃该反应的分压平衡常数
___________ (结果用分数表示)。
 在一定条件下转化为化工原料,其中
在一定条件下转化为化工原料,其中 和
和 可发生如下两个平行反应:
可发生如下两个平行反应:①


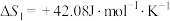
②

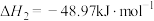
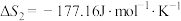
(1)根据所给信息,若要反应②自发进行,需要控制温度范围为
(2)将
 和
和 按物质的量之比
按物质的量之比 通入刚性密闭容器中,在催化剂作用下发生反应①和反应②,在相同的时间内
通入刚性密闭容器中,在催化剂作用下发生反应①和反应②,在相同的时间内 的选择性和产率随温度的变化如下表所示。
的选择性和产率随温度的变化如下表所示。已知:X代表
 的选择性=
的选择性=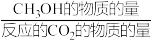 ×100%,Y代表甲醇的产率%
×100%,Y代表甲醇的产率%| 温度/K | 催化剂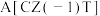 | 催化剂B(CZT) | ||
| X(甲醇选择性) | Y(甲醇产率) | X(甲醇选择性) | Y(甲醇产率) | |
| 483 | 38 | 2 | 19 | 0.9 |
| 503 | 26 | 4.5 | 33 | 2.2 |
| 523 | 23 | 3.9 | 30 | 1.9 |
| 543 | 18 | 3 | 25 | 1.8 |
| 563 | 16 | 3 | 25 | 1.6 |
①在上述条件下合成甲醇的工业条件是
A.
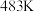 B.
B.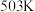
C.催化剂B(CZT) D.催化剂
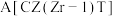
②
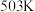 以上,升高温度导致
以上,升高温度导致 的转化率增大,甲醇的产率降低。可能的原因是
的转化率增大,甲醇的产率降低。可能的原因是(3)在容器体积不变的条件下,下列说法中,能判断反应②达到平衡状态的有
A.混合气体总压强不再变化 B.断裂
 键的同时断裂
键的同时断裂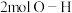 键
键C.
 和
和 的物质的量之比不再变化 D.混合气体的平均相对分子质量不再变化
的物质的量之比不再变化 D.混合气体的平均相对分子质量不再变化E.混合气体的密度不再变化 F.
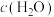 保持不变
保持不变(4)若体积不变的密闭容器中只发生上述反应①,在进气比
 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度
平衡转化率如图所示。则B和D两点的温度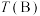
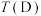 (选填“<”,“>”或“=”)。
(选填“<”,“>”或“=”)。
 )、乙(容积为
)、乙(容积为 )两刚性容器中分别充入
)两刚性容器中分别充入 和
和 在适宜的催化剂作用下发生反应②,容器内总压强随时间变化如图所示:
在适宜的催化剂作用下发生反应②,容器内总压强随时间变化如图所示:
②利用图中数据计算250℃该反应的分压平衡常数

您最近一年使用:0次



