名校
1 . 哈伯法合成氨的反应原理为 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是A.该反应在低温下能自发进行,则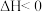 |
B.选用高效催化剂,可降低该反应的 |
C.其它条件不变,增大起始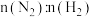 的比值,可提高N2的平衡转化率 的比值,可提高N2的平衡转化率 |
| D.提高体系的压强可增大反应的化学平衡常数 |
您最近一年使用:0次
2024-05-08更新
|
162次组卷
|
2卷引用:江苏省徐州市第一中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
2 . 下列图示与对应的叙述相符的是
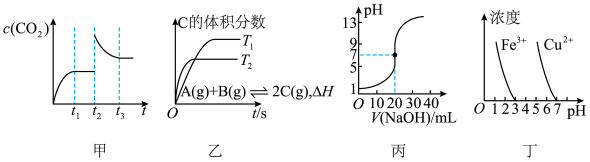
A.图甲表示t2时刻向CaCO3(s) CO2(g)+CaO(s)恒温恒容体系中通入CO2,其浓度的变化 CO2(g)+CaO(s)恒温恒容体系中通入CO2,其浓度的变化 |
| B.图乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH>0 |
| C.图丙表示0.1 000mol·L-1 NaOH溶液滴定20.00 mL 等浓度醋酸溶液的滴定曲线 |
| D.根据图丁,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
您最近一年使用:0次
名校
解题方法
3 . 有效去除大气中的NOx和水体中的氮,并且转化为可利用的资源是重要课题。
(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: (aq)+2O2(g)=
(aq)+2O2(g)= (aq)+2H+(aq)+H2O(l) ΔH=
(aq)+2H+(aq)+H2O(l) ΔH=_______ kJ·mol-1
(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。_______ (请填“C”或“D”)极相连。
②该电解池的阳极反应式为_______ 。
③该电解池(图乙)中离子交换膜为_______ (请填“阴”或“阳”)离子交换膜。
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)_______ mol。
(3)纳米颗粒在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。_______ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_______ (填字母)的活化能。
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮( 和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含
和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含 ),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。_______ 。
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是_______ 。
(1)在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: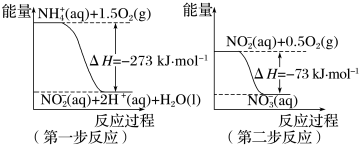
 (aq)+2O2(g)=
(aq)+2O2(g)= (aq)+2H+(aq)+H2O(l) ΔH=
(aq)+2H+(aq)+H2O(l) ΔH=(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。
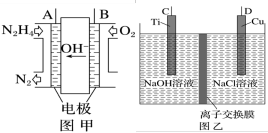
②该电解池的阳极反应式为
③该电解池(图乙)中离子交换膜为
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)
(3)纳米颗粒在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。
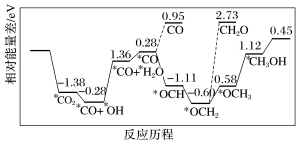
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(
 和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含
和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含 ),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。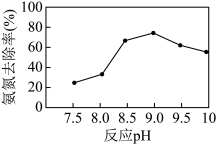
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是
您最近一年使用:0次
名校
4 . 工业废水中常含有一定量的 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:
步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中 转化为
转化为 。
。
步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 mol·L-1 溶液进行滴定,数据记录如下:(
溶液进行滴定,数据记录如下:( )
)
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是_______ 。
(2)滴定达到终点时的实验现象是_______ 。
(3)以下操作会造成废水中 含量测定值偏小的是
含量测定值偏小的是_______ (填字母)。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取 溶液的滴定管用蒸馏水洗后未用标准液润洗
溶液的滴定管用蒸馏水洗后未用标准液润洗
E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
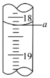
(4)步骤Ⅲ中a的读数如下图所示,则 的含量为
的含量为_______ g·L (写出计算过程)。
(写出计算过程)。
 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中
 转化为
转化为 。
。步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 mol·L-1
 溶液进行滴定,数据记录如下:(
溶液进行滴定,数据记录如下:( )
)| 实验次数 | 第一次(mL) | 第二次(mL) | 第三次(mL) |
 溶液原始读数 溶液原始读数 | 1.02 | 2.00 | 0.20 |
 溶液终点读数 溶液终点读数 | 19.03 | 19.99 | a |
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是
(2)滴定达到终点时的实验现象是
(3)以下操作会造成废水中
 含量测定值偏小的是
含量测定值偏小的是A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取
 溶液的滴定管用蒸馏水洗后未用标准液润洗
溶液的滴定管用蒸馏水洗后未用标准液润洗E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
(4)步骤Ⅲ中a的读数如下图所示,则
 的含量为
的含量为 (写出计算过程)。
(写出计算过程)。
您最近一年使用:0次
5 . 以工业废铜渣(主要含CuO,还含有CuS、Fe2O3等)为原料制备CuCl,并测定其纯度。其制备过程可表示为
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为_______ 。
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是_______ 。
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 mol·L-1,c(Cu2+)=2 mol·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为____ 。已知:Fe3+完全沉淀后其浓度应小于1×10-6 mol·L-1。
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为_______ 。
②相同条件下,CuCl沉淀率随 的变化如下图所示。
的变化如下图所示。 大于2.5,CuCl沉淀率几乎不变的原因
大于2.5,CuCl沉淀率几乎不变的原因_______ 。
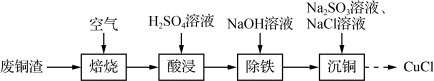
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 mol·L-1,c(Cu2+)=2 mol·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为
②相同条件下,CuCl沉淀率随
 的变化如下图所示。
的变化如下图所示。 大于2.5,CuCl沉淀率几乎不变的原因
大于2.5,CuCl沉淀率几乎不变的原因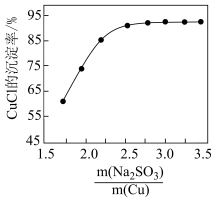
您最近一年使用:0次
名校
6 . 三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。已知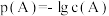 。下列 说法不正确的是
。下列 说法不正确的是

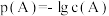 。下列 说法不正确的是
。下列 说法不正确的是 
| A.a点无ZnS沉淀生成 |
| B.可用MnS除去MnCl2溶液中混有的少量ZnCl2 |
C.CuS和MnS共存的悬浊液中, 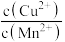 =10-20 =10-20 |
| D.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)减小 |
您最近一年使用:0次
名校
7 . 对下列图示实验的描述正确的是
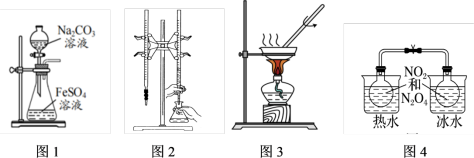
| A.图1所示的实验:制取FeCO3 |
| B.图2所示的实验:用NaOH溶液滴定盐酸 |
| C.图3所示的实验:用装置丁将FeCl3溶液蒸干制得无水FeCl3 |
| D.图4所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断2NO2(g) ⇌N2O4(g)的正反应是吸热反应 |
您最近一年使用:0次
名校
8 . 已知:X(s)+2Y(g)⇌3Z(g),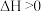 ,下列说法错误的是
,下列说法错误的是
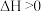 ,下列说法错误的是
,下列说法错误的是| A.增加 X 的用量,对反应速率没有影响 |
| B.升高反应温度,逆反应速率增大,正反应速率减小 |
| C.达到化学平衡状态时,Z 的浓度不再发生变化 |
| D.0.1 mol X 和 0.2 mol Y 充分反应生成 Z 的物质的量一定小于 0.3 mol |
您最近一年使用:0次
名校
9 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离出的c(H+)=1.0×10-13mol/L的溶液中:Na+、 、Cl-、 、Cl-、 |
B.与Al反应放出H2的溶液:Mg2+、Cu2+、 、 、 |
C.加入少量KSCN后变为红色的溶液中:K+、Mg2+、I-、 |
D.无色透明的溶液中:CH3COO-、 、K+、Na+ 、K+、Na+ |
您最近一年使用:0次
名校
10 . 生活与生产都离不开化学。下列说法不正确的是
| A.用碳酸钠溶液可以洗涤油污 |
| B.用氯化铵和氯化锌溶液去除铁器表面的锈迹 |
| C.用明矾可以对自来水杀菌消毒 |
| D.含氟牙膏可以有效防止龋齿 |
您最近一年使用:0次



