名校
解题方法
1 . 分子式为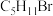 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
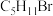 的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)
的烃,分子中含有3个甲基的同分异构体共有(不考虑立体异构)| A.3种 | B.2种 | C.5种 | D.4种 |
您最近一年使用:0次
2024-05-08更新
|
102次组卷
|
8卷引用:江苏无锡市第三高级中学2023-2024学年高二上学期期中考试化学试卷
名校
2 . 中华文化源远流长、博大精深。下列有关诗词中蕴含的化学知识不正确的是
| A.曹植的“磁石引铁,于金不连”——“磁石”能吸引铁,不能吸引金 |
| B.苏轼的“庭下如积水空明,水中藻、荇交横,盖竹柏影也”——句中对月光的描述体现了丁达尔现象 |
| C.杨万里的“庐山山南刷铜绿”——铜锈俗称“铜绿”,其主要成分为铜的氧化物 |
| D.杜牧的“折戟沉沙铁未销”——铁生锈的条件是与水和氧气同时接触 |
您最近一年使用:0次
2024-05-05更新
|
39次组卷
|
2卷引用:江苏省无锡市锡东高级中学2023-2024学年高二下学期5月月考化学试题
3 . 脑白金实为褪黑素,据报道它具有提高免疫力、促进睡眠等功效,其结构简式如下图。下列关于脑白金说法正确的是

| A.分子式为C13H17N2O2 | B.属于芳香族化合物 |
| C.能发生加成反应 | D.不能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
4 . 乙酰苯胺(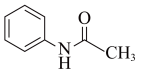 )作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺(
)作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺(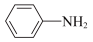 )和冰醋酸反应制得,该反应是放热的可逆反应。
)和冰醋酸反应制得,该反应是放热的可逆反应。
II.可能用到的有关性质如下:
| 名称 | 熔点/℃ | 沸点/℃ | 溶解度/g(20℃) | |
| 水 | 乙醇 | |||
| 苯胺 | -6.3 | 184 | 3.4 | 任意比混合 |
| 冰醋酸 | 16.6 | 118 | 任意比混合 | 任意比混合 |
| 乙酰苯胺 | 114.3 | 304 | 0.46 | 36.9 |
| (温度高溶解度大) | ||||
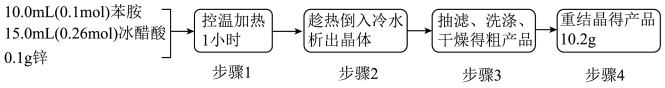
(1)写出制备乙酰苯胺的化学方程式
(2)①加入的锌粒的作用是
②加入的冰醋酸要过量的目的
(3)步骤1所用装置如图所示。


②反应体系的温度控制在100℃~105℃,目的是
③判断反应基本完全的现象是
(4)步骤3中洗涤乙酰苯胺粗产品最合适的试剂是___________(填标号)。
| A.冰水 | B.热水 | C.15%的乙醇溶液 | D.NaOH溶液 |
(5)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→
您最近一年使用:0次
5 . 1 mol有机物A(分子式为C6H10O4)经水解后得到1 mol有机物B和2 mol有机物C,C经分子内脱水得D,D可以发生加聚反应生成高聚物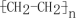 。由此可推知A的结构简式为
。由此可推知A的结构简式为
| A.HOOCCH2CH2COOCH2CH3 | B.HOOC(CH2)3COOCH3 |
| C.CH3OOC(CH2)2COOCH3 | D.CH3CH2OOCCOOCH2CH3 |
您最近一年使用:0次
6 . 现有三种元素的基态原子的电子排布式如下:
①1s22s22p3 ②1s22s22p4 ③1s22s22p63s23p4
下列有关比较中正确的是
①1s22s22p3 ②1s22s22p4 ③1s22s22p63s23p4
下列有关比较中正确的是
| A.原子半径:③>②>① | B.非金属性:③>②>① |
| C.气态氢化物的稳定性:①>②>③ | D.第一电离能:①>②>③ |
您最近一年使用:0次
解题方法
7 . 下列关于反应热和焓变的说法正确的是
| A.放热反应的ΔH<0,吸热反应的ΔH>0 |
| B.任何条件下,焓变完全等于反应热 |
| C.所有化学反应的反应热都可以通过实验直接测得 |
| D.生成物的总焓大于反应物的总焓时,ΔH<0 |
您最近一年使用:0次
8 . 在一定容积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________ 。
(2)该反应为________ (填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。该温度下加入1 mol CO2(g)和1 mol H2(g),充分反应,达到平衡时,CO2的转化率为________ 。
 ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
解题方法
9 . 固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。某科学实验小组将6 mol CO2和8 mol H2充入2 L的恒温密闭容器中,测得H2的物质的量随时间变化如图曲线所示。a、b、c、d、e括号内数据表示坐标。________ ,该时间段内H2的平均反应速率是_______________ 。
(2)8 min时,CO2的转化率是________ ,反应前后容器内的压强比是________ 。
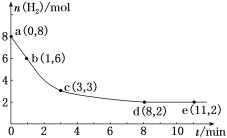
(2)8 min时,CO2的转化率是
您最近一年使用:0次
解题方法
10 . 回答下列问题:
(1)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。________ (填“左”或“右”)移动。
②a电极为电解池的________ (填“阴”或“阳”)极,写出该电极的电极反应式:__________ 。
(2)产生1molH2,电路中通过的电子数目为___________ 。
(1)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。
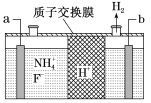
②a电极为电解池的
(2)产生1molH2,电路中通过的电子数目为
您最近一年使用:0次



