硫、硒、碲的化合物在农药、石油工业、矿物开采、萃取及有机合成等领域的应用广泛。回答下列问题:
(1)基态Se原子的价层电子排布式为___________ 。
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
(3)类卤素 分子结构式为
分子结构式为___________ ,1mol 中含有π键的数目为
中含有π键的数目为___________ ,HSCN结构有两种,已知硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是___________ 。
(4)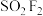 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
___________  (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是___________ 。
(1)基态Se原子的价层电子排布式为
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
A.氧族元素气态氢化物的稳定性按 、 、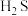 、 、 、 、 的顺序依次减弱 的顺序依次减弱 |
| B.其氢化物中的键长按O―H、S―H、Se―H、Te―H的顺序依次减小 |
C.其阴离子的还原性按 、 、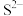 、 、 、 、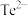 的顺序依次增强 的顺序依次增强 |
D.其最高价氧化物的水化物酸性按 、 、 、 、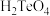 顺序依次增强 顺序依次增强 |
(3)类卤素
 分子结构式为
分子结构式为 中含有π键的数目为
中含有π键的数目为 )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是(4)
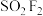 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是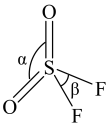

 (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是
更新时间:2024-05-28 13:45:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】硫和硒(34Se)在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
(1)含+4价硫元素的化合物有SO2、H2SO3和X等。
①SO2使品红溶液褪色,说明SO2具有的化学性质是___________ 。
②已知X属于钠盐。写出X转化为SO2的化学方程式:___________ 。
③从下列试剂中任选一种试剂:浓硫酸、酸性高锰酸钾溶液、氯水、硫化钠溶液,设计实验证明SO2中硫元素的化合价在化学反应中可以发生变化(写出一种方案即可),填写下表。
(2)以工业硒为原料制备高纯硒时的主要物质转化如下图。___________ (填字母序号)。
a.硒原子的最外层有6个电子 b.硒元素的非金属性强于硫元素的非金属性
c.SeO2属于酸性氧化物 d.过程i中硒被氧化
②过程iii中使用的还原剂为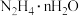 ,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的
,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的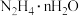 的物质的量之比为
的物质的量之比为___________ (工业硒中杂质与O2的反应可忽略)。
(1)含+4价硫元素的化合物有SO2、H2SO3和X等。
①SO2使品红溶液褪色,说明SO2具有的化学性质是
②已知X属于钠盐。写出X转化为SO2的化学方程式:
③从下列试剂中任选一种试剂:浓硫酸、酸性高锰酸钾溶液、氯水、硫化钠溶液,设计实验证明SO2中硫元素的化合价在化学反应中可以发生变化(写出一种方案即可),填写下表。
| 选择的试剂 | 转化后的含硫物质 | 预期现象 |
(2)以工业硒为原料制备高纯硒时的主要物质转化如下图。
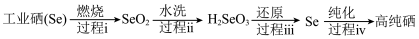
a.硒原子的最外层有6个电子 b.硒元素的非金属性强于硫元素的非金属性
c.SeO2属于酸性氧化物 d.过程i中硒被氧化
②过程iii中使用的还原剂为
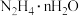 ,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的
,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的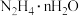 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表中的一部分。
根据A—J在周期表中的位置,用元素符号、化学式或反应式 回答下列问题:
(1)氧化性最强的单质是___ ,用一个化学反应证明H单质的氧化性强于G单质__________ 。
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为_________ 。
(3)B、C、G、H离子半径由大到小的顺序是_________ 。
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为______ 。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | A | |||||||
| 2 | E | F | G | H | J | |||
| 3 | B | C | D | I |
(1)氧化性最强的单质是
(2)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为
(3)B、C、G、H离子半径由大到小的顺序是
(4)D单质可用来制造D—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】黑火药是我国古代的四大发明之一,距今已有1000多年的历史,其成分是木炭(C)、硫粉(S)和硝酸钾(KNO3)。回答下列有关问题:
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为________________ 。
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕________ ,有____ 对成对电子。
(3)C、N、O、K的电负性由大到小的顺序是_________________ 。
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为_______________ 。
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是_________ ;KNO3可电离出NO3-,NO3-的空间构型是______________ 。
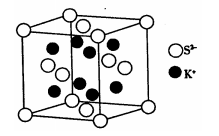
(6)K2S的晶胞结构如图所示。其中K+的配位数为_______ ,若K2S晶体的密度为ρg·cm-3,则晶胞中距离最近的两个S2-核间距为_________ cm(用NA表示阿伏伽德罗常数的值)
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕
(3)C、N、O、K的电负性由大到小的顺序是
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是
(6)K2S的晶胞结构如图所示。其中K+的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素A—D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题:
(1)B元素原子的最外层轨道表示式是_____ ,D离子的核外电子排布____________ 式是______________ 。C和D形成的化合物的电子式为_____________ 。
(2)A、B、C、D的原子半径大小为:______ >______ >________ >(用元素符号表示)
(3)D单质在B单质中燃烧的化学方程式为_______________________
(4)A和D两元素金属性较强的是(用元素符号表示)____ 。写出能证明该结论的一个实验事实________ 。
| A | 单质是热和电的良导体,熔点97.81℃,沸点882.9°C,在氧气中燃烧得到淡黄色固体。 |
| B | 原子核外有7种运动状态不同的电子 |
| C | 单质常温、常压下是气体,原子的L层有一个未成对的p电子。 |
| D | +2价阳离子的核外电子排布与氖原子相同。 |
(1)B元素原子的最外层轨道表示式是
(2)A、B、C、D的原子半径大小为:
(3)D单质在B单质中燃烧的化学方程式为
(4)A和D两元素金属性较强的是(用元素符号表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁镁合金是一种性能优异的储氢材料。关于铁镁两种元素,请回答下列问题:
(1)同周期元素中,第一电离能小于镁的元素有___________ 种。
(2)基态Fe原子的简化电子排布式为___________ ,其中电子的空间运动状态有___________ 种,Fe位于元周期表的___________ 区。
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有___________ 种,下列状态的铁中,电离最外层一个电子所需能量最大的是___________ (填标号)。 易被氧化为
易被氧化为
___________ 。
(1)同周期元素中,第一电离能小于镁的元素有
(2)基态Fe原子的简化电子排布式为
(3)与Fe元素同周期,基态原子有2个未成对电子的金属元素有
a.[Ar] 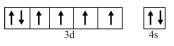 b.[Ar]
b.[Ar]
c.[Ar] d.[Ar]
d.[Ar]
 易被氧化为
易被氧化为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】依据物质结构知识回答下列问题。
Ⅰ.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为_______ 。
(2)根据价层电子对互斥理论,可以推知 的空间构型为
的空间构型为___________ ,其中Se原子采用的轨道杂化方式为___________ 。
(3)已知 与
与 结构相似,①
结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③
、③ 分子内的键角
分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为___________ (填序号)。
Ⅱ. 碳是一种重要元素,可形成多种单质及化合物。
(4) 分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个
分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个 分子中
分子中 键的数目为
键的数目为___________ 。
(5)已知 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为___________ 。氨基氰( )为原料可制得类石墨相氮化碳(
)为原料可制得类石墨相氮化碳( ),氨基氰(
),氨基氰( )分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为
)分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为___________ 。
(6)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
Ⅰ.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为
(2)根据价层电子对互斥理论,可以推知
 的空间构型为
的空间构型为(3)已知
 与
与 结构相似,①
结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③
、③ 分子内的键角
分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为Ⅱ. 碳是一种重要元素,可形成多种单质及化合物。
(4)
 分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个
分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个 分子中
分子中 键的数目为
键的数目为(5)已知
 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为 )为原料可制得类石墨相氮化碳(
)为原料可制得类石墨相氮化碳( ),氨基氰(
),氨基氰( )分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为
)分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为(6)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
A. | B. |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知键能、键长部分数据如下表:
(1)下列推断正确的是___________(填字母,下同)。
(2)下列有关推断正确的是___________。
(3)在表中所给 键中,键长最短的是
键中,键长最短的是___________ ,最长的是___________ ; 键的键长
键的键长___________ (填“大于”“小于”或“等于”) 键的键长。
键的键长。
| 共价键 | 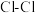 | 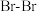 |  | 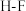 |  | 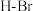 |  |  |
键能 | 242.7 | 193.7 | 152.7 | 567 | 431.8 | 366 | 298.7 | 462.8 |
键长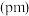 | 19 | 228 | 266 | |||||
| 共价键 |  | 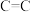 |  |  |  | 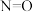 |  |  |
键能 | 347.7 | 615 | 812 | 413.4 | 390.8 | 607 | 142 | 497.3 |
键长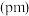 | 154 | 133 | 120 | 109 | 101 |
A.稳定性: | B.氧化性: |
C.沸点: | D.还原性: |
| A.同种元素形成的共价键,稳定性:三键>双键>单键 |
| B.同种元素形成的双键键能一定小于单键的2倍 |
| C.键长越短,键能一定越大 |
| D.氢化物的键能越大,其稳定性一定越强 |
 键中,键长最短的是
键中,键长最短的是 键的键长
键的键长 键的键长。
键的键长。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高纯硅具有良好的硬度和耐磨性以及良好的光、电性能,广泛用于芯片、集成电路、光伏电池板等领域。工业上制备高纯硅反应的化学方程式: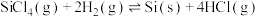
(1)此反应方程式中,呈正四面体型分子的电子式是___________ 。
(2)HCl的稳定性___________ (填“大于”“小于”)HF,说明理由___________ 。
(3)根据下表判断,此反应的 为___________
为___________
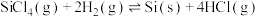
(1)此反应方程式中,呈正四面体型分子的电子式是
(2)HCl的稳定性
(3)根据下表判断,此反应的
 为___________
为___________| 化学键 |  |  |  |  |  |  |
| 键能(kJ/mol) | 460 | 360 | 436 | 431 | 176 | 347 |
| A.+412 kJ/mol | B.+236 kJ/mol | C.-116 kJ/mol | D.-236 kJ/mol |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)Cu的价电子排布图______ ,钾的最高能层符号______ 。
(2)NH3在水中的溶解度大于H2S在水中的溶解度其原因是______ 。
(3)用“>、<、=”来比较下列晶体的熔沸点。
CaO______ MgO HF______ HCl Si______ SiC K______ Ti
(4)某金属晶体堆积方式为面心立方堆积,其配位数为______ ;一个该金属晶胞中含有______ 个该金属原子。
(5)NH3与NH4+的键角大小,NH3______ NH4+(用“>、<、=”比较),原因是______ 。
(2)NH3在水中的溶解度大于H2S在水中的溶解度其原因是
(3)用“>、<、=”来比较下列晶体的熔沸点。
CaO
(4)某金属晶体堆积方式为面心立方堆积,其配位数为
(5)NH3与NH4+的键角大小,NH3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
I.
(1)下列状态的铝中,电离最外层一个电子所需能量最大的是___________。
(2)Mo的价层电子排布式为4d55s1,Mo在周期表中的位置为________ ,Mo3+价层电子排布图为________ 。
(3)写出CNO-的一个等电子体分子___________ 。
II.一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图。

(4)甘氨酸(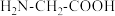 )中N的杂化轨道类型为
)中N的杂化轨道类型为___________ ;甘氨酸易溶于水,请解释理由___________ 。
(5)一水合甘氨酸锌中 的配位数为
的配位数为___________ 。
I.
(1)下列状态的铝中,电离最外层一个电子所需能量最大的是___________。
A.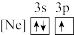 | B. | C. | D. |
(3)写出CNO-的一个等电子体分子
II.一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图。

(4)甘氨酸(
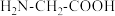 )中N的杂化轨道类型为
)中N的杂化轨道类型为(5)一水合甘氨酸锌中
 的配位数为
的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】我国科学家屠呦呦因成功从黄花蒿中提取青蒿素而获得2015年诺贝尔奖。
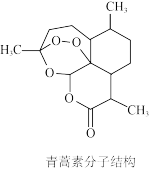
(1)青蒿素是治疗疟疾的有效药物,属于酯类化合物,其分子结构如图所示,请用笔在图中将酯基圈出来。____ 。
(2)从黄花蒿中提取青蒿素的流程如图:
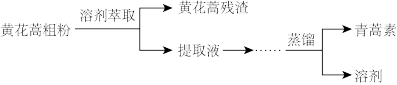
研究团队经历了使用不同溶剂和不同温度的探究过程,实验结果如表:
①用水作溶剂,提取无效的原因是____ 。
②研究发现,青蒿素分子中的某个基团对热不稳定,据此分析用乙醚作溶剂,提取效率高于乙醇的原因是____ 。
(3)研究还发现,将青蒿素通过下面反应转化为水溶性增强的双氢青蒿素,治疗疟疾的效果更好。
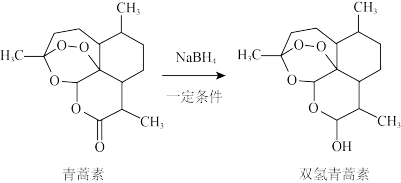
从分子结构与性质的关系角度推测双氢青蒿素疗效更好的原因____ 。
(4)提取并转化青蒿素治疗疟疾的过程中,应考虑物质的____ 、____ 等性质。
(1)青蒿素是治疗疟疾的有效药物,属于酯类化合物,其分子结构如图所示,请用笔在图中将酯基圈出来。

(2)从黄花蒿中提取青蒿素的流程如图:
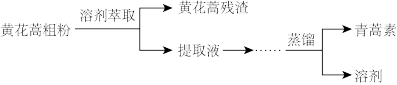
研究团队经历了使用不同溶剂和不同温度的探究过程,实验结果如表:
| 溶剂 | 水 | 乙醇 | 乙醚 |
| 沸点/℃ | 100 | 78 | 35 |
| 提取效率 | 几乎为0 | 35% | 95% |
②研究发现,青蒿素分子中的某个基团对热不稳定,据此分析用乙醚作溶剂,提取效率高于乙醇的原因是
(3)研究还发现,将青蒿素通过下面反应转化为水溶性增强的双氢青蒿素,治疗疟疾的效果更好。

从分子结构与性质的关系角度推测双氢青蒿素疗效更好的原因
(4)提取并转化青蒿素治疗疟疾的过程中,应考虑物质的
您最近一年使用:0次



