已知键能、键长部分数据如下表:
(1)下列推断正确的是___________(填字母,下同)。
(2)下列有关推断正确的是___________。
(3)在表中所给 键中,键长最短的是
键中,键长最短的是___________ ,最长的是___________ ; 键的键长
键的键长___________ (填“大于”“小于”或“等于”) 键的键长。
键的键长。
| 共价键 | 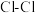 | 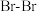 |  | 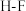 |  | 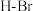 |  |  |
键能 | 242.7 | 193.7 | 152.7 | 567 | 431.8 | 366 | 298.7 | 462.8 |
键长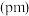 | 19 | 228 | 266 | |||||
| 共价键 |  | 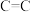 |  |  |  | 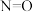 |  |  |
键能 | 347.7 | 615 | 812 | 413.4 | 390.8 | 607 | 142 | 497.3 |
键长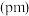 | 154 | 133 | 120 | 109 | 101 |
A.稳定性: | B.氧化性: |
C.沸点: | D.还原性: |
| A.同种元素形成的共价键,稳定性:三键>双键>单键 |
| B.同种元素形成的双键键能一定小于单键的2倍 |
| C.键长越短,键能一定越大 |
| D.氢化物的键能越大,其稳定性一定越强 |
 键中,键长最短的是
键中,键长最短的是 键的键长
键的键长 键的键长。
键的键长。
21-22高二·全国·课后作业 查看更多[3]
(已下线)2.1.2 键参数——键能、键长与键角(提高)贵州省贵阳清镇北大培文学校2022-2023学年高二下学期3月月考化学试题专题3 微粒间作用力与物质性质 第三单元 共价键共价晶体 第2课时 共价键的键能与化学反应的反应热 共价晶体
更新时间:2022-08-22 16:42:28
|
【知识点】 键能、键长、键角及应用解读
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题。
(1)气态氢化物热稳定性HF大于HCl的主要原因是____________________ 。
(2)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是___________ 。
(1)气态氢化物热稳定性HF大于HCl的主要原因是
(2)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知氢分子的形成过程示意图如图所示,请据图回答问题。

(1)H—H键的键长为___________ ,①~⑤中,体系能量由高到低的顺序是___________ 。
(2)下列说法中正确的是___________ (填字母)。
A.氢分子中含有一个π键
B.由①到④,电子在核间出现的概率增大
C.由④到⑤,必须消耗外界的能量
D.氢分子中含有一个极性共价键
Ⅱ.几种常见化学键的键能如下表所示。
请回答下列问题:
(1)试比较Si—C键与Si—Si键的键能大小:X_______ (填“>”“<”或“=”)226kJ·mol-1。
(2)H2被认为是21世纪人类最理想的燃料,而又有科学家提出硅是“21世纪的能源”“未来的石油”等观点。结合Ⅰ中图象,试计算每千克H2燃烧(生成水蒸气)放出的热量约为___________ ;每摩尔硅完全燃烧放出的热量约为________ (已知1molSi中含有2molSi—Si键,1molSiO2中含有4molSi—O键)。

(1)H—H键的键长为
(2)下列说法中正确的是
A.氢分子中含有一个π键
B.由①到④,电子在核间出现的概率增大
C.由④到⑤,必须消耗外界的能量
D.氢分子中含有一个极性共价键
Ⅱ.几种常见化学键的键能如下表所示。
| 化学键 | Si—O | H—O | O==O | Si—Si | Si—C |
| 键能/kJ·mol-1 | 452 | 462.8 | 497.3 | 226 | X |
请回答下列问题:
(1)试比较Si—C键与Si—Si键的键能大小:X
(2)H2被认为是21世纪人类最理想的燃料,而又有科学家提出硅是“21世纪的能源”“未来的石油”等观点。结合Ⅰ中图象,试计算每千克H2燃烧(生成水蒸气)放出的热量约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】光伏材料是指能将太阳能直接转换成电能的材料,光伏材料又称太阳能材料,只有半导体材料具有这种功能。硅(Si)、镓(Ga)、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:___________ 。硅烷很难像烷烃一样形成长链,这是因为硅的原子半径___________ (填“大于”“小于”或“等于”)碳的原子半径,因此键长___________ (填“长”或“短”),键能小。丁硅烯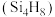 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是___________ 。
(3)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是___________ 。
(4)硅和锗都能与氯元素形成四氯化物 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:___________ 。
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
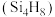 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近一年使用:0次



