光伏材料是指能将太阳能直接转换成电能的材料,光伏材料又称太阳能材料,只有半导体材料具有这种功能。硅(Si)、镓(Ga)、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:___________ 。硅烷很难像烷烃一样形成长链,这是因为硅的原子半径___________ (填“大于”“小于”或“等于”)碳的原子半径,因此键长___________ (填“长”或“短”),键能小。丁硅烯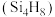 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是___________ 。
(3)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是___________ 。
(4)硅和锗都能与氯元素形成四氯化物 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:___________ 。
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
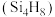 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
更新时间:2024-03-24 12:46:58
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】CO2、CO作为碳源,可以制备多种有机化合物,在能源结构方面具有重要意义。回答下列问题:
(1)CO2的电子式为_________ 。
(2)一定条件下,CO与H2可化合生成甲醇(CH3OH),该反应的化学方程式为_____ 。
(3)利用CO2可合成聚碳酸酯(易降解),反应原理如下:

从环境角度来看,用聚碳酸酯塑料代替聚乙烯和聚苯乙烯传统塑料的最大优点是______ 。
(4)研究表明,相对原子质最小的金属氧化时,都可以获得高的燃烧热,从而可解决二氧化碳的排放问题。其中镁粉作燃料时还可消除过量的二氧化碳,其原因是_____ (用化学方程式解释)。
(5)最近我国科学家采用In2O3/分子筛催化剂,实现了CO2加氢一步转化有机物X,化学式为C6H14,该物质一氯代物有2种,X的结构简式为______ 。
(1)CO2的电子式为
(2)一定条件下,CO与H2可化合生成甲醇(CH3OH),该反应的化学方程式为
(3)利用CO2可合成聚碳酸酯(易降解),反应原理如下:

从环境角度来看,用聚碳酸酯塑料代替聚乙烯和聚苯乙烯传统塑料的最大优点是
(4)研究表明,相对原子质最小的金属氧化时,都可以获得高的燃烧热,从而可解决二氧化碳的排放问题。其中镁粉作燃料时还可消除过量的二氧化碳,其原因是
(5)最近我国科学家采用In2O3/分子筛催化剂,实现了CO2加氢一步转化有机物X,化学式为C6H14,该物质一氯代物有2种,X的结构简式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)比较酸性的相对强弱: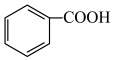
________ 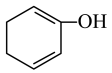 (填“>”、“<”或“=”);用一个化学方程式说明
(填“>”、“<”或“=”);用一个化学方程式说明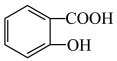 两个官能团酸性的相对强弱
两个官能团酸性的相对强弱___________ 。
(2) 是离子化合物,各原子均满足
是离子化合物,各原子均满足 稳定结构,且两个氮原子环境完全相同。写出
稳定结构,且两个氮原子环境完全相同。写出 的电子式
的电子式__________ 。
(3)一定条件下,测定 的相对分子质量时,实验数据明显大于理论值,原因是
的相对分子质量时,实验数据明显大于理论值,原因是__________ 。

 (填“>”、“<”或“=”);用一个化学方程式说明
(填“>”、“<”或“=”);用一个化学方程式说明 两个官能团酸性的相对强弱
两个官能团酸性的相对强弱(2)
 是离子化合物,各原子均满足
是离子化合物,各原子均满足 稳定结构,且两个氮原子环境完全相同。写出
稳定结构,且两个氮原子环境完全相同。写出 的电子式
的电子式(3)一定条件下,测定
 的相对分子质量时,实验数据明显大于理论值,原因是
的相对分子质量时,实验数据明显大于理论值,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_____ 。
(2)基态Ti原子的核外电子排布式为_____ 。
(3)Fe基态核外电子排布式为_____ 。
(4)氮原子价层电子的轨道表达式(电子排布图)为_____ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)基态Ti原子的核外电子排布式为
(3)Fe基态核外电子排布式为
(4)氮原子价层电子的轨道表达式(电子排布图)为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】第四周期是周期表中的第一个长周期,元素种类丰富,其中有一种未成对电子数最多的元素,完成以下填空:
(1)该元素是_______ (填名称),它位于第_______ 族。
(2)核外电子排布式是_______ ,最高能层符号为_______ 。
(3)它有_______ 个能层,_______ 个能级,_______ 种运动状态不同的电子。
(4)价电子排布式:_______ ,价电子排布图:_______ 。
(5)属于_______ 区。
(1)该元素是
(2)核外电子排布式是
(3)它有
(4)价电子排布式:
(5)属于
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
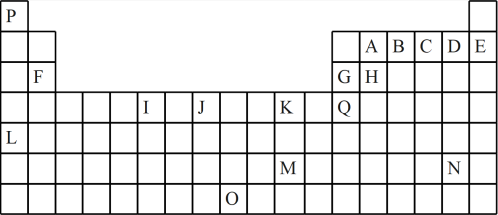
(1)I的最高化合价为____ ;K的元素名称为____ 。
(2)基态时G元素原子的电子排布式___ ,J元素原子的外围电子排布式___ 。
(3)下列对比正确的是___ 。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是____ 。
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)元素B和C的气态氢化物热稳定性较强的是____ (填化学式)。

(1)I的最高化合价为
(2)基态时G元素原子的电子排布式
(3)下列对比正确的是
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)元素B和C的气态氢化物热稳定性较强的是
您最近半年使用:0次
【推荐2】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是___________ ,占据该能层电子的电子云轮廓图形状为___________ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:___________ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是___________ 。
(4)已知铁是26号元素,写出Fe的价层电子排布式___________ ;在元素周期表中,该元素在_____________ 填“s”“p”“d”“f”或“ds”)区。
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为___________ 。电负性的顺序是___________ 。
(6)写出C的核外电子排布图为:___________ 。
(7)Zn2+的核外电子排布式为___________ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(6)写出C的核外电子排布图为:
(7)Zn2+的核外电子排布式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)基态N原子的价电子轨道表示式为_______ ,基态N原子中电子占据最高能级的电子云轮廓图为_______ 形; 分子中存在配位键,提供空轨道的原子是
分子中存在配位键,提供空轨道的原子是_______ ,分子中的N原子杂化方式为_______ 。
(2)B元素在周期表中的位置_______ ,B的第一电离能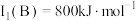 ,判断
,判断
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:电负性由大到小的顺序是
。在H、B、N三种元素中:电负性由大到小的顺序是_______ 。
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:(1)基态N原子的价电子轨道表示式为
 分子中存在配位键,提供空轨道的原子是
分子中存在配位键,提供空轨道的原子是(2)B元素在周期表中的位置
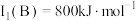 ,判断
,判断
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:电负性由大到小的顺序是
。在H、B、N三种元素中:电负性由大到小的顺序是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为_______ ;反应③中被破坏的化学键属于_______ 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是_______ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第_______ 周期_______ 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是_______
a卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:
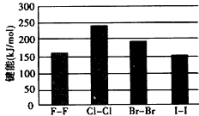
①非金属性强的卤素,其单质分子的化学键_______ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:_______
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键
②卤素单质键能大小与键长的关系为:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Si(NH2)4分子的空间结构(以Si为中心)名称为________ ,分子中氮原子的杂化轨道类型是_______ 。Si(NH2)4受热分解生成Si3N4和NH3,其受热不稳定的原因是________ 。
您最近半年使用:0次




