第四周期是周期表中的第一个长周期,元素种类丰富,其中有一种未成对电子数最多的元素,完成以下填空:
(1)该元素是_______ (填名称),它位于第_______ 族。
(2)核外电子排布式是_______ ,最高能层符号为_______ 。
(3)它有_______ 个能层,_______ 个能级,_______ 种运动状态不同的电子。
(4)价电子排布式:_______ ,价电子排布图:_______ 。
(5)属于_______ 区。
(1)该元素是
(2)核外电子排布式是
(3)它有
(4)价电子排布式:
(5)属于
更新时间:2022-10-05 18:10:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】推导下列元素,回答有关问题:
(1)具有1个4p电子的元素为________ (写元素名称)。基态Fe原子有____ 个未成对电子。Fe3+的电子排布式为_____________ 。
(2)3d能级全充满,4s能级只有1个电子的元素为_______ ,原子序数为________ 。在基态14C原子中,核外存在____ 对自旋相反的电子。基态Si原子中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为____ 、电子数为____ 。
(3)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是________ ,M能层有______ 个电子
(1)具有1个4p电子的元素为
(2)3d能级全充满,4s能级只有1个电子的元素为
(3)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分。
回答下列问题
(1)表中元素原子半径最大的是(写元素符号)__________ ,Z原子核外电子能量最高的电子亚层是__________ 。
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:_________________ ;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因______________________________________________________ 。
(4)硫酸工业生产中接触室内发生的反应方程式为______________________________________ ;
在实际生产中,操作温度选定400—500℃、压强通常采用常压的原因分别是__________________________________________________________________________________________________ 。
碳 | 氮 | Y | |
X | 硫 | Z |
(1)表中元素原子半径最大的是(写元素符号)
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:
(4)硫酸工业生产中接触室内发生的反应方程式为
在实际生产中,操作温度选定400—500℃、压强通常采用常压的原因分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子中,电子填充的能量最高的能级符号为_______ 。
(2)在空气中FeO稳定性小于 ,从电子排布的角度分析,其主要原因是:
,从电子排布的角度分析,其主要原因是:_______ 。
(3)铁氰化钾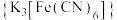 溶液是检验
溶液是检验 常用的试剂。lmol
常用的试剂。lmol 含σ键的数目为
含σ键的数目为_______ 。
(4) 的一种配离子
的一种配离子 中,
中, 的配位数是
的配位数是_______ 。配体 中心原子的杂化类型为
中心原子的杂化类型为_______ 。CoO的熔点是1935℃,CoS的熔点是1135℃,试分析CoO的熔点较高的原因_______ 。
(1)基态Fe原子中,电子填充的能量最高的能级符号为
(2)在空气中FeO稳定性小于
 ,从电子排布的角度分析,其主要原因是:
,从电子排布的角度分析,其主要原因是:(3)铁氰化钾
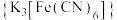 溶液是检验
溶液是检验 常用的试剂。lmol
常用的试剂。lmol 含σ键的数目为
含σ键的数目为(4)
 的一种配离子
的一种配离子 中,
中, 的配位数是
的配位数是 中心原子的杂化类型为
中心原子的杂化类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求填空:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_____ 。
(2)基态Ti原子的核外电子排布式为_____ 。
(3)Fe基态核外电子排布式为_____ 。
(4)氮原子价层电子的轨道表达式(电子排布图)为_____ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)基态Ti原子的核外电子排布式为
(3)Fe基态核外电子排布式为
(4)氮原子价层电子的轨道表达式(电子排布图)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】第四周期中的18 种元素具有重要的用途,在现代工业中备受青睐。
(1)其中,未成对电子数最多的元素名称为_______ ,该元素的基态原子中,电子占据的最高能层具有的原子轨道数为_______ 。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是_______ 。
(3)AsH3 中心原子杂化的类型为_______ ,分子构型为_______
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为_______ 。
(5)与CN-互为等电子体的一种分子为_______ (填化学式);1.5mol [Fe(CN)6]3-中含有键的数目为_______
(1)其中,未成对电子数最多的元素名称为
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是
(3)AsH3 中心原子杂化的类型为
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为
(5)与CN-互为等电子体的一种分子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题。
(1)Cu+基态核外电子排布式为___________ 。
(2)基态Fe原子有___________ 个未成对电子,Fe+的电子排布式为___________ 。
(3)S的基态原子核外有___________ 个未成对电子;Si的基态原子核外电子排布式为___________ 。
(4)Cu的价层电子轨道示意图为___________ 。
(5)基态Si原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ 。
(1)Cu+基态核外电子排布式为
(2)基态Fe原子有
(3)S的基态原子核外有
(4)Cu的价层电子轨道示意图为
(5)基态Si原子中,电子占据的最高能层符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氰酸(化学式:HOCN)是一种有挥发性和腐蚀性的液体,在水中立刻发生如下反应形成盐X(俗名碳铵):HOCN + 2H2O → X。
(1)在上述反应所涉及的各元素中,半径最大的元素原子在周期表中的位置是___________ ,该原子核外电子共占据_______ 个轨道。
(2)X所含阳离子的电子式是________ ;已知25℃时0.1mol/L X溶液pH=7.8,用离子方程式表示原因:______________________ 。
(3)能说明氮元素的非金属性比碳元素强的事实是_________ (选填编号)。
a. 共用电子对偏向:H-N>H-C
b. 氧化性:NO2>CO2
c. 酸性:HNO3>H2CO3
d. 沸点:NH3>CH4
(4)据测定,氰酸有两种结构,一种分子内含有叁键,称为正氰酸,另一种分子内不含叁键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写出正氰酸和异氰酸的结构式:_______________ 、______________ 。
(1)在上述反应所涉及的各元素中,半径最大的元素原子在周期表中的位置是
(2)X所含阳离子的电子式是
(3)能说明氮元素的非金属性比碳元素强的事实是
a. 共用电子对偏向:H-N>H-C
b. 氧化性:NO2>CO2
c. 酸性:HNO3>H2CO3
d. 沸点:NH3>CH4
(4)据测定,氰酸有两种结构,一种分子内含有叁键,称为正氰酸,另一种分子内不含叁键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写出正氰酸和异氰酸的结构式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表中第四周期的某些过渡元素(如Ti、Co等)在生产、生活中有着广泛的应用。Co2+能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
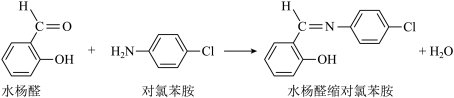
(1)基态Co2+核外电子排布式_______ ;C原子的轨道表示式为_______ ;C、N、O元素的电负性由大到小的顺序为_______ 。
(2)水杨醛所含的官能团为_______ 。
(3)1mol水杨醛最多与_______ H2发生加成反应。
(4)一定条件下,水杨醛缩对氯苯胺与足量NaOH溶液反应的化学方程式_______ 。

(1)基态Co2+核外电子排布式
(2)水杨醛所含的官能团为
(3)1mol水杨醛最多与
(4)一定条件下,水杨醛缩对氯苯胺与足量NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)①基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是__________ (填元素符号,下同),其价层电子排布式为__________ 。
②最外层电子数是次外层电子数3倍的元素是__________ ,其轨道表示式为__________ 。
③ 原子的结构示意图为
原子的结构示意图为__________ 。
(2)H、C、N、O、 的原子半径从小到大的顺序为
的原子半径从小到大的顺序为__________ 。
(3) 是直线形分子,
是直线形分子, 是
是__________ 分子(填“极性”“非极性”)。
(1)①基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是
②最外层电子数是次外层电子数3倍的元素是
③
 原子的结构示意图为
原子的结构示意图为(2)H、C、N、O、
 的原子半径从小到大的顺序为
的原子半径从小到大的顺序为(3)
 是直线形分子,
是直线形分子, 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氟乙(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_________ 。
(2)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填标号);第三电离能的变化图是________ (填标号)。

(3)固态氟化氢中存在(HF)n形式,每个HF以氢键相连。画出(HF)3的链状结构_________ 。
(4)N2F2(二氟氮烯)分子中,氮原子的杂化类型为sp2,则N2F2的结构式为_________ 。
(5)NaHF2熔点为160℃(分解生成HF),电解可制得氟气,推测NaHF2中所含作用力的类型有________ 。
(6)BiOC1是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚(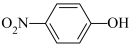 )等。对硝基苯酚的熔点高于邻硝基苯酚(
)等。对硝基苯酚的熔点高于邻硝基苯酚( )的熔点,其原因是
)的熔点,其原因是_______ 。
(7)V元素在元素周期表________ 区;基态钛原子的核外价层电子排布式是________ 。
(8)在周期表中,与Al化学性质最相似的邻族元素是________ 。基态Al原子核外电子云轮廓图呈哑铃形的能级上电子数为________ 。在下列状态的铝元素中,电离最外层一个电子所需能量出高到低的顺序是________ 。(填标号)
A.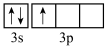 B.
B.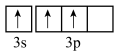 C.
C.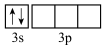 D.
D.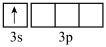
(9)CF2=CF2和ETFE分子中C的杂化轨道类型分别为________ 和________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________ 。
(1)基态F原子的价电子排布图(轨道表示式)为
(2)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(3)固态氟化氢中存在(HF)n形式,每个HF以氢键相连。画出(HF)3的链状结构
(4)N2F2(二氟氮烯)分子中,氮原子的杂化类型为sp2,则N2F2的结构式为
(5)NaHF2熔点为160℃(分解生成HF),电解可制得氟气,推测NaHF2中所含作用力的类型有
(6)BiOC1是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚(
 )等。对硝基苯酚的熔点高于邻硝基苯酚(
)等。对硝基苯酚的熔点高于邻硝基苯酚( )的熔点,其原因是
)的熔点,其原因是(7)V元素在元素周期表
(8)在周期表中,与Al化学性质最相似的邻族元素是
A.
 B.
B. C.
C. D.
D.
(9)CF2=CF2和ETFE分子中C的杂化轨道类型分别为
您最近一年使用:0次

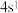 ,元素周期表的位置第
,元素周期表的位置第

