解题方法
1 . 某锂离子电池电解液中溶质的结构如图所示,X、Y、Z、W为原子序数依次增大的短周期元素,W原子的最外层电子数是内层电子数的一半。下列说法正确的是
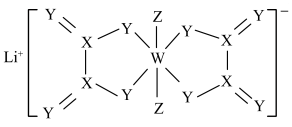
| A.原子半径:W>Z>Y |
| B.含X、Y元素的盐溶液可能呈碱性 |
| C.W的最高价氧化物对应水化合物是强酸 |
| D.Y和Z分别形成的最简单氢化物的稳定性:Y>Z |
您最近半年使用:0次
名校
2 . X、Y、Z、M、R、Q是短周期主族元素,部分信息如表所示:
(1)Z的单质与水反应的化学方程式为___________ 。
(2)Y与R相比,非金属性较强的是___________ (用元素符号表示),下列事实能证明这一结论的是___________ (填标号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:
c.最高价氧化物对应的水化物的酸性: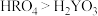
(3)根据表中数据推测Y的原子半径的范围:___________ 
___________  。
。
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙 丙+水,则丙的化学式为
丙+水,则丙的化学式为___________ (写出一种即可)。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色试验呈黄色 |
(2)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:

c.最高价氧化物对应的水化物的酸性:
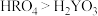
(3)根据表中数据推测Y的原子半径的范围:

 。
。(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙
 丙+水,则丙的化学式为
丙+水,则丙的化学式为
您最近半年使用:0次
名校
解题方法
3 . 食用碱是人们生活中常用的食品疏松剂和肉类嫩化剂,其成分为纯碱( )和小苏打(
)和小苏打( )。下列说法正确的是
)。下列说法正确的是
 )和小苏打(
)和小苏打( )。下列说法正确的是
)。下列说法正确的是A.离子半径: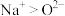 | B. 中的C为 中的C为 杂化 杂化 |
C.非金属性: | D.第一电离能: |
您最近半年使用:0次
名校
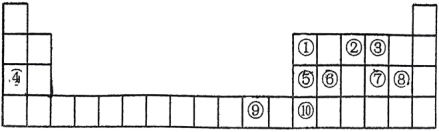
4 . 如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:__________ 种不同空间运动状态。⑨号元素在周期表中的位置是__________ ,基态时其最高能层的电子占据的原子轨道电子云轮廓为__________ 形。第二周期所有元素中第一电离能介于①②之间的有__________ 种。基态⑩原子的简化电子排布式__________ ,该元素位于__________ 区。
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式__________ ,该分子为__________ (填“极性”或“非极性”)分子。
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
| A.非金属性:②>③ |
| B.气态最简单氢化物的稳定性:③>⑦ |
| C.最高价氧化物对应的水化物的碱性:④>⑤ |
| D.最简单氢化物的沸点:③>⑦ |
您最近半年使用:0次
5 . 下列实验操作、现象和结论均正确的是
| A.向蛋白质溶液中加入饱和Na2SO4溶液,有沉淀出现:蛋白质发生了变性 |
| B.将一定量的SO3加入水玻璃中,产生白色胶状沉淀:非金属性:S>Si |
| C.室温下,用pH试纸测定浓度均为0.1mol/L的NaClO溶液、CH3COONa溶液的pH,NaClO溶液的pH较大。酸性:HClO>CH3COOH |
| D.向NaOH溶液中滴加MgCl2溶液,产生白色沉淀,继续滴加FeCl3溶液产生红褐色沉淀:Fe(OH)3的溶解度小于Mg(OH)2的溶解度 |
您最近半年使用:0次
6 . X、Y、Z、M和W五种短周期主族元素,原子序数依次增大,X元素最高化合价=|最低化合价|,Y在周期表中电负性最大,W与M、X相邻,基态Z的价电子层上只有1个电子,下列说法不正确的是
| A.单核离子半径:M<Z<Y |
| B.W与O原子可形成以平面三角形为结构单元的长链阴离子 |
| C.简单气态氢化物的沸点:Y>W>X |
| D.最高价氧化物中离子键成分百分数:Z>M>X |
您最近半年使用:0次
今日更新
|
149次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
7 . 下列实验装置不能达到实验目的的是

| A.甲:干燥氨气 |
| B.乙:验证溴单质的得电子能力强于碘单质 |
C.丙:用 做喷泉实验 做喷泉实验 |
D.丁:证明 溶液对 溶液对 分解的催化作用 分解的催化作用 |
您最近半年使用:0次
名校
解题方法
8 . 下列实验操作、实验现象以及得出的结论均正确的是
选项 | 操作 | 现象 | 结论 |
| 取碳粉与二氧化硅混合加热后的固体,溶于足量氢氧化钠溶液 | 有气泡产生 | 碳的非金属性比硅强 |
| 取一定量固体于试管中,加入浓 | 试纸变蓝 | 该固体为铵盐 |
| 取等体积同浓度的两份 |
| 探究浓度对化学反应速率的影响 |
| 向某溶液中加入过量的盐酸 | 产生使石灰水变浑浊的气体 | 该溶液中一定含 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
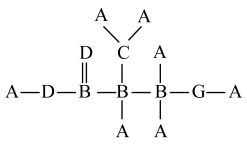
9 . 有机物半胱氨酸主要用于医药,化妆品、生化研究等方面,结构简式如图所示,其中A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素,E原子半径在短周期中最大,F的原子序数等于B和C的原子序数之和。回答下列问题:__________ 族。
(2)实验室保存E单质的方法是__________ 。
(3)在D、G的简单氢化物中,稳定性较强的是__________ (填化学式,下同);还原性较强的是__________ ;沸点较高的是__________ 。
(4)化合物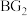 属于易燃液体,严禁在公共交通工具上携带,
属于易燃液体,严禁在公共交通工具上携带,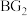 的电子式为
的电子式为__________ 。
(5)若将E、F的单质组成的混合物投入水中恰好完全反应,则E、F单质的质量之比为__________ 。
(6)AB两元素能组成电子数为42、相对分子质量为72的化合物M,M的分子式为__________ ,M的结构简式可能为__________ (若有多种可能,写出其中一种即可)。
(2)实验室保存E单质的方法是
(3)在D、G的简单氢化物中,稳定性较强的是
(4)化合物
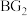 属于易燃液体,严禁在公共交通工具上携带,
属于易燃液体,严禁在公共交通工具上携带,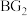 的电子式为
的电子式为(5)若将E、F的单质组成的混合物投入水中恰好完全反应,则E、F单质的质量之比为
(6)AB两元素能组成电子数为42、相对分子质量为72的化合物M,M的分子式为
您最近半年使用:0次
10 . I.1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:_______ (任写一种)。
(2)请写出元素⑦的氧化物与元素③的氢化物的水溶液反应的化学方程式_______ 。
(3)元素①和元素⑦最高价氧化物的水化物中酸性较强的是_______ (填化学式)。
II.硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(4)硅元素在自然界中通常以石英石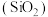 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。 的SiO2中含有Si-O键
的SiO2中含有Si-O键_______ 个。
(5)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”);
iii.由于硅酸盐组成比较复杂,通常用氧化物的形式表示:请用氧化物的形式表示钾云母K(Al3Si3O10)(OH)2的组成_______ 。
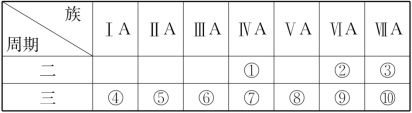
(2)请写出元素⑦的氧化物与元素③的氢化物的水溶液反应的化学方程式
(3)元素①和元素⑦最高价氧化物的水化物中酸性较强的是
II.硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(4)硅元素在自然界中通常以石英石
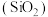 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 的SiO2中含有Si-O键
的SiO2中含有Si-O键(5)高纯硅单质可由石英砂(主要成分是
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:
ii.流程①焦炭体现了
iii.由于硅酸盐组成比较复杂,通常用氧化物的形式表示:请用氧化物的形式表示钾云母K(Al3Si3O10)(OH)2的组成
您最近半年使用:0次



 溶液,将湿润的红色石蕊试纸靠近试管口
溶液,将湿润的红色石蕊试纸靠近试管口
 溶液,同时加入等体积
溶液,同时加入等体积 的硫酸和
的硫酸和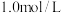 的硫酸
的硫酸


