1 . 有机化合物是生命活动的物质基础,也是能源开发和新型合成材料研制的基础物质。
(1)实验室制备乙炔的化学方程式为_______ ,为防止气体生成的速率过快,常用_______ 代替水来制取乙炔,制取的乙炔气体中常含有H2S等杂质,可将气体先通过_______ (填字母序号)洗气后再收集乙炔。
a.高锰酸钾溶液 b.溴水 c.硫酸铜溶液
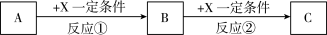
(2)芳香烃A可以合成两种有机化合物B和C,如下图所示:_______ ,写出反应②的化学方程式:_______ 。
(3)聚氯乙烯是生活中常用的塑料。工业生产聚氯乙烯的一种工艺路线如下:_______ ,反应类型为_______ ;反应②的反应类型为_______ 。
(1)实验室制备乙炔的化学方程式为
a.高锰酸钾溶液 b.溴水 c.硫酸铜溶液
(2)芳香烃A可以合成两种有机化合物B和C,如下图所示:

(3)聚氯乙烯是生活中常用的塑料。工业生产聚氯乙烯的一种工艺路线如下:

您最近一年使用:0次
名校
2 . 根据下列几种有机化合物回答问题:_______ (填序号)。
(2)③、④的官能团名称分别为_______ 、_______ 。
(3)按官能团分类,①属于_______ 类有机物,最多有_______ 个原子在同一平面上。
(4)⑤与氯气发生1,4加成的化学方程式为_______ 。
(5)④的同分异构体中,含苯环结构的共有_______ 种(不含④),其中核磁共振氢谱有5组峰的结构简式为_______ 。
(6)根据化合物②的结构特征,分析预测其可能的化学性质,参考I的示例,完成下表。
①CH3CH=CHCH3② CH2CH=CHCOOH③
CH2CH=CHCOOH③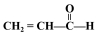 ④
④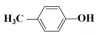 ⑤CH2=CHCH=CH2⑥
⑤CH2=CHCH=CH2⑥
(2)③、④的官能团名称分别为
(3)按官能团分类,①属于
(4)⑤与氯气发生1,4加成的化学方程式为
(5)④的同分异构体中,含苯环结构的共有
(6)根据化合物②的结构特征,分析预测其可能的化学性质,参考I的示例,完成下表。
| 序号 | 结构特征 | 可反应的试剂 | 反应形成的新结构 | 反应类型 |
| I | —COOH | CH3OH | —COOCH3 | 酯化反应 |
| II | 加成反应 |
您最近一年使用:0次
名校
3 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为___________ ;As的第一电离能比Se的第一电离能大的原因为___________ 。
(2) 中心原子的杂化类型是:
中心原子的杂化类型是:___________ , 的立体构型是
的立体构型是___________ 。
(3) 属于
属于___________ (填“极性”或“非极性”)分子;比较 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:___________ 。
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ ;若该晶胞密度为ρg⋅cm ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为___________ 。
(1)基态硒原子的价层电子排布式为
(2)
 中心原子的杂化类型是:
中心原子的杂化类型是: 的立体构型是
的立体构型是(3)
 属于
属于 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
 ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为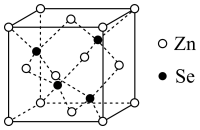
您最近一年使用:0次
2024-05-03更新
|
419次组卷
|
2卷引用:广东省茂名市高州中学2023-2024学年高二下学期期中考试化学试题
名校
4 . 下表为元素周期表的一部分,用化学用语回答下列问题:___________ 。
(2)⑥、⑦、⑧、③的简单离子的半径由大到小顺序为___________ 。(写离子符号)
(3)元素③、⑤、⑧组成的化合物是84消毒液的主要成分,可以在碱性条件下处理CN-,将CN-氧化成CO 和N2,写出反应的离子方程式
和N2,写出反应的离子方程式___________ 。
(4)将⑤和⑥单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积___________ L。最终获得溶液的物质的量浓度为___________ mol/L。
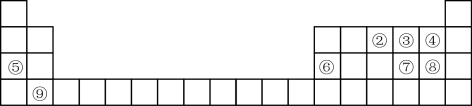
(2)⑥、⑦、⑧、③的简单离子的半径由大到小顺序为
(3)元素③、⑤、⑧组成的化合物是84消毒液的主要成分,可以在碱性条件下处理CN-,将CN-氧化成CO
 和N2,写出反应的离子方程式
和N2,写出反应的离子方程式(4)将⑤和⑥单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次
名校
5 . 硫及其化合物的“价-类”二维图体现了化学变化之美。
(1)自然界中有斜方硫和单斜硫,它们的关系是___________ (填“同位素”或“同素异形体”),二者转化属于化学变化。
(2)如图中属于酸性氧化物的物质是___________ (用化学式表示)。___________ 。
(4)如果有反应Z M,H2S
M,H2S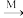 N,M是下列物质中的
N,M是下列物质中的___________ (填字母序号)。
a.Na2SO4 b.CuSO4 c.K2SO4 d.Fe2(SO4)3
Q可以是___________ (用化学式表示,写出至少2类物质)。
(5)S2Cl2和SCl2均为重要的化工产品。已知S4的结构式 和有关化学键能如下,则反应S4(g)+4Cl2(g)=4SCl2(g)
和有关化学键能如下,则反应S4(g)+4Cl2(g)=4SCl2(g)___________ (填“吸收”或“放出”)的能量为___________ mol。
(1)自然界中有斜方硫和单斜硫,它们的关系是
(2)如图中属于酸性氧化物的物质是

(4)如果有反应Z
 M,H2S
M,H2S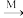 N,M是下列物质中的
N,M是下列物质中的a.Na2SO4 b.CuSO4 c.K2SO4 d.Fe2(SO4)3
Q可以是
(5)S2Cl2和SCl2均为重要的化工产品。已知S4的结构式
 和有关化学键能如下,则反应S4(g)+4Cl2(g)=4SCl2(g)
和有关化学键能如下,则反应S4(g)+4Cl2(g)=4SCl2(g)| 化学键 | S-S | S-Cl | Cl-Cl |
| 键能/(kJ/mol) | 266 | 255 | 243 |
您最近一年使用:0次
名校
解题方法
6 . 填空。
(1)键线式 表示的物质的分子式为
表示的物质的分子式为___________ 。
(2)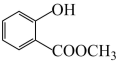 中含有的官能团的名称为
中含有的官能团的名称为___________ 、___________ 。
(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:___________ 。
(4)某芳香烃的结构为 ,它的分子式为
,它的分子式为___________ ,一氯代物有___________ 种。
(5)维生素C是重要的营养素,其分子结构如图所示。___________ 。
(1)键线式
 表示的物质的分子式为
表示的物质的分子式为(2)
 中含有的官能团的名称为
中含有的官能团的名称为(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:
(4)某芳香烃的结构为
 ,它的分子式为
,它的分子式为(5)维生素C是重要的营养素,其分子结构如图所示。

您最近一年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)表中元素,电负性最强的是___________ (填元素符号),J的元素名称为___________ 。N基态原子核外能级上有___________ 未成对电子。
(2)D元素原子的价电子排布图为___________ ,核外有___________ 种不同运动状态的电子。
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是___________ (填“极性”或“非极性”)分子。
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是___________ (填字母)。
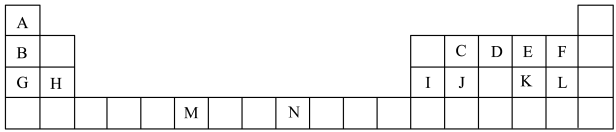
(1)表中元素,电负性最强的是
(2)D元素原子的价电子排布图为
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.  b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
您最近一年使用:0次
名校
解题方法
8 . 如图为元素周期表的一部分,请根据元素①~⑧在表中的位置,回答下列问题:

(1)请写出元素⑦在元素周期表中的位置___________ 。在上述元素的最高价氧化物对应的水化物中,酸性最强的是___________ (用化学式表示)。
(2)由元素①、④、⑤形成的化合物的电子式为___________ ,该物质属于___________ (填“离子”或“共价”)化合物。
(3)③、④、⑤、⑥的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)在发生地震后,地震灾区需要大量的“84消毒液”来消毒杀菌。84消毒液(主要成分为NaClO)和洁厕灵(主要成分为盐酸)混合使用会产生一种有毒气体,写出两者混合时发生反应的离子方程式:___________ 。
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
若A、B、C含同一金属元素,X为电解质溶液,可电离出 ,所有反应都在溶液中进行。B的化学式为
,所有反应都在溶液中进行。B的化学式为___________ ,X的化学式为___________ 。

(1)请写出元素⑦在元素周期表中的位置
(2)由元素①、④、⑤形成的化合物的电子式为
(3)③、④、⑤、⑥的简单离子半径由大到小的顺序是
(4)在发生地震后,地震灾区需要大量的“84消毒液”来消毒杀菌。84消毒液(主要成分为NaClO)和洁厕灵(主要成分为盐酸)混合使用会产生一种有毒气体,写出两者混合时发生反应的离子方程式:
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:

若A、B、C含同一金属元素,X为电解质溶液,可电离出
 ,所有反应都在溶液中进行。B的化学式为
,所有反应都在溶液中进行。B的化学式为
您最近一年使用:0次
名校
9 . 学以致用是学习化学的动力和源泉,掌握化学知识有助于我们更好地认识世界。回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是______ ,胶体和溶液的本质区别是_______ 。
(2)生铁是______ (填“混合物”或“化合物”)。通常合金的熔点_____ (填“高于”或“低于”)其组成单质的熔点。
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得: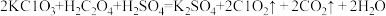 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为______ mol;该反应中的还原剂是______ (填化学式)。
(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=____ 。
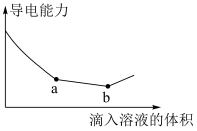
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是______ ,从a点到b点反应的离子方程式是______ ,解释b点之后导电能力上升的原因:______ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)生铁是
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得:
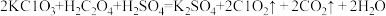 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是
您最近一年使用:0次
2024-01-28更新
|
111次组卷
|
4卷引用:广东省高州市某校2023-2024学年高一上学期期末模拟化学试题
名校
解题方法
10 . (一)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
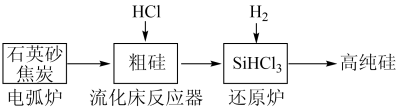
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:___________ 。
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:___________ 。
(二)某化学兴趣小组利用下列图示装置探究氨气的性质。
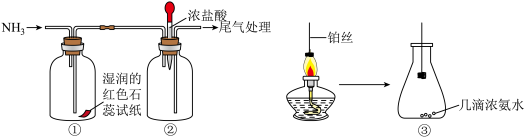
(3)①中湿润的红色石蕊试纸变蓝的原因:___________ (用化学方程式表示)。
(4)向②中滴入浓盐酸,现象为:___________ 。
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:___________ ,瓶中红棕色气体为___________ (填化学式)。
(三)某氨氮废水( 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:

(6)检验氨氮废水中含有 的方法是:
的方法是:___________ 。
(7)过程Ⅱ在硝化细菌作用下实现 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:___________ 。

(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl
 SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:(二)某化学兴趣小组利用下列图示装置探究氨气的性质。

(3)①中湿润的红色石蕊试纸变蓝的原因:
(4)向②中滴入浓盐酸,现象为:
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:
(三)某氨氮废水(
 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:
(6)检验氨氮废水中含有
 的方法是:
的方法是:(7)过程Ⅱ在硝化细菌作用下实现
 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
您最近一年使用:0次



