学以致用是学习化学的动力和源泉,掌握化学知识有助于我们更好地认识世界。回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是______ ,胶体和溶液的本质区别是_______ 。
(2)生铁是______ (填“混合物”或“化合物”)。通常合金的熔点_____ (填“高于”或“低于”)其组成单质的熔点。
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得: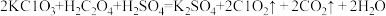 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为______ mol;该反应中的还原剂是______ (填化学式)。
(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=____ 。
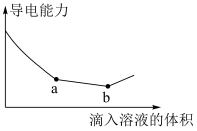
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是______ ,从a点到b点反应的离子方程式是______ ,解释b点之后导电能力上升的原因:______ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)生铁是
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得:
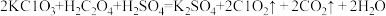 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是
更新时间:2024-01-28 20:48:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ\(1)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是 ____ 。
A.能全部透过滤纸 B.有丁达尔效应 C.所得液体呈胶状 D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是__________ 。
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:__ ,继续滴加至稀硫酸过量可观察到的现象是_____ ,写出上述反应的化学方程式____ 。
Ⅱ\给下图①~⑤选择适当的物质,使有连线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉。

(1)请推断它们的化学式分别为:②______ ,③ ______ ,⑤_______ 。
(2)写出下列序号之间的化学方程式:①和②:_______________ ,②和④:____________ ,③和④:______________ 。
A.能全部透过滤纸 B.有丁达尔效应 C.所得液体呈胶状 D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:
Ⅱ\给下图①~⑤选择适当的物质,使有连线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉。

(1)请推断它们的化学式分别为:②
(2)写出下列序号之间的化学方程式:①和②:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为3ClO-+2Fe3++xOH-=2FeO +3Cl-+yH2O。
+3Cl-+yH2O。
(1)上述反应中的x =___________ ,y=___________ 。
(2)上述反应中氧化剂为___________ ;还原产物为___________ 。
(3)由上述反应可知,氧化性强弱:ClO-___________ (填“>”或“<”,下同)FeO ;还原性强弱:Cl-
;还原性强弱:Cl-___________ Fe3+。
(4)请用单线桥法表示该反应中电子的转移情况:___________ 。
(5)已知:Na2FeO4在处理饮用水的过程中铁元素会被转化为Fe3+,进而Fe3+在水中产生Fe(OH)3胶体,Fe(OH)3胶体具有吸附性。
①Na2FeO4在处理饮用水的过程中___________ (填“发生了”或“未发生”)氧化还原反应。
②Fe(OH)3胶体呈___________ 色,写出区分胶体与溶液的操作及现象:___________ 。
③已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是___________ ,装置是下列中的___________ (填序号)。
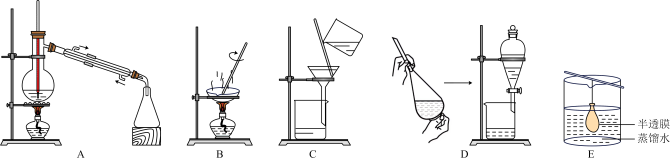
④现有10 mL明胶的水溶液与5mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜
能够透过半透膜___________ 。
 +3Cl-+yH2O。
+3Cl-+yH2O。(1)上述反应中的x =
(2)上述反应中氧化剂为
(3)由上述反应可知,氧化性强弱:ClO-
 ;还原性强弱:Cl-
;还原性强弱:Cl-(4)请用单线桥法表示该反应中电子的转移情况:
(5)已知:Na2FeO4在处理饮用水的过程中铁元素会被转化为Fe3+,进而Fe3+在水中产生Fe(OH)3胶体,Fe(OH)3胶体具有吸附性。
①Na2FeO4在处理饮用水的过程中
②Fe(OH)3胶体呈
③已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是

④现有10 mL明胶的水溶液与5mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜
能够透过半透膜
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有如下物质:①泥砂浆②NaCl溶液③NaHSO4固体④CO2⑤酒精⑥蒸馏水⑦CCl4⑧熔融的KNO3⑨红褐色的氢氧化铁胶体
(1)已知蒸馏水有非常微弱的导电性,以上物质中,属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)上述物质除⑥⑨外,能导电的是___________ 。
(3)分离①与②的混合液所用的方法是___________ ;鉴别②与⑨所用的方法是___________ 效应。
(4)物质③溶于水的电离方程式为___________ 。
(5)向⑨中逐滴滴加③的溶液,看到的现象是___________ 。
(1)已知蒸馏水有非常微弱的导电性,以上物质中,属于电解质的是
(2)上述物质除⑥⑨外,能导电的是
(3)分离①与②的混合液所用的方法是
(4)物质③溶于水的电离方程式为
(5)向⑨中逐滴滴加③的溶液,看到的现象是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】(1)质量之比为16:7:6的三种气体SO2、CO、NO,分子个数之比为_____________ ;氧原子个数之比为____________ ;相同条件下的体积之比为_____________ 。
(2)①标准状况下22.4 L CH4 ②1.5 mol NH3 ③1.806 x1024个H2O④标准状况下73g HCl所含H原子个数由多到少的顺序为______________ 。
(2)①标准状况下22.4 L CH4 ②1.5 mol NH3 ③1.806 x1024个H2O④标准状况下73g HCl所含H原子个数由多到少的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】计算。
(1)0.3molNH3分子中所含原子数与___________ 个H2O分子中所含原子数相等。
(2)标准状况下1.12LNH3所含氨分子物质的量为_______ ,电子数为_________ 。
(3)3.9gNa2X含有Na+0.1mol,则Na2X的摩尔质量为___________ ,X的相对原子质量为___________ 。
(4)同温同压下,O2、SO2、SO3的质量之比为1∶2∶5,则它们所含的氧原子数之比为___ ,密度之比为_______ 。
(5)amLKAl(SO4)2溶液中含有Al3+xg,加水稀释至bmL,则稀释后所得溶液中c( )为
)为______ mol·L-1。
(6)14gC2H4与C4H8的混合物所含质子的物质的量为___________ 。
(1)0.3molNH3分子中所含原子数与
(2)标准状况下1.12LNH3所含氨分子物质的量为
(3)3.9gNa2X含有Na+0.1mol,则Na2X的摩尔质量为
(4)同温同压下,O2、SO2、SO3的质量之比为1∶2∶5,则它们所含的氧原子数之比为
(5)amLKAl(SO4)2溶液中含有Al3+xg,加水稀释至bmL,则稀释后所得溶液中c(
 )为
)为(6)14gC2H4与C4H8的混合物所含质子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)下面是某同学推导“1molNa 的质量在数值上等于 Na 的相对原子质量,单位取 g”的过 程,请你补充完整。【其中 m(Na 原子)表示一个 Na 原子的质量,m(12C)表示一个 12C原子的质量 ,Ar 表示 Na 的相对原子质量,NA 表示阿伏伽德罗常数】
因为:m(Na 原子)=1/12m(12C)Ar,所以:1molNa 原子的质量=1/12________ Ar=1/12_____ Ar=Ar g
(2)由 CO2 与 CO 组成的混合气体对 H2 的相对密度 20,则混合气体中 CO2 的体积分数为_____ ,CO 的质量分数_______
(3)标准状况下,336L 的 NH3 溶于 1L 水中,若该溶液的密度为 ag/cm3,则其物质的量浓度为。将上述氨水全部转化为 NH4CL,所需 2mol/L 的盐酸的体积为_____ (NH3+HCl=NH4Cl)。
因为:m(Na 原子)=1/12m(12C)Ar,所以:1molNa 原子的质量=1/12
(2)由 CO2 与 CO 组成的混合气体对 H2 的相对密度 20,则混合气体中 CO2 的体积分数为
(3)标准状况下,336L 的 NH3 溶于 1L 水中,若该溶液的密度为 ag/cm3,则其物质的量浓度为。将上述氨水全部转化为 NH4CL,所需 2mol/L 的盐酸的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
I.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨。
(1)以上物质中属于电解质的是________ (填序号,下同);属于非电解质的是_______ 。
(2)以上物质属于纯净物且能导电的是________ 。
II.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:

(3)加水的烧杯为________ 。
(4)向烧杯A滴入Ba(OH)2溶液,溶液导电性________ 。
(5)H3PO4是三元酸,能生成NaH2PO4、Na2HPO4两种酸式盐和Na3PO4一种正盐。磷还有一种含氧酸叫亚磷酸(H3PO3)。已知:H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。那么Na2HPO3为________ (填“正盐”或“酸式盐”);写出H3PO3与少量NaOH溶液反应的离子方程式________ 。
I.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨。
(1)以上物质中属于电解质的是
(2)以上物质属于纯净物且能导电的是
II.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:

(3)加水的烧杯为
(4)向烧杯A滴入Ba(OH)2溶液,溶液导电性
| A.变强 | B.变弱 | C.先变弱后变强 | D.先变强后变弱 |
(5)H3PO4是三元酸,能生成NaH2PO4、Na2HPO4两种酸式盐和Na3PO4一种正盐。磷还有一种含氧酸叫亚磷酸(H3PO3)。已知:H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。那么Na2HPO3为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】①铝②盐酸③碳酸④液氨⑤硝酸钾⑥干冰⑦酒精 ⑧液态氢氧化钠⑨熔融硫酸钡⑩氯水⑪明矾⑫氢氧化铁胶体
(1)属于强电解质的是___________________________ 。(填序号, 下同)
(2)属于非电解质的是___________________________ 。
(3)能导电的是________________________________ 。
(4)除去硝酸钾固体中少量的KCl,选择正确的操作并排序___________________________ 。
①过滤②趁热过滤 ③固体溶于水④冷却结晶 ⑤蒸发浓缩
(5)⑪溶于水后的电离方程式为:_____________________________ 。
(1)属于强电解质的是
(2)属于非电解质的是
(3)能导电的是
(4)除去硝酸钾固体中少量的KCl,选择正确的操作并排序
①过滤②趁热过滤 ③固体溶于水④冷却结晶 ⑤蒸发浓缩
(5)⑪溶于水后的电离方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】向稀硫酸溶液中逐滴加入Ba(OH)2.请完成下列问题:
(1)写出反应的离子方程式_______________________________________ ;
(2)下列三种情况下,离子方程式与(1)相同的是________ (填序号)
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入Ba(OH)2直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用图中的曲线表示是________ (填序号);

(1)写出反应的离子方程式
(2)下列三种情况下,离子方程式与(1)相同的是
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至
 恰好完全沉淀
恰好完全沉淀C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入Ba(OH)2直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用图中的曲线表示是

您最近一年使用:0次
【推荐1】实验室用50mL浓盐酸和足量的氯酸钾固体共热制取氯气,其中氯气中的氯元素部分来自氯酸钾,部分来自盐酸,该反应的化学方程式为: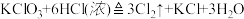
(1)用双线桥法表示电子转移的方向和数目_____________________________
(2)浓盐酸在此反应中体现的化学性质是________ (填写编号)
①挥发性 ②酸性 ③氧化性 ④还原性
(3)当反应过程转移电子数为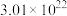 时,产生的
时,产生的 在标准状况下的体积为
在标准状况下的体积为________ mL。
(4)当反应结束时,生成氯气为0.15mol,若反应中HCl的利用率为50%,则原浓盐酸的物质的量浓度为________ 。
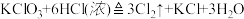
(1)用双线桥法表示电子转移的方向和数目
(2)浓盐酸在此反应中体现的化学性质是
①挥发性 ②酸性 ③氧化性 ④还原性
(3)当反应过程转移电子数为
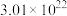 时,产生的
时,产生的 在标准状况下的体积为
在标准状况下的体积为(4)当反应结束时,生成氯气为0.15mol,若反应中HCl的利用率为50%,则原浓盐酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】H5IO6是白色晶体,易溶于水,在强酸溶液中能与Mn2+发生反应:_______Mn2++_______H5IO6=_______MnO +_______IO
+_______IO +_______H++_______H2O
+_______H++_______H2O
(1)配平上述离子反应_______ 。
(2)根据以上离子方程式判断,H5IO6是_______ (填“易”或“难”,下同)电离物质,HIO3是_______ 电离物质。
(3)上述反应中,被氧化的元素是_______ (填元素符号),当1molMn2+参加反应时,转移电子的物质的量为_______ 。
 +_______IO
+_______IO +_______H++_______H2O
+_______H++_______H2O(1)配平上述离子反应
(2)根据以上离子方程式判断,H5IO6是
(3)上述反应中,被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.草酸与高锰酸钾在酸性条件下能够发生如下反应:Mn +H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:
(1)该反应中氧化剂和还原剂的物质的量之比为_______ 。
(2)如果研究催化剂对化学反应速率的影响,使用实验_______ 和_______ (用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验_______ 和_______ 。
(3)对比实验Ⅰ和Ⅳ,可以研究_______ 对化学反应速率的影响,实验Ⅳ加入1 mL蒸馏水的目的是_______ 。
II.某可逆反应在容积为5 L的密闭容器中进行,在从0~3 min内各物质的量的变化情况如图所示(A、B、C均为气体)。
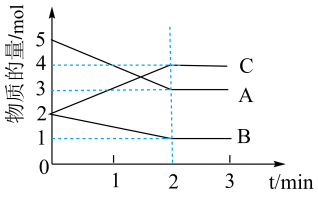
(4)该反应的化学方程式为_______ 。
(5)反应开始至2分钟时,B的平均反应速率为_______ 。
(6)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是_______ (填序号)。
①降低温度 ②加入催化剂 ③增大容器体积
 +H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:| 实验编号 | 10%硫酸溶液的体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | — |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | — |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(2)如果研究催化剂对化学反应速率的影响,使用实验
(3)对比实验Ⅰ和Ⅳ,可以研究
II.某可逆反应在容积为5 L的密闭容器中进行,在从0~3 min内各物质的量的变化情况如图所示(A、B、C均为气体)。

(4)该反应的化学方程式为
(5)反应开始至2分钟时,B的平均反应速率为
(6)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂 ③增大容器体积
您最近一年使用:0次



