1 . Ⅰ.某些有机化合物的模型如图所示。回答下列问题:
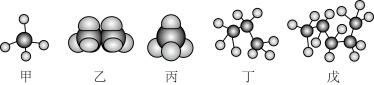
(1)属于填充模型的是___________ (填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
(2)表示同一种有机化合物的是___________ 。
(3)存在同分异构体的是___________ ,请写出其任意一种同分异构体的结构简式___________ 。
Ⅱ.农药波尔多液的主要成分是CuSO4,下列两个反应都有CuSO4生成。
①Cu+2H2SO4=CuSO4+SO2+2H2O ②CuO+H2SO4=CuSO4+H2O
请回答下列问题:
(4)从分类角度来看CuSO4属于___________。
(5)上述两个反应属于氧化还原反应的是___________ (填序号),其中氧化剂是___________ 。
(6)反应①的副产物SO2是大气污染物,可用NaOH溶液吸收,反应方程式是___________ 。

(1)属于填充模型的是
(2)表示同一种有机化合物的是
(3)存在同分异构体的是
Ⅱ.农药波尔多液的主要成分是CuSO4,下列两个反应都有CuSO4生成。
①Cu+2H2SO4=CuSO4+SO2+2H2O ②CuO+H2SO4=CuSO4+H2O
请回答下列问题:
(4)从分类角度来看CuSO4属于___________。
| A.氧化物 | B.盐 | C.碱 | D.酸 |
(5)上述两个反应属于氧化还原反应的是
(6)反应①的副产物SO2是大气污染物,可用NaOH溶液吸收,反应方程式是
您最近一年使用:0次
2 . 回答下列问题。
(1)H2S、CH4、H2O的沸点由高到低的顺序为:___________ 。
(2)HCN(H-C≡N)的一个分子中σ键和π键的个数比为:___________ 。
(3)SO 的中心原子采取
的中心原子采取___________ 杂化,空间结构是___________ 。
(4)基态硅原子最外层的电子排布图为:___________ 。
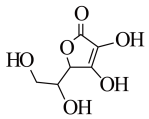
(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性___________ (填“难溶于水”或“易溶于水”)。
(6)LiBH4中不存在的作用力有___________。
(7)氢化锂(LiH)中负离子半径大于正离子半径,其原因是___________ 。
(1)H2S、CH4、H2O的沸点由高到低的顺序为:
(2)HCN(H-C≡N)的一个分子中σ键和π键的个数比为:
(3)SO
 的中心原子采取
的中心原子采取(4)基态硅原子最外层的电子排布图为:
(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性

(6)LiBH4中不存在的作用力有___________。
| A.离子键 | B.极性共价键 | C.非极性共价键 | D.分子间作用力 |
(7)氢化锂(LiH)中负离子半径大于正离子半径,其原因是
您最近一年使用:0次
3 . 回答下列问题。
(1)①比较键长大小:C-H___________ N-H___________ H-O(用“>”或“<”填空)。
②比较键能大小:C-H___________ N-H___________ H-O(用“>”或“<”填空)。
(2)乙烯分子中的碳原子均采取___________ 杂化,碳原子与氢原子形成σ键,两碳原子之间形成双键(1个___________ 键和1个___________ 键)。
(3)乙烯分子中的所有原子都位于___________ ,相邻两个键之间的夹角约为___________ 。
(4)铁原子的价层电子排布式为:___________ 。
(1)①比较键长大小:C-H
②比较键能大小:C-H
(2)乙烯分子中的碳原子均采取
(3)乙烯分子中的所有原子都位于
(4)铁原子的价层电子排布式为:
您最近一年使用:0次
解题方法
4 . 回答下列问题。
(1)基态N原子的电子排布式为___________ 。基态P原子中,电子占据的最高能级原子轨道形状为___________ 。
(2)H2O中心原子杂化轨道类型为___________ ,说明H2O沸点大于H2S的原因___________ 。
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为___________ (填“发射”或“吸收”)光谱。
(4)下列氧原子电子排布图表示的状态中,能量最高的是___________ (填标号,下同),能量最低的是___________ 。
A.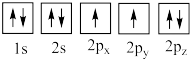 B.
B.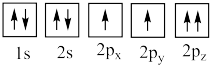
C. D.
D.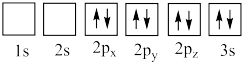
(1)基态N原子的电子排布式为
(2)H2O中心原子杂化轨道类型为
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为
(4)下列氧原子电子排布图表示的状态中,能量最高的是
A.
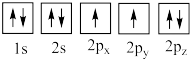 B.
B.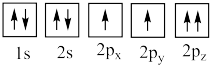
C.
 D.
D.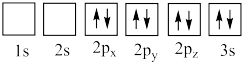
您最近一年使用:0次
2024-03-22更新
|
486次组卷
|
2卷引用:广东省普宁市勤建学校2023-2024学年高二下学期第一次月考化学试题
解题方法
5 . 回答下列问题
(1)按要求填空:①石墨②CaCO3③盐酸④CO2⑤CaO⑥KOH(熔融)⑦Al(OH)3⑧Fe(NO3)3⑨酒精⑩冰醋酸⑪Ca(OH)2;以上指定物质中,属于非电解质的是_______ 属于强电解质的是_______ 能导电的是_______
(2)书写下列物质的电离方程式
①亚硫酸_______
②氢氧化铁_______
③硫酸钡_______
④硫酸氢钾在水溶液中_______
(3)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,写出表甲醇燃烧热的化学方程式_______ 。
(4)反应N2(g)+3H2(g) 2NH3(g) ΔH=akJ/mol。根据下表中所列键能数据计算a的数值为
2NH3(g) ΔH=akJ/mol。根据下表中所列键能数据计算a的数值为_______ 。
(5)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ/mol
写出:C(s,石墨)和H2(g)生成1molC2H2(g)热化学方程式:_______ 。
(1)按要求填空:①石墨②CaCO3③盐酸④CO2⑤CaO⑥KOH(熔融)⑦Al(OH)3⑧Fe(NO3)3⑨酒精⑩冰醋酸⑪Ca(OH)2;以上指定物质中,属于非电解质的是
(2)书写下列物质的电离方程式
①亚硫酸
②氢氧化铁
③硫酸钡
④硫酸氢钾在水溶液中
(3)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,写出表甲醇燃烧热的化学方程式
(4)反应N2(g)+3H2(g)
 2NH3(g) ΔH=akJ/mol。根据下表中所列键能数据计算a的数值为
2NH3(g) ΔH=akJ/mol。根据下表中所列键能数据计算a的数值为| 化学键 | H-H | N-H | N≡N |
| 键能kJ/mol | 436 | 391. | 945 |
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ/mol
写出:C(s,石墨)和H2(g)生成1molC2H2(g)热化学方程式:
您最近一年使用:0次
6 . 2021年10月16日,神舟十三号载人飞船与“天和”核心舱成功径向交会对接。化学助力我国航天事业发展,借助元素周期表可以认识各种材料的组成、结构和性质。a~h8种元素在元素周期表中的位置如下:
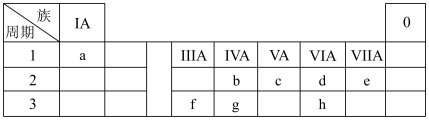
(1)a的单质常用作火箭推进剂,该过程中a单质对应的产物为_______ (填化学式)。
(2)g单质在太阳能电池和芯片制造等领域有着重要应用,g最高价氧化物的化学式为_______ ;b的氧化物含有的化学键类型为_______ 。
(3)飞船的制造使用了f的合金,f的简单离子结构示意图为_______ ,比较f和g原子半径大小:f_______ (填“>”“<”或“=”)g。
(4)请写出b与足量d完全反应生成的化合物的电子式:_______ 。元素c与元素e所形成的简单氢化物的稳定性大小:c_______ (填“>”“<”或“=”)e。

(1)a的单质常用作火箭推进剂,该过程中a单质对应的产物为
(2)g单质在太阳能电池和芯片制造等领域有着重要应用,g最高价氧化物的化学式为
(3)飞船的制造使用了f的合金,f的简单离子结构示意图为
(4)请写出b与足量d完全反应生成的化合物的电子式:
您最近一年使用:0次
7 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式_______ 。
(2)小苏打的化学式为_______ ,可用于治疗胃酸过多。
(3)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①漂白粉能杀菌消毒是因有强_______ 性;氯气与水反应制氯水的化学方程式为_______ 。
②某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

浓H2SO4的作用是_______ 。与研究目的直接相关的实验现象是_______ 。该实验设计存在事故隐患,应在D处增加一装置,请在D处画出装置图并标明所装试剂_______ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式
(2)小苏打的化学式为
(3)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①漂白粉能杀菌消毒是因有强
②某同学设计了下图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。回答下列问题:

浓H2SO4的作用是
您最近一年使用:0次
8 . 已知下列两个反应:
反应Ⅰ:
反应Ⅱ:
反应Ⅰ的化学平衡常数 与温度的关系如下表所示:
与温度的关系如下表所示:
请回答下列问题:
(1)若反应Ⅱ的化学平衡常数为 ,则
,则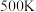 时,
时,
___________ 。
(2)反应Ⅰ的
___________ (填“>”、“<”或“=”)0,依据是:___________ 。
(3)温度为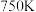 时,向某恒容密闭容器中通入一定量的
时,向某恒容密闭容器中通入一定量的 和
和 进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。
进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。
(4)工业上利用电解饱和食盐水制取 和
和 ,其化学方程式为:
,其化学方程式为:___________ ,电解结束后溶液
___________ (填“减小”、“不变”或“增大”)。
反应Ⅰ:

反应Ⅱ:

反应Ⅰ的化学平衡常数
 与温度的关系如下表所示:
与温度的关系如下表所示: | 500 | 750 | 1000 | 1300 |
 | 0.5 | 0.64 | 1 | 1.5 |
(1)若反应Ⅱ的化学平衡常数为
 ,则
,则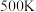 时,
时,
(2)反应Ⅰ的

(3)温度为
 时,向某恒容密闭容器中通入一定量的
时,向某恒容密闭容器中通入一定量的 和
和 进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。
进行反应Ⅱ,下列能判断反应Ⅱ已达到平衡的依据是___________(填标号)。| A.容器中的压强不再改变 |
| B.混合气体的密度不再改变 |
C.每断裂 键,同时断裂 键,同时断裂 键 键 |
D. |
 和
和 ,其化学方程式为:
,其化学方程式为:
您最近一年使用:0次
名校
解题方法
9 . 2023年10月央视的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
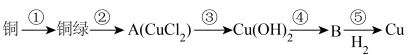
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:______
(2)A、B在无色火焰上灼烧时,其焰色______ (填“相同”或“不相同”),该原理是______ (填“物理”或“化学”)变化。
(3)完成步骤②和③可选用的试剂分别为______ 、______ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少______ ?(写出计算过程)
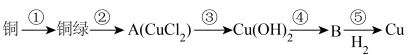
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)A、B在无色火焰上灼烧时,其焰色
(3)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少
您最近一年使用:0次
名校
解题方法
10 . 现有以下物质:①酒精②硫酸氢钠溶液③熔融Al2O3④液氯⑤CO2⑥硫酸铝固体⑦石墨⑧NaHCO3固体,按要求完成下列填空。
(1)上述物质可导电的有______ ;上述物质属于电解质的有______ (填写相应的编号);
(2)写出⑥在水溶液中的电离方程式______ 。
(3)写出②和⑧发生反应的离子方程式______ 。
(4)0.5molAl2O3的质量为______ 。
(1)上述物质可导电的有
(2)写出⑥在水溶液中的电离方程式
(3)写出②和⑧发生反应的离子方程式
(4)0.5molAl2O3的质量为
您最近一年使用:0次



