回答下列问题。
(1)基态N原子的电子排布式为___________ 。基态P原子中,电子占据的最高能级原子轨道形状为___________ 。
(2)H2O中心原子杂化轨道类型为___________ ,说明H2O沸点大于H2S的原因___________ 。
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为___________ (填“发射”或“吸收”)光谱。
(4)下列氧原子电子排布图表示的状态中,能量最高的是___________ (填标号,下同),能量最低的是___________ 。
A.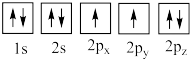 B.
B.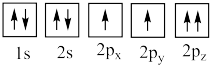
C. D.
D.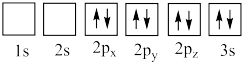
(1)基态N原子的电子排布式为
(2)H2O中心原子杂化轨道类型为
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为
(4)下列氧原子电子排布图表示的状态中,能量最高的是
A.
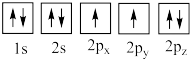 B.
B.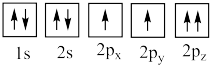
C.
 D.
D.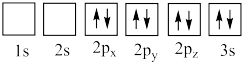
更新时间:2024-03-22 18:18:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】基态与激发态

(1)基态原子:处于___________ 状态的原子,
(2)基态原子___________ ,电子跃迁到___________ ,变为激发态原子;
(3)电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将___________ ;
(4)___________ 是电子跃迁释放能量的重要形式之一。

(1)基态原子:处于
(2)基态原子
(3)电子从较高能量的激发态跃迁到较低能量的激发态乃至基态时,将
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)下列物质变化,只与范德华力有关的是___ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:
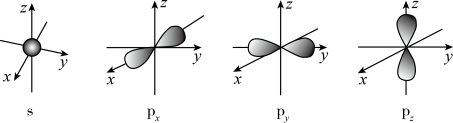
请回答下列问题:
s电子的原子轨道呈__ 形,每个s能级有__ 个原子轨道;p电子的原子轨道呈___ 形,每个p能级有___ 个原子轨道.
(3)Na、Mg、Al第一电离能的由大到小的顺序:___ 。
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是___ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:

请回答下列问题:
s电子的原子轨道呈
(3)Na、Mg、Al第一电离能的由大到小的顺序:
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】运用核外电子排布和元素周期律(表)相关规律或知识,回答下列相关的问题。
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断:违反了泡利原理的是____ 。
①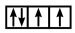 ②
②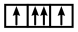 ③
③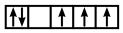 ④
④ ⑤
⑤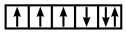
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为____ 。
(3)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na____ Mg。
②电负性:O____ F。
③能量高低:ns____ (n+1)s。
④除O、F元素外,主族序数____ 价电子数。
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断:违反了泡利原理的是
①
 ②
② ③
③ ④
④ ⑤
⑤
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
(3)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na
②电负性:O
③能量高低:ns
④除O、F元素外,主族序数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题
(1)氮原子价层电子对的轨道表达式(电子排布图)为_____________ 。
(2)基态Ni原子的电子排布式为______ ,该元素位于元素周期表的第_______ 族。
(3)基态Fe原子有________ 个未成对电子,Fe3+的电子排布式为________
(4)C、N、O三种元素第一电离能从小到大的顺序为_________ 。
(5)基态Ti原子核外电子排布的能量最高的能级符号是______ 。与钛同周期的元素中,基态原子的未成对电子数与钛相同的有________ 种。
(6)磷和砷是同一主族的元素,第一电离能:磷___________ 砷(填“>”“<”或“=”,下同),它们形成的氢化物的沸点:PH3___________ AsH3,原因是____________
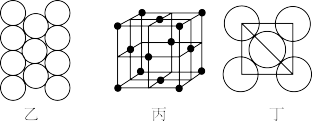
(7)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。若已知Al的原子半径为dnm,NA代表阿伏加 德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目_____ 个;Al晶体的密度为_____ g/cm3(用字母表示)
(1)氮原子价层电子对的轨道表达式(电子排布图)为
(2)基态Ni原子的电子排布式为
(3)基态Fe原子有
(4)C、N、O三种元素第一电离能从小到大的顺序为
(5)基态Ti原子核外电子排布的能量最高的能级符号是
(6)磷和砷是同一主族的元素,第一电离能:磷
(7)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。若已知Al的原子半径为dnm,NA代表阿伏加 德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________ 。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_______ ,提供孤电子对的成键原子是________ 。
(3)单质铜及镍都是由______ 键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol–1、INi=1 753 kJ·mol–1,ICu> INi的原因是_______________________ 。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为
(3)单质铜及镍都是由
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铜及其化合物在工农业生产中有广泛的应用。
I. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(1)向 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有_______ (填字母)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键 E.氢键
(2) 可以与乙二胺
可以与乙二胺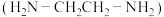 形成配离子,如图所示:
形成配离子,如图所示:
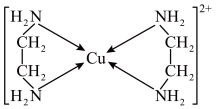
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______ 。
(2)该配离子中的配体数与配位数之比为_______ 。
II.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(3)下列物质中,属于顺磁性物质的是_______(填字母)。
III.请回答以下问题:
(4)① ②
② ③
③
将上述物质键角按由大到小的顺序排列:_______ (用序号表示)。
(5)三甲胺(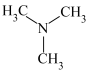 )和异丙胺(
)和异丙胺(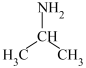 )的沸点大小关系为:三甲胺
)的沸点大小关系为:三甲胺_______ (填“>”“<”或“=”)异丙胺,原因是_______ 。
(6)基态原子的核外电子填充在5个轨道中的元素有_______ 种。
I.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(1)向
 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有A.离子键 B.金属键 C.极性共价键 D.非极性共价键 E.氢键
(2)
 可以与乙二胺
可以与乙二胺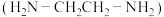 形成配离子,如图所示:
形成配离子,如图所示:
(1)C、N、O三种元素的第一电离能从大到小的顺序为
(2)该配离子中的配体数与配位数之比为
II.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(3)下列物质中,属于顺磁性物质的是_______(填字母)。
A. | B. | C. | D. |
III.请回答以下问题:
(4)①
 ②
② ③
③
将上述物质键角按由大到小的顺序排列:
(5)三甲胺(
 )和异丙胺(
)和异丙胺( )的沸点大小关系为:三甲胺
)的沸点大小关系为:三甲胺(6)基态原子的核外电子填充在5个轨道中的元素有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】新质生产力的底色是绿色低碳。而化学,在绿色低碳方面当仁不让,新质生产力涵盖的产业链很多与化学化工相关,合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为___________ 。
②自然固氮过程中生成的NO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②基态铬原子的电子排布式为___________ 。
③下列比较正确的是___________ 。
A.第一电离能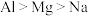 B.熔点:
B.熔点: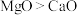
C.离子半径: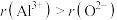 D.键角:
D.键角: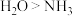
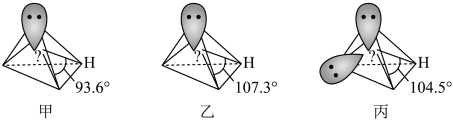
④NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是___________ 、___________ 。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为
②自然固氮过程中生成的NO
 的VSEPR模型名称为
的VSEPR模型名称为(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②基态铬原子的电子排布式为
③下列比较正确的是
A.第一电离能
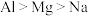 B.熔点:
B.熔点: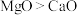
C.离子半径:
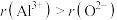 D.键角:
D.键角:
④NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】光刻胶常含C、N等元素,在基态C原子中,核外存在_______ 对自旋方向相反的电子,N的3个2p轨道的取向为_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在1778年,法国马厚比无意中发现用硫酸钠、木炭和铁(后改用氧化铁)一起灼烧,再用水滗取可得到纯碱。这一发明使他建立起世界上第一座纯碱工厂。
2Fe2O3+3NazSO4+16C Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+O2+2CO2 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3
回答下列问题:
(1)基态铁原子的价层电子排布式为_______ ,其3d能级上有_______ 个运动状态不同的电子。
(2)基态 原子核外有
原子核外有_______ 对自旋方向相反的电子对。基态钠原子核外电子占据能量最高的能级符号是_______ 。
(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是_______ (填化学式)。C、O、F三种元素中,电负性由大到小的顺序为_______ 。
(4)某同学书写的基态碳原子轨道表示式为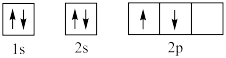 ,他违背了
,他违背了_______ 。
2Fe2O3+3NazSO4+16C
 Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑Na6Fe4S3+O2+2CO2
 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3回答下列问题:
(1)基态铁原子的价层电子排布式为
(2)基态
 原子核外有
原子核外有(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是
(4)某同学书写的基态碳原子轨道表示式为
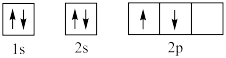 ,他违背了
,他违背了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】早期发现的一种天然二十面体准晶颗粒由三种Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过_______________ 方法区分晶体、准晶体和非晶体。
(2)基态Fe原子有_________ 个未成对电子,Fe3+的电子排布式为_______________ 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为_______________ 。
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为____________ ,乙醛分子中各元素的电负性由大到小的顺序为_______________ 。乙酸的沸点明显高于乙醛,其主要原因是_____________________________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________ 个铜原子。
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为__________ 。列式表示Al单质的密度_______________ g·cm-3。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态Fe原子有
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以Fe和BN为原料合成的铁氮化合物在光电子器材领域有广泛应用。
(1)基态Fe原子核外电子排布式为___ 。
(2)硼在室温下与F2反应生成BF3,BF3的空间构型为__ 。写出一种与BF3互为等电子体的阴离子:___ 。
(3)以氨硼烷(NH3BH3)为原料可以获得BN。氨硼烷的结构式为__ (配位键用“→”表示),氨硼烷能溶于水,其主要原因是__ 。
(4)如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为__ 。

(1)基态Fe原子核外电子排布式为
(2)硼在室温下与F2反应生成BF3,BF3的空间构型为
(3)以氨硼烷(NH3BH3)为原料可以获得BN。氨硼烷的结构式为
(4)如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为

您最近一年使用:0次

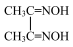 )作用生成腥红色配合物沉淀A。丁二酮肟分子中碳原子的杂化轨道类型有
)作用生成腥红色配合物沉淀A。丁二酮肟分子中碳原子的杂化轨道类型有

